Clear Sky Science · it
Il monossido di azoto induce la morte cellulare mediata da p53 nelle cellule epiteliali nasali umane
Perché conta la prima linea del tuo naso
I passaggi nasali sono più che semplici condotti d’aria; costituiscono uno scudo vivente che aiuta a tenere virus, batteri e agenti inquinanti fuori dal corpo e dal cervello. Durante infezioni e infiammazioni croniche, questo scudo è investito da segnali chimici che combattono i germi ma possono anche danneggiare le nostre stesse cellule. Una di queste molecole, il monossido di azoto, è al contempo un noto difensore e un elemento dannoso. Questo studio pone una domanda semplice ma importante: quando il monossido di azoto persiste a livelli elevati intorno alla mucosa nasale, indebolisce silenziosamente questa prima linea di difesa?
Un gas utile con un lato oscuro
Il monossido di azoto è una piccola molecola gassosa che il nostro organismo usa per dilatare i vasi sanguigni, facilitare la comunicazione nervosa e potenziare le difese immunitarie. Le cellule immunitarie ne rilasciano getti per aiutare a uccidere i microrganismi invasori e, in quantità normali, supporta la funzionalità sana. Ma in reazioni immunitarie intense o prolungate il monossido di azoto può essere prodotto in eccesso e reagire con l’ossigeno formando specie chimiche altamente reattive. Queste possono danneggiare il DNA e altri componenti cellulari vitali, trasformando un’arma utile in una fonte di danno collaterale. Poiché la mucosa nasale è esposta direttamente all’ambiente esterno ed è un punto di ingresso principale per virus respiratori come SARS-CoV-2, capire come un’esposizione prolungata al monossido di azoto influisca su queste cellule è cruciale.
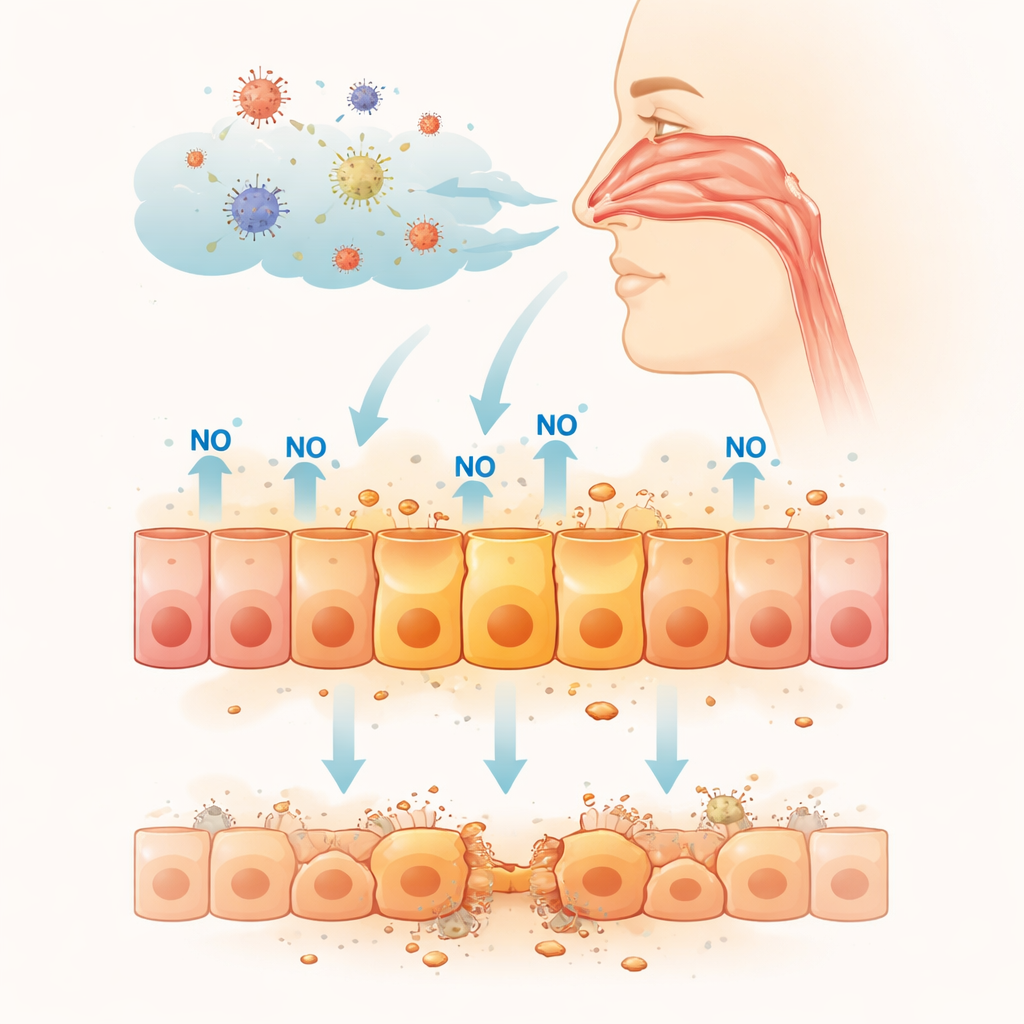
Testare l’esposizione prolungata nelle cellule nasali
Per indagare questo aspetto, i ricercatori hanno usato una linea cellulare epiteliale nasale umana coltivata in laboratorio, un modello largamente impiegato per rappresentare la barriera nasale. Hanno esposto queste cellule per fino a tre giorni a un composto che rilascia monossido di azoto a livelli simili a quelli riportati nei tessuti infiammati. Con il tempo, la crescita cellulare rallentava e aumentava la mortalità cellulare, indicando che un’esposizione sostenuta al monossido di azoto è tossica per questo modello nasale. Per scoprire cosa accadeva all’interno delle cellule, il team ha analizzato quali geni venivano attivati o repressi dopo 48 ore di esposizione. Centinaia di geni hanno modificato la loro attività, e molti di quelli più fortemente attivati si sono rivelati collegati a una proteina guardiana centrale della cellula chiamata p53, che monitora i danni al DNA e controlla se le cellule si riparano, smettono di dividersi o si autodistruggono.
Come il guardiano della cellula si rivolge contro le cellule danneggiate
Esperimenti di follow-up hanno confermato che il monossido di azoto induce l’accumulo della proteina p53 nelle cellule nasali nel giro di poche ore, un segno distintivo della sua attivazione. All’aumentare dei livelli di p53 aumentava anche l’attività di diversi suoi geni bersaglio che indirizzano le cellule verso la morte programmata e l’arresto del ciclo cellulare. I marcatori dell’apoptosi, il programma ordinato di autodistruzione che frammenta le cellule in parti piccole e smaltibili, sono aumentati nel tempo. Quando gli scienziati hanno usato un farmaco che blocca specificamente la capacità di p53 di regolare i geni, sia l’aumento dei geni bersaglio di p53 sia la quantità di cellule morte sono stati significativamente ridotti. Ciò ha dimostrato che p53 è un importante motore della perdita di cellule epiteliali nasali indotta dal monossido di azoto, pur essendo probabile il contributo anche di altre vie molecolari.
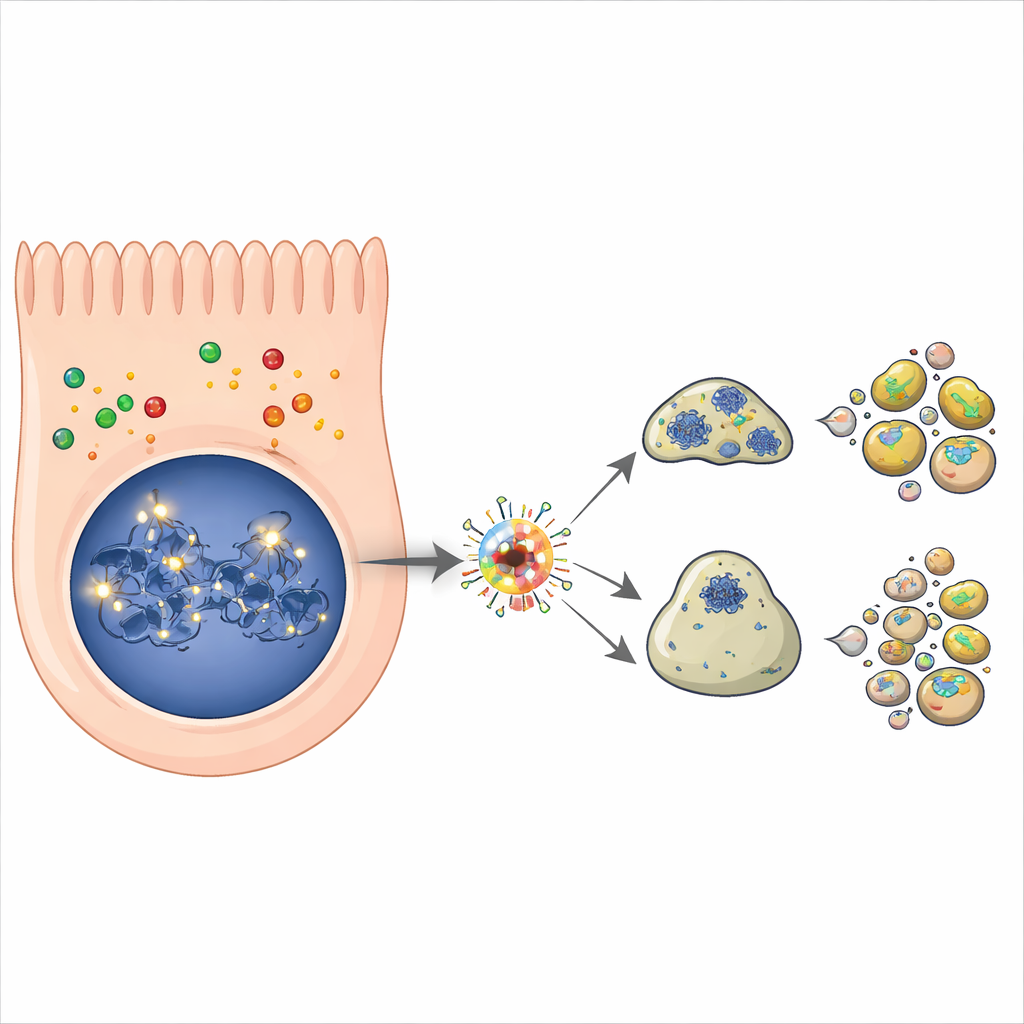
Collegamenti con infiammazione, perdita dell’olfatto e malattie croniche
I risultati si inseriscono in un quadro più ampio in cui monossido di azoto e p53 plasmano insieme la risposta dei tessuti a stress e infiammazione. In condizioni come la COVID-19, l’infiammazione nasale e gli enzimi che producono monossido di azoto sono aumentati, e si pensa che l’attività di p53 cresca durante reazioni immunitarie intense. Lo studio suggerisce una catena di eventi plausibile: durante un picco infiammatorio, il monossido di azoto persistente potrebbe danneggiare il DNA nelle cellule nasali, attivare p53 e scatenare la loro morte. Nel tempo, questo può assottigliare o alterare la barriera nasale, facilitando l’ingresso di virus, inquinanti e segnali infiammatori più in profondità nelle vie respiratorie o persino al cervello. Tale danno potrebbe contribuire a problemi persistenti come la perdita prolungata dell’olfatto o malattie croniche del naso e delle vie aeree.
Cosa significa per la protezione della barriera nasale
In termini semplici, lo studio mostra che quando il monossido di azoto persiste a livelli elevati può spingere le cellule della mucosa nasale ad attivare il proprio interruttore interno di “autodistruzione” tramite p53, riducendo il numero cellulare e potenzialmente indebolendo la barriera interna del naso. Pur essendo il lavoro condotto in un sistema cellulare semplificato e non in soggetti umani viventi, sottolinea che le sostanze chimiche di difesa del corpo devono essere mantenute in equilibrio. Troppo poco monossido di azoto può compromettere la protezione immunitaria, ma troppo a lungo può erodere i tessuti che ci proteggono. Una migliore comprensione di questo equilibrio potrebbe in futuro orientare strategie per preservare la salute della barriera nasale durante infezioni gravi e infiammazioni croniche.
Citazione: Kamiuezono, S., Kubota, S., Tsuchida, T. et al. Nitric oxide induces p53-mediated cell death in human nasal epithelial cells. Sci Rep 16, 10055 (2026). https://doi.org/10.1038/s41598-026-40908-6
Parole chiave: monossido di azoto, epitelio nasale, p53, apoptosi, infiammazione