Clear Sky Science · fr
Le monoxyde d’azote induit une mort cellulaire médiée par p53 dans les cellules épithéliales nasales humaines
Pourquoi la première ligne de défense de votre nez compte
Vos voies nasales ne sont pas de simples conduits d’air ; elles forment un bouclier vivant qui aide à empêcher virus, bactéries et polluants d’entrer dans le corps et le cerveau. Lors d’infections et d’inflammations chroniques, ce bouclier est baigné de signaux chimiques qui combattent les agents pathogènes mais peuvent aussi endommager nos propres cellules. L’un de ces acteurs, le monoxyde d’azote, est à la fois défenseur et fauteur de troubles bien connu. Cette étude pose une question simple mais importante : lorsque le monoxyde d’azote persiste à des niveaux élevés autour de la muqueuse nasale, affaiblit‑il silencieusement cette première ligne de défense ?
Un gaz utile au revers sombre
Le monoxyde d’azote est une petite molécule gazeuse que notre organisme utilise pour dilater les vaisseaux sanguins, faciliter la communication nerveuse et alimenter les défenses immunitaires. Les cellules immunitaires en libèrent par bouffées pour aider à tuer les microbes envahisseurs, et à des concentrations normales il soutient un fonctionnement sain. Mais lors de réactions immunitaires intenses ou prolongées, le monoxyde d’azote peut être produit en excès et réagir avec l’oxygène pour former des espèces chimiques très agressives. Celles‑ci peuvent endommager l’ADN et d’autres composants cellulaires vitaux, transformant une arme utile en source de dommages collatéraux. Parce que la muqueuse nasale est directement exposée au monde extérieur et constitue une porte d’entrée majeure pour des virus respiratoires tels que le SARS‑CoV‑2, comprendre les effets d’une exposition durable au monoxyde d’azote sur ces cellules est crucial.
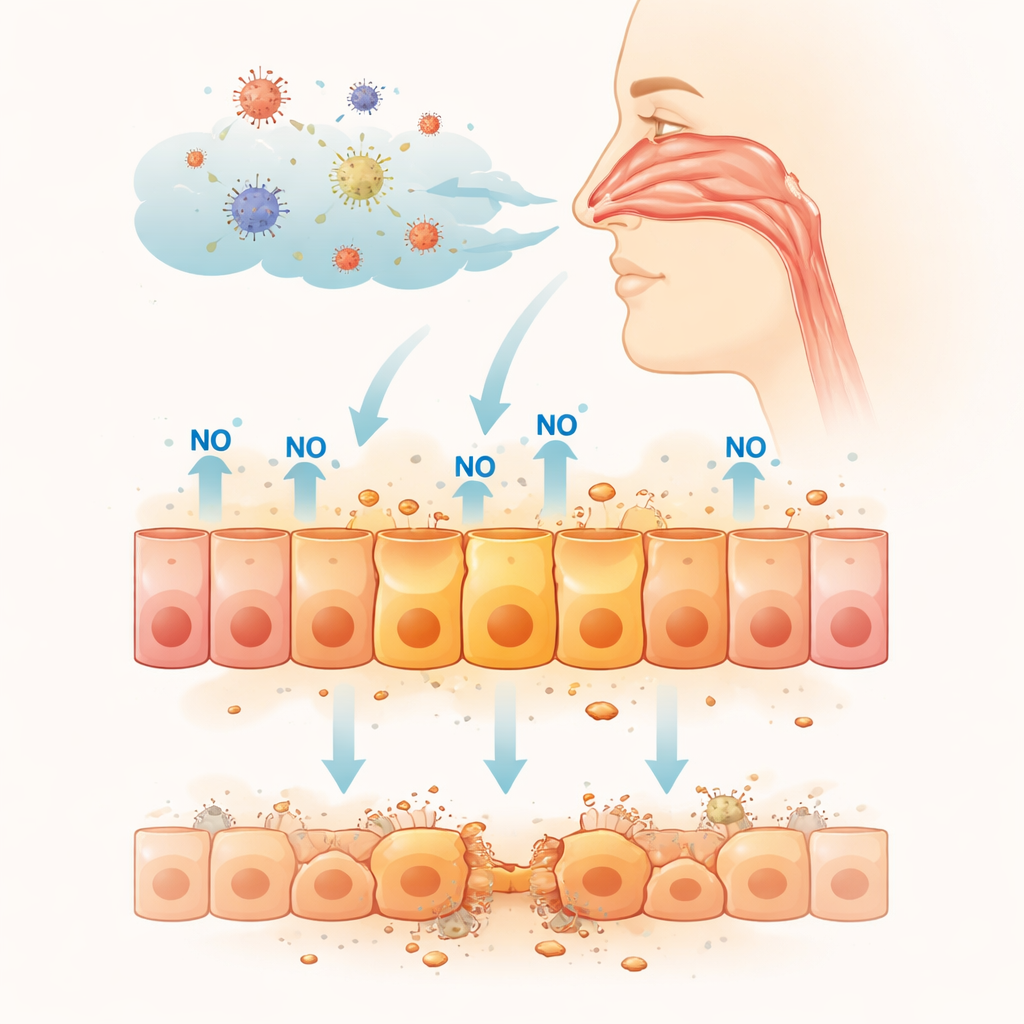
Tester une exposition prolongée sur des cellules nasales
Pour explorer cela, les chercheurs ont utilisé une lignée cellulaire d’épithélium nasal humain cultivée en laboratoire, un substitut couramment employé du barrage nasal. Ils ont exposé ces cellules pendant jusqu’à trois jours à un composé libérant du monoxyde d’azote à des niveaux similaires à ceux rapportés dans les tissus enflammés. Au fil du temps, la croissance cellulaire a ralenti et davantage de cellules sont mortes, indiquant qu’un monoxyde d’azote soutenu est toxique pour ce modèle nasal. Pour comprendre ce qui se passait à l’intérieur des cellules, l’équipe a analysé les gènes activés ou réprimés après 48 heures d’exposition. Des centaines de gènes ont modifié leur activité, et beaucoup des gènes les plus fortement activés étaient liés à une protéine gardienne centrale de la cellule appelée p53, qui surveille les dommages à l’ADN et contrôle si les cellules se réparent, cessent de se diviser ou s’autodétruisent.
Comment la sentinelle cellulaire se retourne contre les cellules endommagées
Des expériences de suivi ont confirmé que le monoxyde d’azote provoque l’accumulation de la protéine p53 dans les cellules nasales en quelques heures seulement, une signature de son activation. À mesure que les niveaux de p53 augmentaient, l’activité de plusieurs de ses gènes cibles favorisant la mort cellulaire programmée et l’arrêt du cycle cellulaire augmentait également. Les marqueurs de l’apoptose, le programme propre d’autodestruction qui fragmente les cellules en petits éléments éliminables, se sont accrus au fil du temps. Lorsque les scientifiques ont utilisé un médicament bloquant spécifiquement la capacité de p53 à réguler les gènes, à la fois la montée des gènes cibles de p53 et le taux de mortalité cellulaire ont été significativement réduits. Cela a montré que p53 est un moteur majeur de la perte de cellules épithéliales nasales induite par le monoxyde d’azote, même si d’autres voies contribuent probablement aussi.
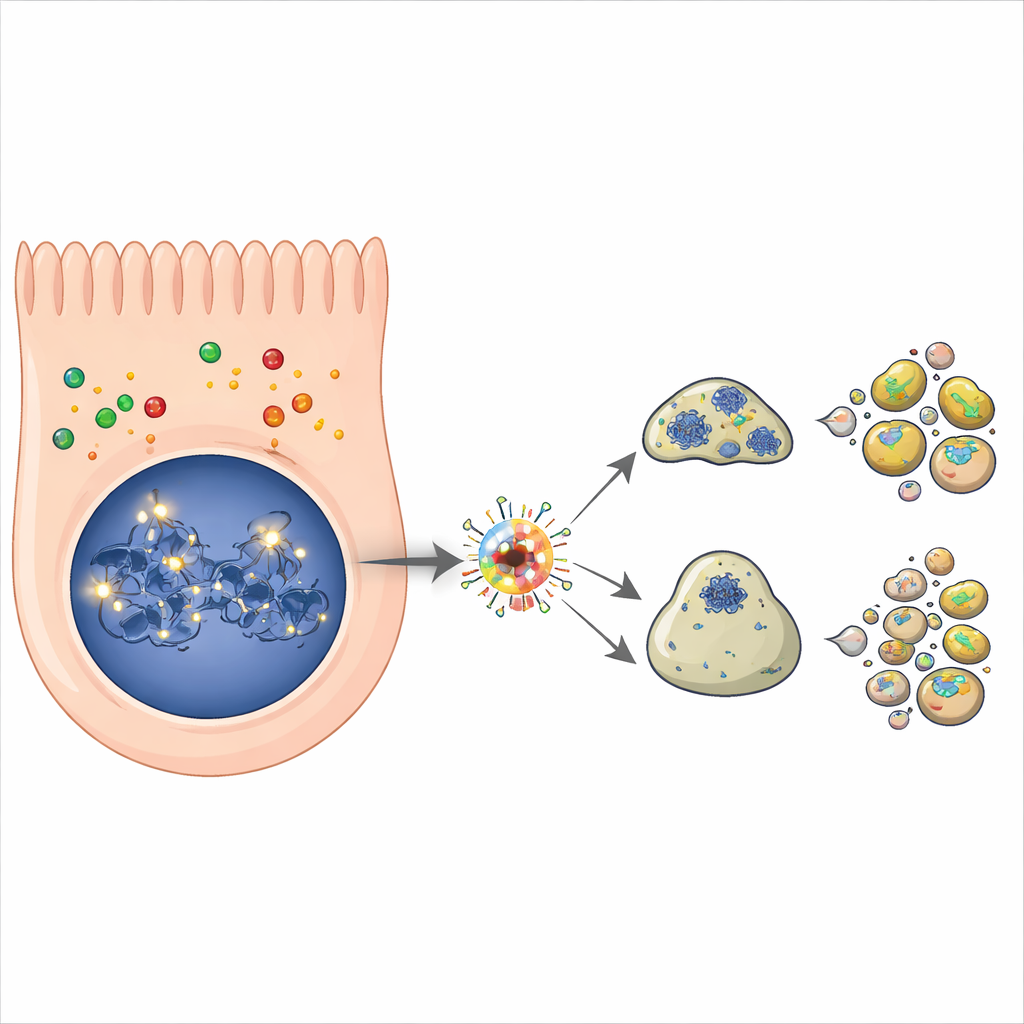
Liens avec l’inflammation, la perte d’odorat et les maladies chroniques
Ces résultats s’inscrivent dans un panorama plus large où le monoxyde d’azote et p53 conjuguent leurs effets pour façonner la réponse des tissus au stress et à l’inflammation. Dans des affections telles que la COVID‑19, l’inflammation nasale et les enzymes produisant du monoxyde d’azote sont élevées, et l’activité de p53 est supposée augmenter lors de fortes réactions immunitaires. L’étude suggère une chaîne d’événements plausible : pendant un pic inflammatoire, un monoxyde d’azote prolongé pourrait endommager l’ADN des cellules nasales, activer p53 et déclencher leur mort. Avec le temps, cela peut amincir ou perturber la barrière nasale, facilitant la pénétration plus profonde de virus, polluants et signaux inflammatoires dans les voies respiratoires ou même jusqu’au cerveau. De tels dommages pourraient contribuer à des problèmes persistants comme une perte d’odorat durable ou des maladies nasales et respiratoires chroniques.
Ce que cela signifie pour protéger la barrière nasale
En termes simples, l’étude montre que lorsque le monoxyde d’azote persiste à des niveaux élevés, il peut pousser les cellules de la muqueuse nasale à activer leur interrupteur interne d’« autodestruction » via p53, réduisant le nombre de cellules et affaiblissant potentiellement la barrière nasale. Bien que le travail ait été réalisé dans un système cellulaire simplifié et non chez des êtres humains vivants, il souligne que les substances défensives produites par le corps doivent être finement équilibrées. Trop peu de monoxyde d’azote peut nuire à la protection immunitaire, mais trop, pendant trop longtemps, peut éroder les tissus mêmes qui nous protègent. Une meilleure compréhension de cet équilibre pourrait, à terme, informer des stratégies visant à préserver la santé de la barrière nasale lors d’infections sévères et d’inflammations chroniques.
Citation: Kamiuezono, S., Kubota, S., Tsuchida, T. et al. Nitric oxide induces p53-mediated cell death in human nasal epithelial cells. Sci Rep 16, 10055 (2026). https://doi.org/10.1038/s41598-026-40908-6
Mots-clés: monoxyde d’azote, épithélium nasal, p53, apoptose, inflammation