Clear Sky Science · de
Nitric oxide induces p53-mediated cell death in human nasal epithelial cells
Warum die vordere Abwehr Ihrer Nase wichtig ist
Ihre Nasengänge sind mehr als nur Luftkanäle; sie bilden einen lebenden Schutzschild, der verhindert, dass Viren, Bakterien und Schadstoffe in Körper und Gehirn eindringen. Bei Infektionen und chronischer Entzündung wird dieser Schild von chemischen Signalen durchspült, die Krankheitserreger bekämpfen, aber auch die eigenen Zellen schädigen können. Ein solches Molekül, Stickstoffmonoxid, ist zugleich bewährter Verteidiger und Störenfried. Diese Studie stellt eine einfache, aber wichtige Frage: Schwächt Stickstoffmonoxid, wenn es in hohen Konzentrationen an der Nasenschleimhaut verharrt, stillschweigend diese erste Verteidigungslinie?
Ein nützliches Gas mit dunkler Seite
Stickstoffmonoxid ist ein winziges Gasmolekül, das unser Körper nutzt, um Blutgefäße zu erweitern, die Nervensignalübertragung zu unterstützen und die Immunabwehr anzutreiben. Immunzellen setzen es in Stößen frei, um eindringende Mikroben zu töten; in normalen Mengen fördert es gesunde Funktionen. Bei starken oder anhaltenden Immunreaktionen kann jedoch zu viel Stickstoffmonoxid produziert werden, das mit Sauerstoff reagiert und hochreaktive chemische Spezies bildet. Diese können DNA und andere lebenswichtige Zellkomponenten schädigen und aus einer hilfreichen Waffe eine Quelle von Kollateralschäden machen. Da die Nasenschleimhaut direkt der Außenwelt ausgesetzt ist und ein Haupteingang für Atemwegsviren wie SARS-CoV-2 ist, ist es entscheidend zu verstehen, wie lang andauernde Stickstoffmonoxid-Exposition diese Zellen beeinflusst.
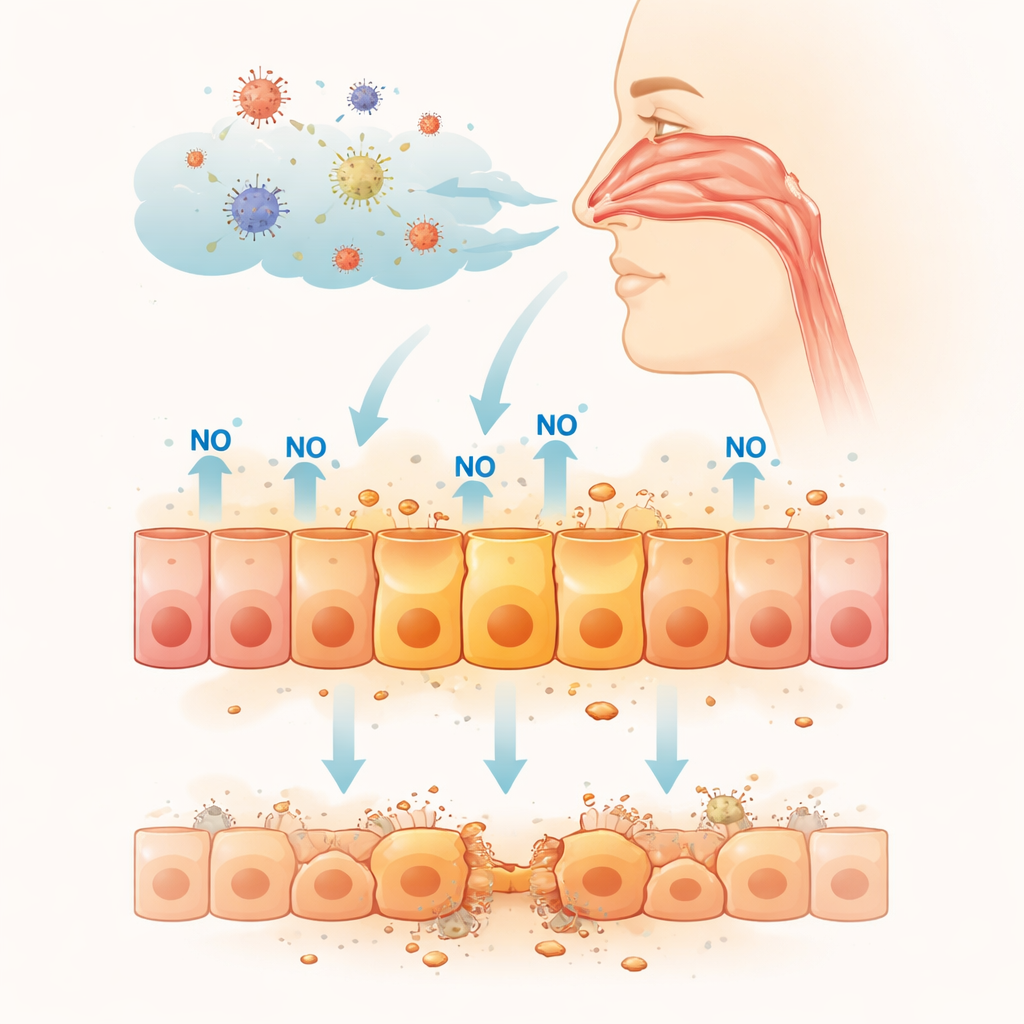
Langzeit-Exposition in Nasenzellen testen
Um dies zu untersuchen, verwendeten die Forscher eine im Labor gezüchtete humane Nasenepithelzelllinie, einen häufig genutzten Ersatz für die Nasenbarriere. Sie setzten diese Zellen bis zu drei Tage lang einer Stickstoffmonoxid-freisetzenden Verbindung in Konzentrationen aus, die denen in entzündetem Gewebe ähneln. Mit der Zeit verlangsamte sich das Zellwachstum und mehr Zellen starben, was darauf hinweist, dass anhaltendes Stickstoffmonoxid für dieses Nasenmodell toxisch ist. Um herauszufinden, was sich innerhalb der Zellen abspielte, analysierte das Team, welche Gene nach 48 Stunden Exposition ein- oder ausgeschaltet waren. Hunderte Gene veränderten ihre Aktivität, und viele der am stärksten aktivierten Gene standen in Verbindung mit einem zentralen zellulären Wächterprotein namens p53, das DNA-Schäden überwacht und steuert, ob Zellen sich reparieren, die Teilung einstellen oder sich selbst zerstören.
Wie der Zellwächter gegen beschädigte Zellen vorgeht
Folgeexperimente bestätigten, dass Stickstoffmonoxid dazu führt, dass das p53-Protein bereits innerhalb weniger Stunden in den Nasenzellen akkumuliert — ein Kennzeichen seiner Aktivierung. Mit steigenden p53-Werten nahm auch die Aktivität mehrerer Zielgene zu, die Zellen in Richtung programmierter Zelltod treiben und den Zellzyklus anhalten. Marker der Apoptose, des ordentlichen Selbstzerstörungsprogramms, das Zellen in kleine, entsorgbare Fragmente zerlegt, erhöhten sich im Laufe der Zeit. Als die Wissenschaftler ein Medikament einsetzten, das spezifisch p53s Fähigkeit zur Genregulation blockiert, gingen sowohl der Anstieg der p53-Zielgene als auch das Ausmaß des Zelltods erheblich zurück. Das zeigte, dass p53 ein wichtiger Treiber des durch Stickstoffmonoxid induzierten Verlusts von Nasenepithelzellen ist, auch wenn wahrscheinlich weitere Signalwege beitragen.
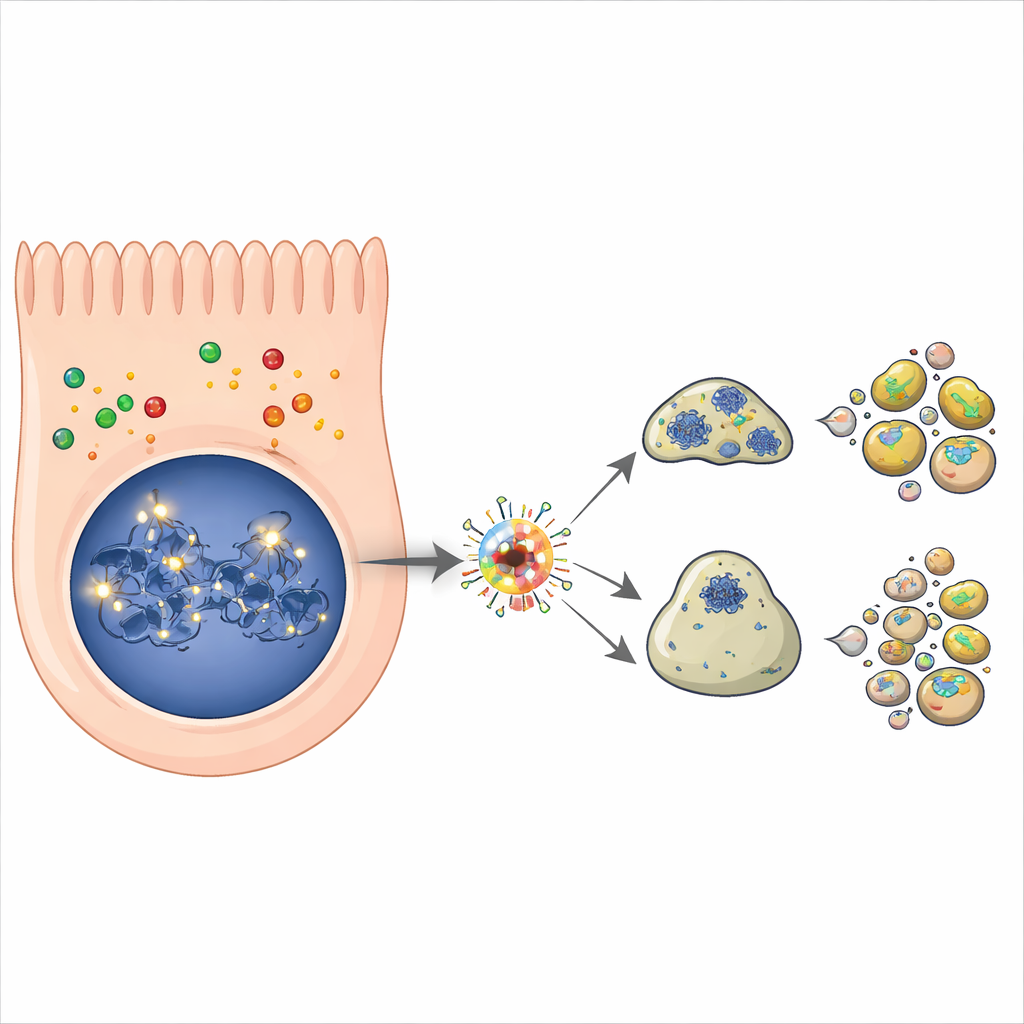
Bezüge zu Entzündung, Geruchsverlust und chronischen Erkrankungen
Die Ergebnisse fügen sich in ein größeres Bild, in dem Stickstoffmonoxid und p53 gemeinsam bestimmen, wie Gewebe auf Stress und Entzündung reagieren. Bei Erkrankungen wie COVID-19 sind Nasenentzündungen und die stickstoffmonoxidproduzierenden Enzyme erhöht, und man nimmt an, dass die p53-Aktivität während intensiver Immunreaktionen zunimmt. Die Studie schlägt eine plausible Abfolge vor: Während eines entzündlichen Schubs könnte anhaltendes Stickstoffmonoxid DNA in Nasenzellen schädigen, p53 aktivieren und deren Tod auslösen. Im Laufe der Zeit könnte dies die Nasenbarriere ausdünnen oder stören und es Viren, Schadstoffen und entzündlichen Signalen erleichtern, tiefer in die Atemwege oder sogar ins Gehirn vorzudringen. Solche Schäden könnten zu anhaltenden Problemen wie länger andauerndem Geruchsverlust oder chronischen Nasen- und Atemwegserkrankungen beitragen.
Was das für den Schutz der Nasenbarriere bedeutet
Einfach gesagt zeigt die Studie, dass Stickstoffmonoxid, wenn es längere Zeit in hohen Konzentrationen präsent ist, Nasenschleimhautzellen dazu bringen kann, über p53 ihren inneren „Selbstzerstörungs“-Schalter zu aktivieren, wodurch die Zellzahl sinkt und die Barriere im Inneren der Nase möglicherweise geschwächt wird. Obwohl die Arbeit in einem vereinfachten Zellmodell und nicht an lebenden Menschen durchgeführt wurde, unterstreicht sie, dass die körpereigenen Abwehrchemikalien sorgfältig austariert sein müssen. Zu wenig Stickstoffmonoxid kann den Immunschutz schwächen, aber zu viel über lange Zeiträume kann die Gewebe angreifen, die uns schützen. Ein besseres Verständnis dieses Gleichgewichts könnte schließlich zu Strategien führen, die die Gesundheit der Nasenbarriere bei schweren Infektionen und chronischer Entzündung erhalten.
Zitation: Kamiuezono, S., Kubota, S., Tsuchida, T. et al. Nitric oxide induces p53-mediated cell death in human nasal epithelial cells. Sci Rep 16, 10055 (2026). https://doi.org/10.1038/s41598-026-40908-6
Schlüsselwörter: nitric oxide, nasal epithelium, p53, apoptosis, inflammation