Clear Sky Science · sv
Bedömning av antimikrobiell aktivitet hos [1,2,4]triazolo[4, 3-a]kinoxalin‑derivat individuellt och i kombination med levofloxacin
Varför nya samarbetspartner mot bakterier spelar roll
Antibiotikaresistens urholkar effekten hos många beprövade läkemedel och lämnar läkare med färre alternativ för att behandla vanliga infektioner. Denna studie undersöker en strategi som inte bygger på att uppfinna ett helt nytt antibiotikum utan i stället utveckla små partnermolekyler som kan förstärka effekten hos ett befintligt läkemedel, levofloxacin. Genom att para ihop detta vanliga antibiotikum med särskilt utformade hjälpföreningar strävar forskarna efter att slå ut farliga bakterier, inklusive resistenta stammar, med lägre doser och begränsad skada på människoceller. 
Att bygga nya kemiska hjälpmedel
Teamet fokuserade på en familj ringformade molekyler kallade triazoloquinoxaliner, strukturer som redan är kända för att interagera väl med biologiska mål. Med en femstegs syntes framställde de tio nya varianter av dessa molekyler, var och en försedd med en annan liten kemisk sidokedja. Dessa sidogrupper varierade från enkla kolkedjor till alkoholinnehållande grupper och större sidofunktioner. Forskarna använde sedan en rad analytiska verktyg—såsom infraröd absorption och kärnmagnetisk resonans—för att bekräfta att varje syntessteg gav den avsedda strukturen och att de nya ringarna var korrekt uppbyggda.
Testning mot vanliga mikrober
När strukturerna bekräftats testades föreningarna mot flera medicinskt viktiga mikrober: två stafylokockbakterier (Staphylococcus aureus och Staphylococcus epidermidis), två tarmrelaterade bakterier (Escherichia coli och Pseudomonas aeruginosa) samt jästen Candida albicans. Tre medlemmar i familjen—betecknade 5b, 5d och 5h—visade starkast förmåga att sakta eller stoppa tillväxt, även om de var mindre potenta än standardantibiotika på egen hand. Subtila förändringar i deras kemiska sidokedjor gjorde stor skillnad: en förgrenad kolkedja och en alkoholgrupp hjälpte dessa molekyler att ta sig igenom bakteriers försvar och interagera mer effektivt, medan långa raka kedjor eller skrymmande ringsystem tenderade att dämpa deras aktivitet.
Att samarbeta med ett befintligt antibiotikum
Eftersom inga av de nya föreningarna på egen hand matchade styrkan hos befintliga läkemedel vände sig forskarna till kombinationsterapi. De blandade 5b, 5d och 5h med levofloxacin och mätte hur stora mängder av varje som krävdes för att stoppa bakterietillväxt. Resultaten visade stark synergi: i kombination krävdes avsevärt lägre mängder både av hjälpföreningarna och av levofloxacin för att kontrollera bakterier, inklusive sjukhusisolerade stammar av meticillinresistent S. aureus (MRSA) och resistent P. aeruginosa. I vissa fall minskade den effektiva dosen levofloxacin med mer än en storleksordning. Elektronmikroskopbilder förde ytterligare stöd, och visade att bakterier exponerade för kombinationerna hade ihopskrynklade, rupturerade ytor och läckande innehåll, i skarp kontrast till de släta, intakta cellerna i obehandlade prover. 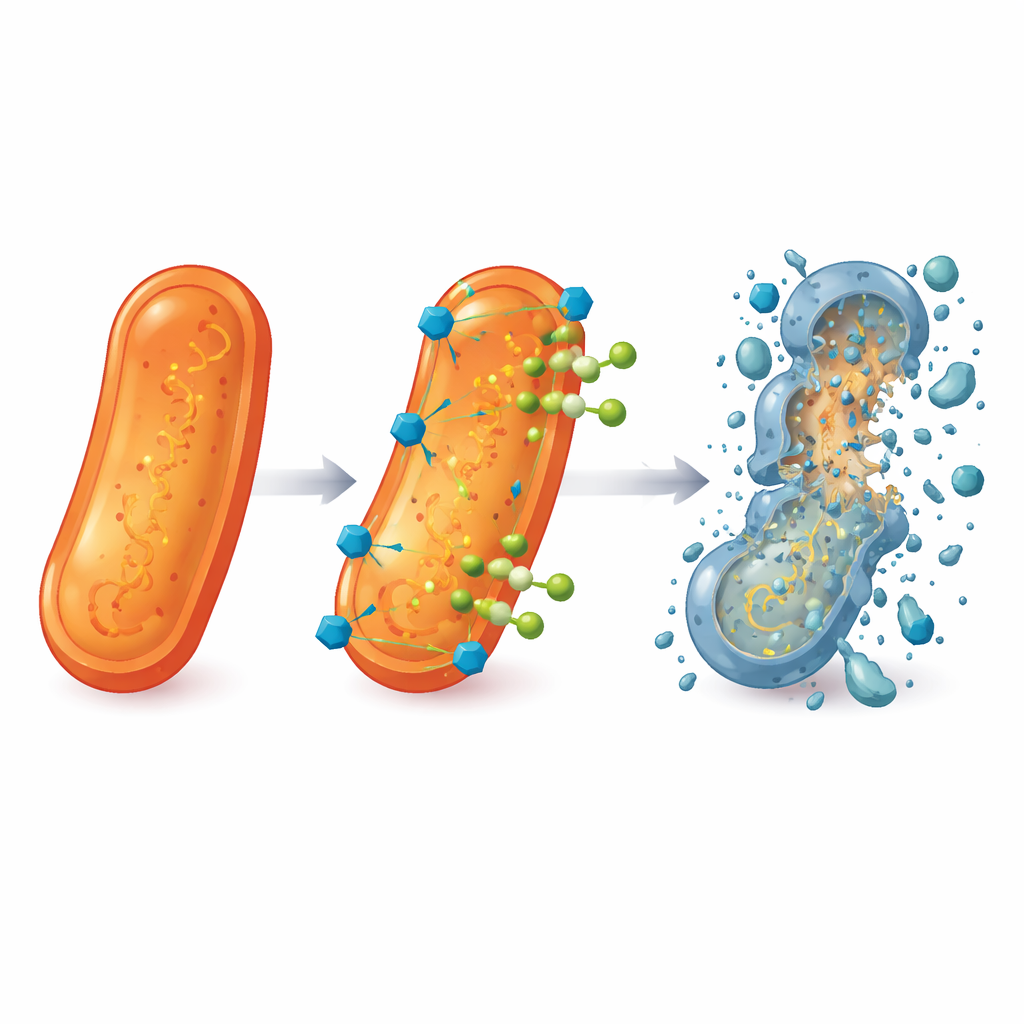
Kontroll av säkerhet för mänskliga celler
Varje potentiellt hjälpläkemedel måste skada mikrober mer än det skadar oss. För att bedöma denna balans exponerade teamet musbindvävsceller och röda blodkroppar för olika doser av de tre bästa föreningarna. Vid nivåer lika med eller dubbla de som krävdes för att hämma bakterier lämnade föreningarna 5b och 5d de flesta däggdjursceller vid liv och orsakade nästan ingen skada på röda blodkroppar. Förening 5h var något mer retande vid dessa doser men visade ändå begränsad skada vid de koncentrationer som användes i antibakteriella tester. Först vid mycket högre nivåer blev alla tre föreningarna tydligt giftiga, vilket tyder på att det finns ett användbart fönster där bakterier slås hårt medan humana celler i stor utsträckning förblir opåverkade.
Vad detta betyder för framtida behandlingar
Enkelt uttryckt visar studien att noggrant utformade kemiska partner kan få ett befintligt antibiotikum att fungera bättre mot både vanliga och läkemedelsresistenta mikrober. Triazoloquinoxalin‑hjälparna 5b, 5d och 5h ersätter inte levofloxacin; de verkar i stället försvaga bakteriers försvar—sannolikt genom att störa cellväggar eller rikta in sig på andra interna system—så att antibiotikumet kan göra jobbet vid lägre doser. För patienter kan sådana kombinationer en dag innebära effektivare behandlingar med färre biverkningar och en långsammare utveckling av resistens. Innan det kan bli verklighet måste dessa lovande hjälpämnen dock fortfarande testas i djur och så småningom i kliniska prövningar för att bekräfta deras säkerhet, stabilitet och verkliga effekt mot svårbehandlade infektioner.
Citering: Harooni, N.S., Naimi-Jamal, M.R., Dekamin, M.G. et al. Assessment of antimicrobial activity of [1,2,4]triazolo[4, 3-a]quinoxaline derivatives individually and in combination with levofloxacin. Sci Rep 16, 9902 (2026). https://doi.org/10.1038/s41598-026-39141-y
Nyckelord: antimikrobiell resistens, kombinationsterapi, levofloxacin, heterocykliska föreningar, läkemedelssynergi