Clear Sky Science · es
Evaluación de la actividad antimicrobiana de derivados de [1,2,4]triazolo[4,3-a]quinoxalina de forma individual y en combinación con levofloxacino
Por qué importan nuevos aliados contra los gérmenes
La resistencia a los antibióticos está socavando la eficacia de muchos fármacos de confianza, dejando a los médicos con menos opciones para tratar infecciones comunes. Este estudio explora una estrategia que no depende de inventar un antibiótico completamente nuevo, sino de diseñar pequeñas moléculas compañeras que pueden potenciar el rendimiento de un fármaco ya existente, el levofloxacino. Al combinar este antibiótico habitual con compuestos auxiliares especialmente diseñados, los investigadores buscan eliminar bacterias peligrosas, incluidas cepas resistentes, empleando dosis más bajas y con un daño limitado a las células humanas. 
Construyendo nuevos ayudantes químicos
El equipo se centró en una familia de moléculas en forma de anillo llamadas triazoloquinoxalinas, estructuras ya conocidas por interactuar bien con objetivos biológicos. Mediante una ruta de laboratorio de cinco pasos, elaboraron diez nuevas versiones de estas moléculas, cada una con una cola química pequeña distinta. Estas colas iban desde cadenas carbonadas simples hasta grupos que contienen alcohol y brazos laterales más voluminosos. Los investigadores emplearon una batería de herramientas analíticas—como espectroscopía infrarroja y resonancia magnética nuclear—para confirmar que cada paso de la síntesis había producido la estructura prevista y que los nuevos anillos estaban correctamente ensamblados.
Probando la eficacia frente a microbios comunes
Una vez confirmadas las estructuras, los compuestos se probaron frente a varios microbios de importancia médica: dos estafilococos (Staphylococcus aureus y Staphylococcus epidermidis), dos bacterias vinculadas al tracto intestinal (Escherichia coli y Pseudomonas aeruginosa) y la levadura Candida albicans. Tres miembros de la familia—denominados 5b, 5d y 5h—mostraron la mayor capacidad para frenar o detener el crecimiento, aunque por sí solos fueron menos potentes que los antibióticos estándar. Pequeños cambios en sus colas químicas marcaron una gran diferencia: una cadena carbonada ramificada y un grupo alcohol ayudaron a estas moléculas a atravesar las defensas bacterianas e interactuar con mayor eficacia, mientras que cadenas largas y rectas o sistemas cíclicos voluminosos tendían a reducir su actividad.
Trabajando en conjunto con un antibiótico existente
Dado que ninguno de los compuestos nuevos igualó por sí solo la potencia de los fármacos actuales, los investigadores optaron por la terapia combinada. Mezclaron 5b, 5d y 5h con levofloxacino y midieron cuánto de cada uno se necesitaba para detener el crecimiento bacteriano. Los resultados revelaron una fuerte sinergia: al combinarse, se requirieron cantidades mucho menores tanto de las moléculas auxiliares como del levofloxacino para controlar las bacterias, incluidas cepas hospitalarias de Staphylococcus aureus resistentes a la meticilina (MRSA) y P. aeruginosa resistente. En algunos casos, la dosis eficaz de levofloxacino se redujo en más de un orden de magnitud. Imágenes de microscopía electrónica respaldaron estos hallazgos, mostrando que las bacterias expuestas a las combinaciones presentaban superficies arrugadas, rotas y contenido filtrándose, en marcado contraste con las células lisas e intactas observadas en las muestras no tratadas. 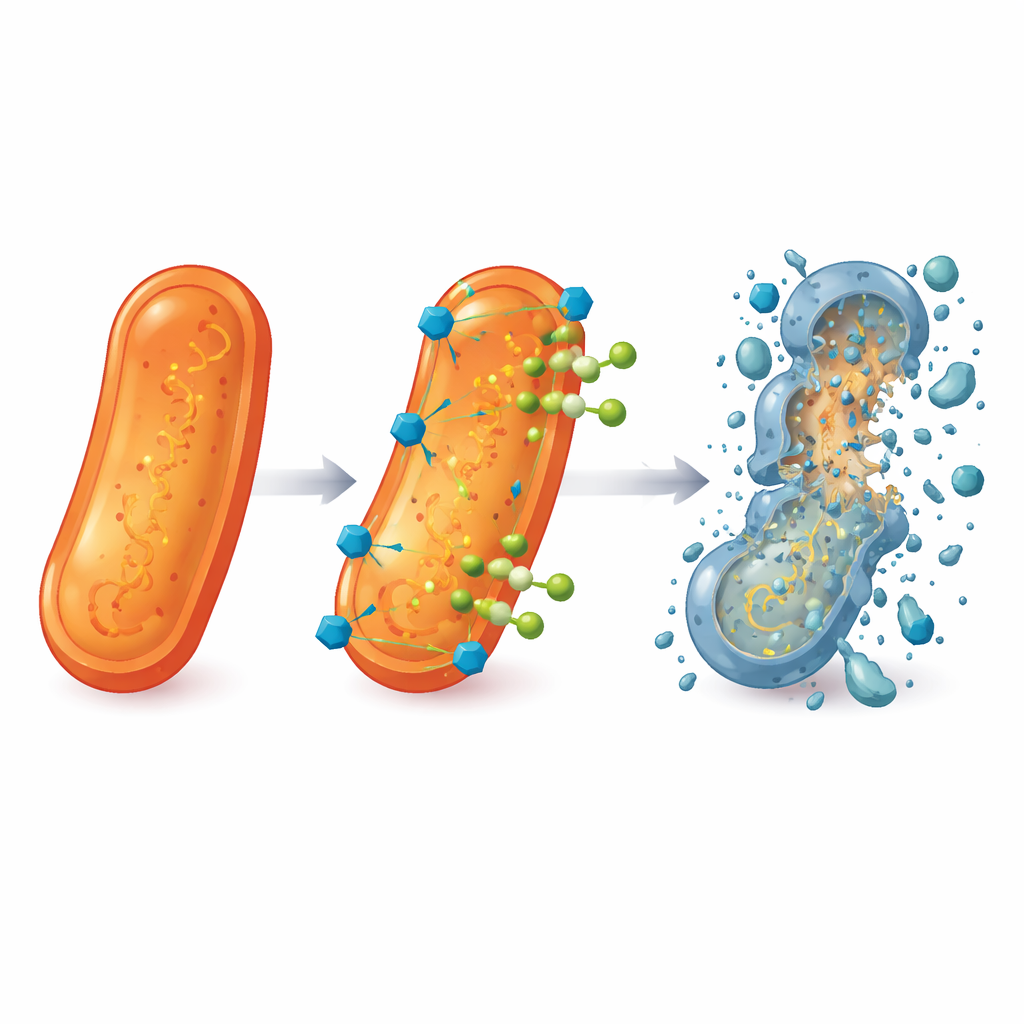
Comprobando la seguridad para células humanas
Cualquier posible fármaco auxiliar debe dañar más a los microbios que a nosotros. Para evaluar este equilibrio, el equipo expuso células del tejido conectivo de ratón y glóbulos rojos a distintas dosis de los tres mejores compuestos. A niveles iguales o el doble de los necesarios para inhibir las bacterias, los compuestos 5b y 5d dejaron la mayoría de las células de mamífero viables y causaron casi ningún daño a los glóbulos rojos. El compuesto 5h fue algo más irritante a esas dosis, pero aún mostró un daño limitado en las concentraciones usadas para las pruebas antibacterianas. Solo a niveles mucho más altos los tres compuestos se volvieron claramente tóxicos, lo que sugiere que existe una ventana útil en la que las bacterias reciben un golpe fuerte mientras las células humanas permanecen mayormente indemnes.
Qué significa esto para tratamientos futuros
En pocas palabras, el estudio demuestra que compañeros químicos cuidadosamente diseñados pueden mejorar la eficacia de un antibiótico existente contra microbios tanto comunes como resistentes a fármacos. Los ayudantes triazoloquinoxalina 5b, 5d y 5h no sustituyen al levofloxacino; en cambio, parecen debilitar las defensas bacterianas—probablemente perturbando las paredes celulares o atacando otros sistemas internos—para que el antibiótico pueda terminar el trabajo con dosis más bajas. Para los pacientes, tales combinaciones podrían algún día traducirse en tratamientos más eficaces con menos efectos secundarios y un avance más lento hacia la resistencia. Antes de que eso ocurra, sin embargo, estos prometedores ayudantes deben aún probarse en animales y, eventualmente, en ensayos clínicos para confirmar su seguridad, estabilidad e impacto real en infecciones difíciles de tratar.
Cita: Harooni, N.S., Naimi-Jamal, M.R., Dekamin, M.G. et al. Assessment of antimicrobial activity of [1,2,4]triazolo[4, 3-a]quinoxaline derivatives individually and in combination with levofloxacin. Sci Rep 16, 9902 (2026). https://doi.org/10.1038/s41598-026-39141-y
Palabras clave: resistencia antimicrobiana, terapia combinada, levofloxacino, compuestos heterocíclicos, sinergia farmacológica