Clear Sky Science · de
Bewertung der antimikrobiellen Aktivität von [1,2,4]triazolo[4,3-a]chinoxalin-Derivaten einzeln und in Kombination mit Levofloxacin
Warum neue Partner im Keimkampf wichtig sind
Antibiotikaresistenzen schwächen die Wirkung vieler bewährter Medikamente und lassen Ärzten weniger Optionen zur Behandlung alltäglicher Infektionen. Diese Studie untersucht eine Strategie, die nicht auf der Erfindung eines völlig neuen Antibiotikums beruht, sondern kleine Partnermoleküle entwickelt, die die Leistung eines bestehenden Wirkstoffs, Levofloxacin, verbessern können. Indem dieses vertraute Antibiotikum mit speziell entworfenen Helferverbindungen kombiniert wird, wollen die Forschenden gefährliche Bakterien — einschließlich medikamentenresistenter Stämme — mit geringeren Dosen bekämpfen und dabei die Schädigung menschlicher Zellen begrenzen. 
Neue chemische Helfer aufbauen
Das Team konzentrierte sich auf eine Familie ringförmiger Moleküle, die Triazolochinoxaline genannt werden, Strukturen, die bereits dafür bekannt sind, gut mit biologischen Zielen zu interagieren. Mithilfe einer fünfstufigen Laborsynthese stellten sie zehn neue Varianten dieser Moleküle her, von denen jede einen anderen kleinen chemischen Seitenrest trägt. Diese Endgruppen reichten von einfachen Kohlenstoffketten über alkoholhaltige Gruppen bis hin zu voluminöseren Seitenarmen. Die Forschenden nutzten dann ein Bündel analytischer Methoden — etwa Infrarot-Absorptionsspektroskopie und Kernspinresonanz — um zu bestätigen, dass jeder Syntheseschritt die beabsichtigte Struktur erzeugt hatte und die neuen Ringe korrekt aufgebaut waren.
Prüfung gegen verbreitete Mikroben
Sobald die Strukturen bestätigt waren, testete man die Verbindungen gegen mehrere medizinisch relevante Mikroorganismen: zwei Staphylokokken (Staphylococcus aureus und Staphylococcus epidermidis), zwei darmassoziierte Bakterien (Escherichia coli und Pseudomonas aeruginosa) sowie die Hefe Candida albicans. Drei Mitglieder der Reihe — bezeichnet als 5b, 5d und 5h — zeigten die stärkste Fähigkeit, Wachstum zu verlangsamen oder zu stoppen, obwohl sie allein weniger wirksam waren als Standardantibiotika. Feine Veränderungen in ihren chemischen Seitenketten machten einen großen Unterschied: Eine verzweigte Kohlenstoffseitenkette und eine Alkoholgruppe halfen diesen Molekülen, bakteriellen Abwehrmechanismen besser zu entkommen und effektiver zu interagieren, während lange gerade Ketten oder sperrige Ringsysteme ihre Aktivität tendenziell abschwächten.
Gemeinsam mit einem vorhandenen Antibiotikum wirken
Da keine der neuen Verbindungen allein die Stärke aktueller Medikamente erreichte, wandten sich die Forschenden der Kombinationstherapie zu. Sie mischten 5b, 5d und 5h mit Levofloxacin und bestimmten, wie viel von jedem benötigt wurde, um das Bakterienwachstum zu stoppen. Die Ergebnisse zeigten starke Synergie: In Kombination waren deutlich geringere Mengen sowohl der Helfermoleküle als auch des Levofloxacins erforderlich, um Bakterien zu kontrollieren, darunter klinische Stämme von methicillinresistentem S. aureus (MRSA) und resistenten P. aeruginosa. In einigen Fällen sank die effektive Dosis von Levofloxacin um mehr als eine Zehnerpotenz. Elektronenmikroskopische Aufnahmen untermauerten dies, indem sie zeigten, dass Bakterien, die den Kombinationen ausgesetzt waren, eingedellte, aufgerissene Oberflächen und austretende Inhalte aufwiesen — im starken Gegensatz zu den glatten, intakten Zellen unbehandelter Proben. 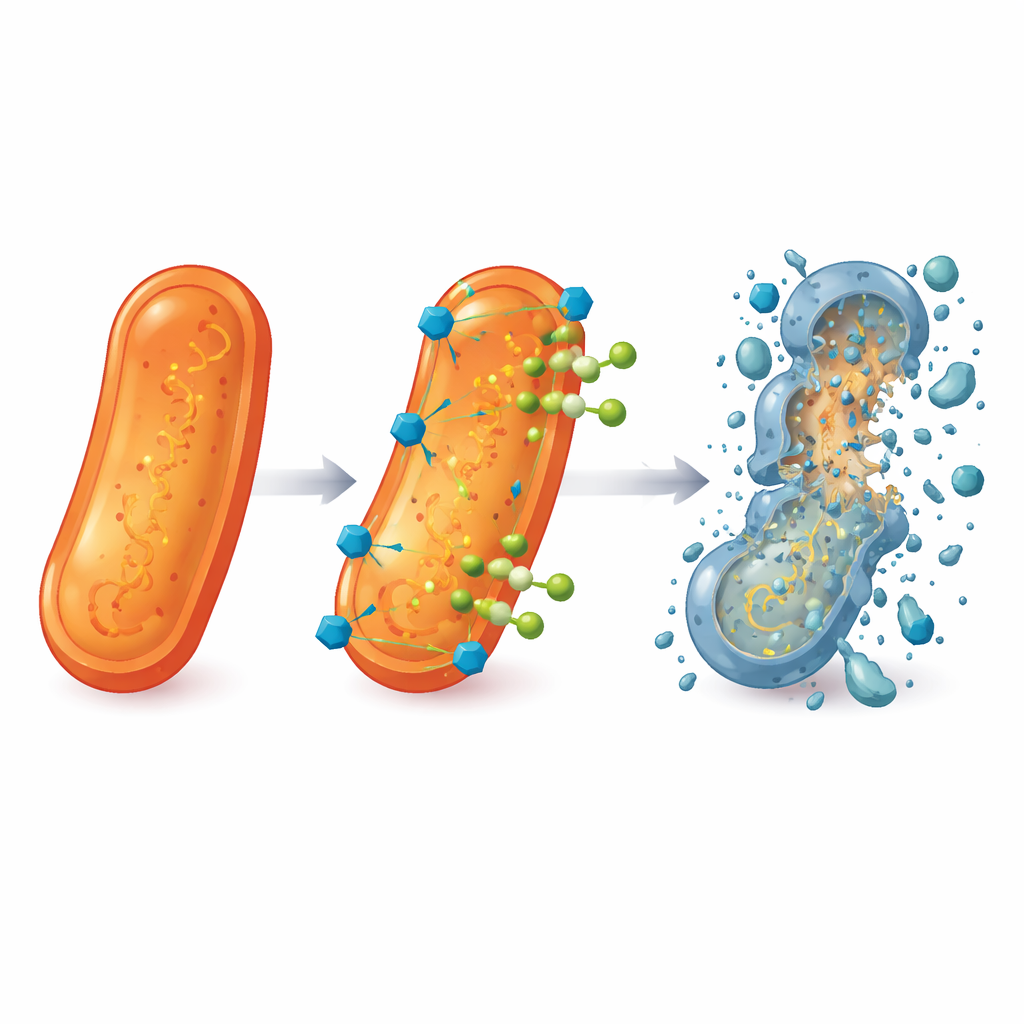
Sicherheitsprüfung für menschliche Zellen
Jedes potenzielle Helfermedikament muss Mikroben stärker schädigen als uns. Um dieses Gleichgewicht zu beurteilen, setzten die Forschenden Maus-Bindegewebszellen und rote Blutkörperchen verschiedenen Dosen der drei besten Verbindungen aus. Bei Konzentrationen, die denjenigen entsprachen oder dem Doppelten der für die Hemmung der Bakterien benötigten Werte, blieben bei den Verbindungen 5b und 5d die meisten Säugerzellen lebensfähig und es trat nahezu keine Schädigung der roten Blutkörperchen auf. Verbindung 5h war bei diesen Dosen etwas reizender, zeigte aber dennoch begrenzte Schäden bei den für die antibakteriellen Tests verwendeten Konzentrationen. Erst bei deutlich höheren Konzentrationen wurden alle drei Verbindungen eindeutig toxisch, was darauf hindeutet, dass es ein nützliches Fenster gibt, in dem Bakterien stark getroffen werden, während menschliche Zellen überwiegend verschont bleiben.
Was das für künftige Behandlungen bedeutet
Kurz gesagt zeigt die Studie, dass sorgfältig entworfene chemische Partner ein bestehendes Antibiotikum wirksamer gegen sowohl gewöhnliche als auch medikamentenresistente Mikroben machen können. Die Triazolochinoxalin-Helfer 5b, 5d und 5h ersetzen Levofloxacin nicht; vielmehr scheinen sie die bakteriellen Abwehrmechanismen aufzuweichen — wahrscheinlich durch Störungen der Zellwand oder durch Angriffe auf andere interne Systeme — sodass das Antibiotikum die Arbeit bei niedrigeren Dosen beenden kann. Für Patienten könnten solche Kombinationen eines Tages wirksamere Behandlungen mit weniger Nebenwirkungen und einer verlangsamten Entwicklung von Resistenzen bedeuten. Bevor das jedoch möglich wird, müssen diese vielversprechenden Helfer noch in Tierversuchen und schließlich in klinischen Studien getestet werden, um ihre Sicherheit, Stabilität und ihren tatsächlichen Nutzen bei schwer behandelbaren Infektionen zu bestätigen.
Zitation: Harooni, N.S., Naimi-Jamal, M.R., Dekamin, M.G. et al. Assessment of antimicrobial activity of [1,2,4]triazolo[4, 3-a]quinoxaline derivatives individually and in combination with levofloxacin. Sci Rep 16, 9902 (2026). https://doi.org/10.1038/s41598-026-39141-y
Schlüsselwörter: antimikrobielle Resistenz, Kombinationstherapie, Levofloxacin, heterocyclische Verbindungen, Wirkstoffsynergie