Clear Sky Science · pl
Ocena aktywności przeciwbakteryjnej pochodnych [1,2,4]triazolo[4,3-a]chinoksaliny samodzielnie i w połączeniu z lewofloksacyną
Dlaczego nowe wspomagacze przeciwdrobnoustrojowe są istotne
Oporność na antybiotyki osłabia skuteczność wielu zaufanych leków, pozostawiając lekarzom mniej opcji leczenia codziennych infekcji. W tym badaniu rozważono strategię, która nie polega na wynalezieniu zupełnie nowego antybiotyku, lecz na opracowaniu niewielkich cząsteczek‑partnerów, które mogą zwiększyć efektywność istniejącego leku, lewofloksacyny. Poprzez łączenie tego powszechnego antybiotyku ze specjalnie zaprojektowanymi związkami pomocniczymi, badacze dążą do zwalczania groźnych bakterii, w tym szczepów opornych, przy użyciu niższych dawek i przy ograniczonej szkodliwości dla komórek ludzkich. 
Tworzenie nowych chemicznych pomocników
Zespół skupił się na rodzinie pierścieniowych cząsteczek zwanych triazolochinoksalinami, strukturach już znanych z dobrego oddziaływania z celami biologicznymi. Wykorzystując pięcioetapową drogę syntezy, opracowali dziesięć nowych wersji tych związków, z których każdy miał inny mały łańcuch boczny. Ogony te obejmowały proste łańcuchy węglowe, grupy zawierające alkohol oraz większe ramiona boczne. Badacze zastosowali następnie zestaw narzędzi analitycznych — takich jak absorpcja w podczerwieni i spektroskopia rezonansu magnetycznego jądrowego — aby potwierdzić, że każdy etap syntezy dał zamierzoną strukturę i że nowe pierścienie zostały poprawnie zmontowane.
Testy przeciwko powszechnym drobnoustrojom
Po potwierdzeniu struktur, związki przetestowano przeciwko kilku medycznie istotnym drobnoustrojom: dwóm bakteriom gronkowcowym (Staphylococcus aureus i Staphylococcus epidermidis), dwóm bakteriom jelitowym (Escherichia coli i Pseudomonas aeruginosa) oraz drożdżakowi Candida albicans. Trzy związki z tej rodziny — oznaczone jako 5b, 5d i 5h — wykazały najsilniejszą zdolność do hamowania lub zatrzymywania wzrostu, choć same w sobie były mniej silne niż standardowe antybiotyki. Subtelne zmiany w ich bocznych łańcuchach chemicznych robiły dużą różnicę: rozgałęziony łańcuch węglowy i grupa alkoholowa pomagały tym molekułom przeniknąć obronę bakterii i skuteczniej wchodzić w interakcje, podczas gdy długie proste łańcuchy czy masywne układy pierścieniowe miały tendencję do tłumienia ich aktywności.
Współdziałanie z istniejącym antybiotykiem
Ponieważ żaden z nowych związków samodzielnie nie dorównywał sile obecnych leków, badacze zwrócili się ku terapii skojarzonej. Zmieszali 5b, 5d i 5h z lewofloksacyną i zmierzyli, jakie ilości każdego związku są potrzebne do zahamowania wzrostu bakterii. Wyniki wykazały silną synergię: w połączeniu wymagane były znacznie mniejsze ilości zarówno związków pomocniczych, jak i lewofloksacyny, aby kontrolować bakterie, w tym szczepy kliniczne metycylinoopornego S. aureus (MRSA) oraz opornego P. aeruginosa. W niektórych przypadkach skuteczna dawka lewofloksacyny spadła o ponad rząd wielkości. Obrazy z mikroskopu elektronowego potwierdziły te obserwacje, pokazując, że bakterie narażone na kombinacje miały pomarszczone, pękające powierzchnie i wypływające wnętrze, w wyraźnym kontraście do gładkich, nienaruszonych komórek w próbkach nieleczonych. 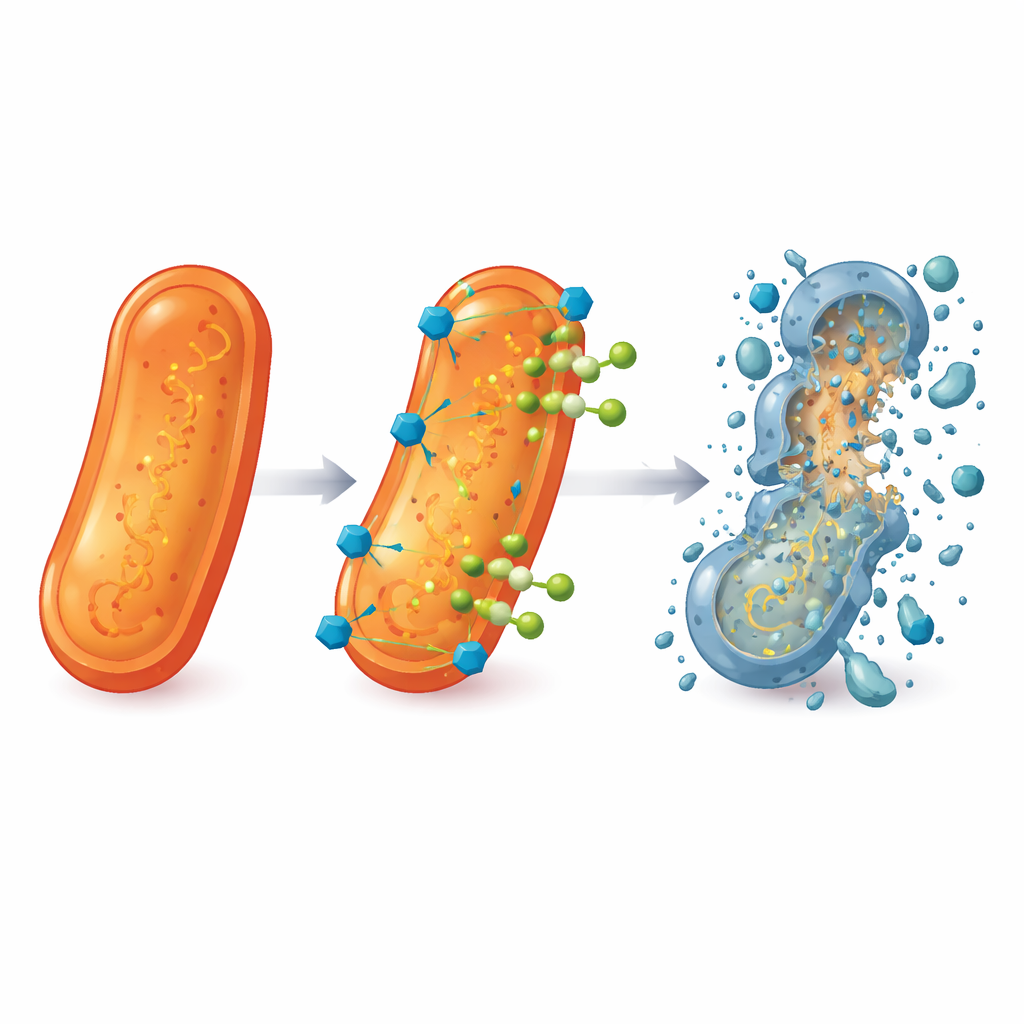
Ocena bezpieczeństwa dla komórek ludzkich
Potencjalny związek pomocniczy musi szkodzić drobnoustrojom bardziej niż nam. Aby ocenić tę równowagę, zespół wystawił komórki tkanki łącznej myszy oraz czerwone krwinki na różne dawki trzech najlepszych związków. Przy poziomach równych lub dwukrotnie wyższych niż te potrzebne do zahamowania bakterii, związki 5b i 5d pozostawiły większość komórek ssaczych żywych i spowodowały niemal żadnych uszkodzeń czerwonych krwinek. Związek 5h był przy tych dawkach nieco bardziej drażniący, ale nadal wykazywał ograniczoną szkodliwość w stężeniach używanych w testach przeciwbakteryjnych. Dopiero przy znacznie wyższych poziomach wszystkie trzy związki stały się wyraźnie toksyczne, co sugeruje istnienie użytecznego okna, w którym bakterie są silnie atakowane, podczas gdy komórki ludzkie pozostają w dużej mierze nienaruszone.
Co to oznacza dla przyszłych terapii
Mówiąc krótko, badanie pokazuje, że starannie zaprojektowane chemiczne partnery mogą sprawić, że istniejący antybiotyk będzie skuteczniejszy przeciwko zarówno zwykłym, jak i opornym drobnoustrojom. Pomocnicze triazolochinoksaliny 5b, 5d i 5h nie zastępują lewofloksacyny; zamiast tego wydają się osłabiać obronę bakterii — prawdopodobnie przez zaburzenie ścian komórkowych lub celów wewnętrznych — tak aby antybiotyk mógł dokończyć zadanie przy niższych dawkach. Dla pacjentów takie kombinacje mogłyby kiedyś oznaczać skuteczniejsze leczenie przy mniejszych skutkach ubocznych i wolniejszym rozwoju oporności. Zanim jednak do tego dojdzie, obiecujące związki muszą zostać przetestowane na zwierzętach, a w końcu w warunkach klinicznych, aby potwierdzić ich bezpieczeństwo, stabilność i rzeczywisty wpływ na trudne do leczenia infekcje.
Cytowanie: Harooni, N.S., Naimi-Jamal, M.R., Dekamin, M.G. et al. Assessment of antimicrobial activity of [1,2,4]triazolo[4, 3-a]quinoxaline derivatives individually and in combination with levofloxacin. Sci Rep 16, 9902 (2026). https://doi.org/10.1038/s41598-026-39141-y
Słowa kluczowe: oporność na środki przeciwdrobnoustrojowe, terapia skojarzona, lewofloksacyna, związki heterocykliczne, synergia leków