Clear Sky Science · sv
Funktionella effekter av EpCAM N-glykosylering i bröstcancercellerna MDA-MB-468
Varför små sockermärken på cancerceller spelar roll
De flesta av oss tänker på socker som något i kosten, men celler använder också komplexa sockerkedjor som små dekorationer på sina proteiner. Dessa sockermärken kan ändra hur proteiner beter sig, och de är ofta förändrade vid cancer. Denna studie ställer en riktad fråga: förändrar specifika sockermärken på en välkänd cancerrmarkör kallad EpCAM verkligen hur aggressiva bröstcancerceller är, eller finjustar de mest proteinet självt utan att omforma sjukdomen?
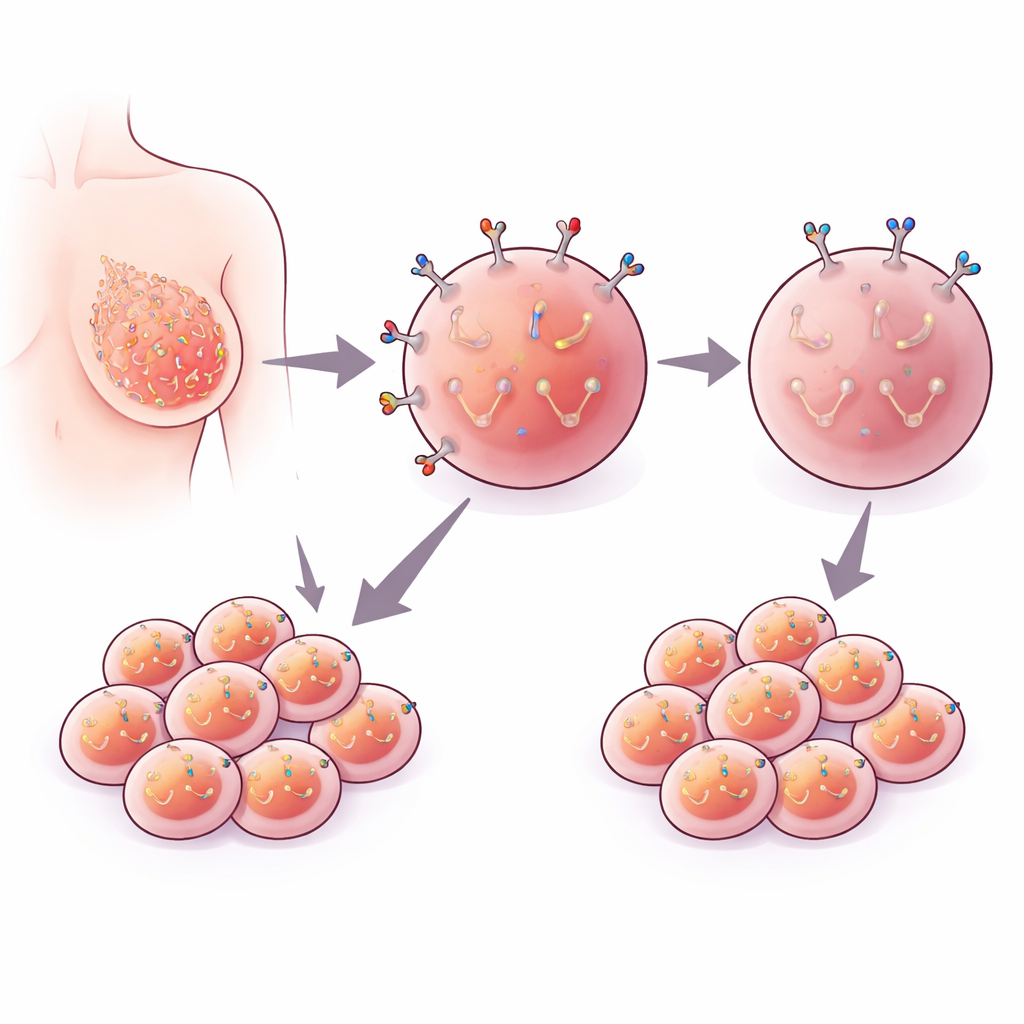
En markör på cancercellens yta
EpCAM är ett protein som sitter i cellmembranet hos många epitelceller, inklusive bröstceller. I flera cancerformer har tumörceller mycket mer EpCAM på ytan än friska celler, och patienter vars tumörer har höga EpCAM-nivåer får ofta en sämre prognos. Därför har EpCAM blivit ett populärt mål för diagnostiska tester och experimentella terapier. Men forskarna är fortfarande inte helt överens om EpCAM aktivt driver cancerspridning eller bara följer med som en åskådare associerad med andra skadliga förändringar.
Inzoomning på EpCAM:s sockerlager
EpCAM bär naturligt tre små sockerfästen på bestämda positioner i sin struktur. Tidigare patientstudier antydde att tumörer med mer EpCAM också visade mer av vissa sockertyper, vilket tyder på att detta sockerlager kan påverka hur EpCAM beter sig i metastas. Att direkt stänga av sockertillägg på bara ett protein är tekniskt svårt, så forskarna använde genengineering för att kringgå problemet. I en trippelnegativ bröstcancercellinje kallad MDA-MB-468 skapade de först celler där den normala EpCAM-genen var helt borttagen. Därefter satte de tillbaka antingen en normal, sockerkompetent version av EpCAM eller en subtilt förändrad version där de tre sockeracceptorpositionerna ändrats så att socker inte längre kan fästas.
Vad som händer när sockermärken tas bort
Med detta rena system mätte teamet vad som hände med EpCAM-proteinet självt. Att ta bort sockerplatserna gjorde EpCAM mycket mindre stabilt: när cellerna behandlades för att stoppa ny proteinproduktion så degraderades den sockerfria EpCAM märkbart snabbare än normal EpCAM. Mikroskopi visade vidare att den sockerfria versionen inte nådde cellytan lika effektivt. Istället tenderade den att dröja kvar inne i cellen, särskilt i det endoplasmatiska retiklet, ett veckat internmembransystem där proteiner viks och kontrolleras. Normal EpCAM, däremot, var koncentrerad vid cellmembranet där det kan kontakta närliggande celler och interagera med signalpartners.
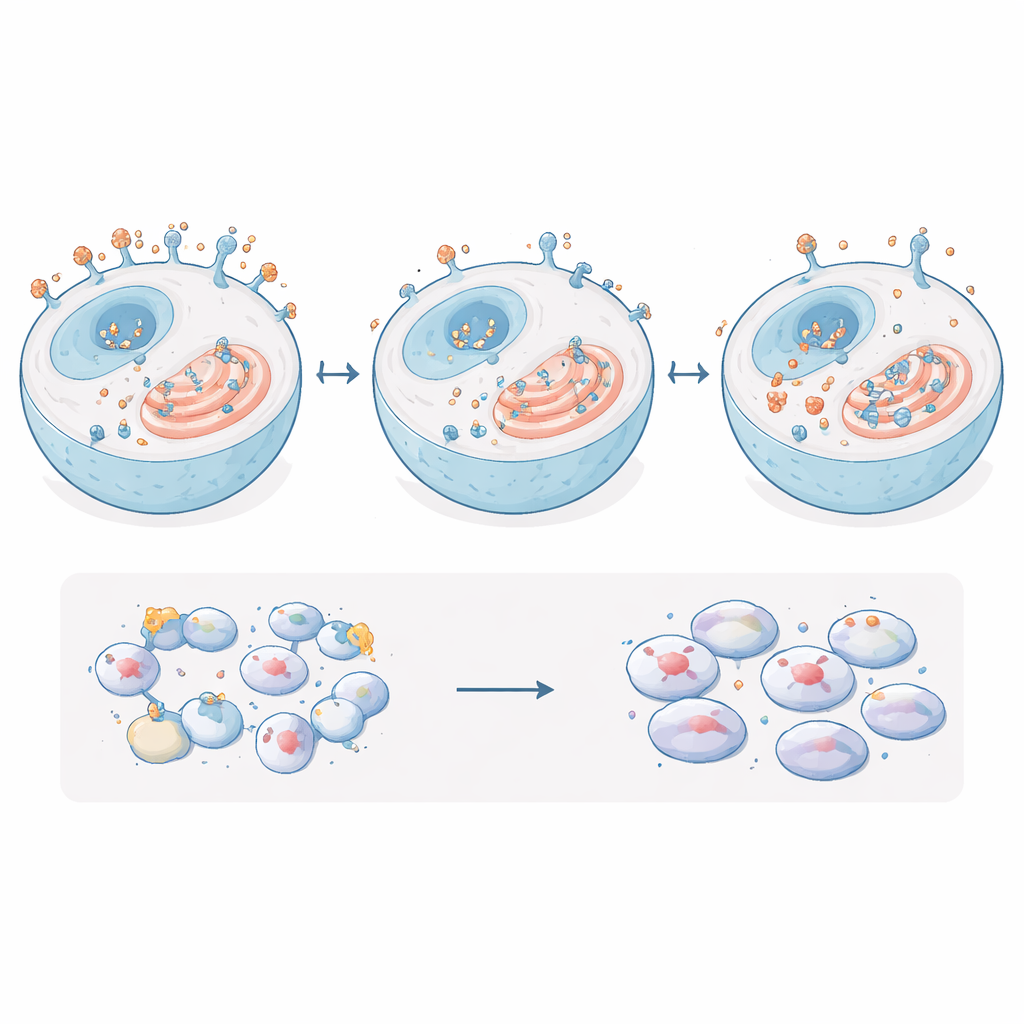
Vad som inte förändras inne i cancercellerna
Där EpCAM har kopplats till flera tillväxt- och överlevnadsvägar frågade forskarna nästa om avskalning av dess sockermärken ändrade viktiga nedströmsmolekyler eller cancerliknande beteenden. De mätte en uppsättning proteiner och gener som ofta regleras av EpCAM, inklusive stora tillväxtregulatorer och adhesionsmolekyler, och fann inga meningsfulla förändringar när de jämförde normala celler, EpCAM-frånvarande celler, EpCAM-överproducerande celler och celler med sockerfri EpCAM. Teamet utförde också standardlaboratorietester för egenskaper kopplade till metastas: hur snabbt cellerna växer, hur väl de rör sig genom en porös barriär, hur lätt de invaderar en gel som efterliknar omgivande vävnad och hur starkt de fastnar i varandra. Alla dessa egenskaper var i huvudsak oförändrade av förlusten av EpCAM-socker. Endast när EpCAM självt överproducerades kraftigt såg de en måttlig ökning i hur tätt cellerna klumpade ihop sig.
Vad detta betyder för förståelsen och inriktningen av EpCAM
Kort sagt visar studien att sockerlagret på EpCAM starkt påverkar proteinets stabilitet och var det befinner sig i bröstcancerceller, men det växlar inte i sig dessa celler till ett mer eller mindre aggressivt tillstånd i denna modell. I MDA-MB-468-celler gör borttagandet av EpCAM:s socker proteinet mindre hållbart och fångar mer av det inne i cellen, samtidigt som grundläggande beteenden kopplade till tumörspridning förblir till största delen desamma. Det tyder på att medan EpCAM och dess sockerdekorationer är viktiga delar av det molekylära pusslet, kan deras funktionella påverkan vara starkt beroende av celltyp och kontext. För terapidesign betonar arbetet att förändring eller riktning mot EpCAM:s sockerprofil kan ändra proteinet självt utan nödvändigtvis att ge en dramatisk, förutsägbar förändring i hur vissa bröstcancerceller beter sig.
Citering: Jenkinson, N.M., Oza, H., Yarema, K.J. et al. Functional effects of EpCAM N-glycosylation in MDA-MB-468 breast cancer cells. Sci Rep 16, 10021 (2026). https://doi.org/10.1038/s41598-026-38920-x
Nyckelord: EpCAM, bröstcancer, celladhesion, proteinglykosylering, metastas