Clear Sky Science · pl
Funkcjonalne efekty N-glikozylacji EpCAM w komórkach raka piersi MDA-MB-468
Dlaczego małe „słodkie” znaczniki na komórkach nowotworowych mają znaczenie
Większość z nas kojarzy cukier z pożywieniem, ale komórki wykorzystują także złożone łańcuchy cukrowe jako drobne ozdoby na swoich białkach. Te „słodkie” znaczniki mogą zmieniać zachowanie białek i często są zmienione w nowotworach. W tym badaniu zadano konkretne pytanie: czy specyficzne przyłączenia cukrów na dobrze znanym markerze nowotworowym zwanym EpCAM rzeczywiście wpływają na złośliwość komórek raka piersi, czy raczej głównie modyfikują samo białko bez przekształcania przebiegu choroby?
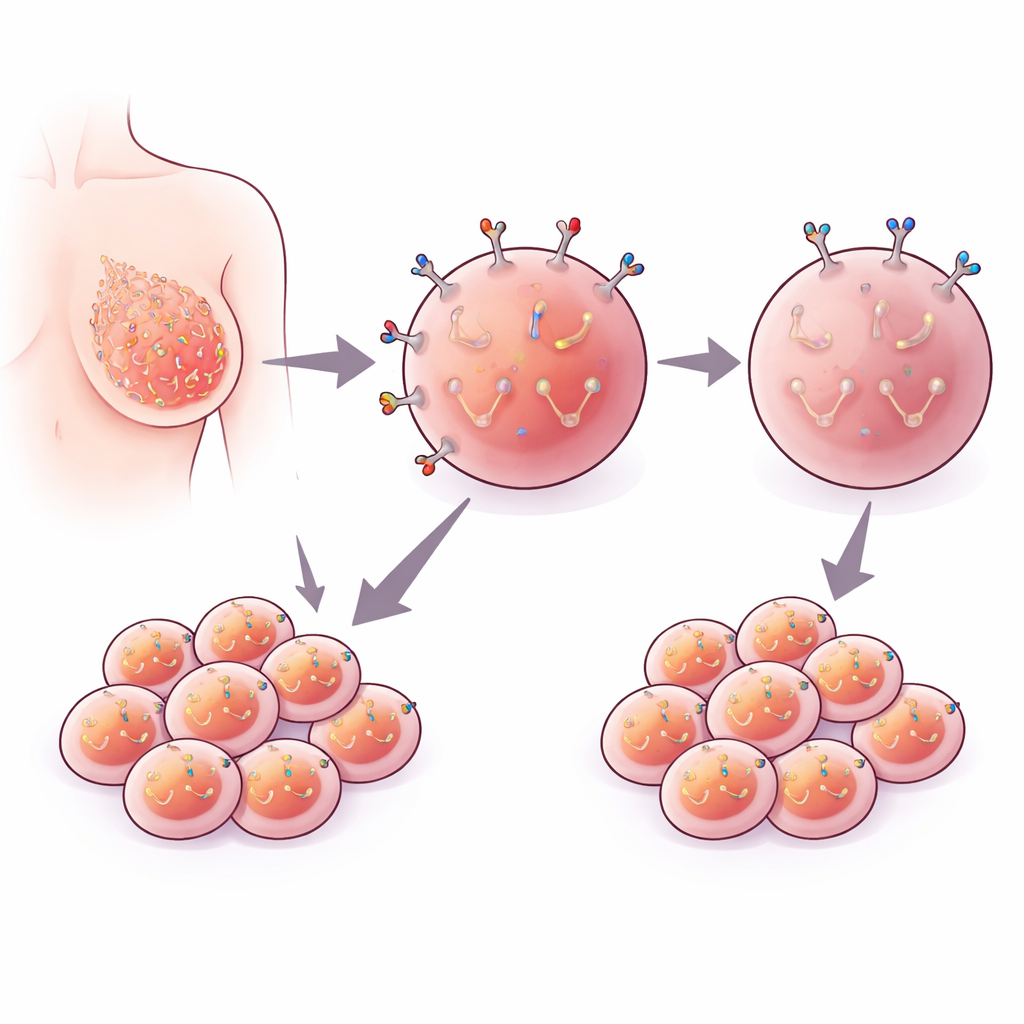
Marker na powierzchni komórki nowotworowej
EpCAM to białko osadzone w błonie zewnętrznej wielu komórek nabłonkowych, w tym komórek piersi. W kilku typach nowotworów komórki guzowe mają znacznie więcej EpCAM na powierzchni niż komórki zdrowe, a pacjenci z guzami o wysokim poziomie EpCAM często mają gorsze rokowanie. Z tego powodu EpCAM stał się popularnym celem testów diagnostycznych i eksperymentalnych terapii. Naukowcy wciąż jednak nie są zgodni, czy EpCAM aktywnie napędza rozprzestrzenianie się raka, czy raczej występuje jako towarzysz powiązany z innymi szkodliwymi zmianami.
Powiększając uwagę na cukrową otoczkę EpCAM
Naturalnie EpCAM nosi trzy małe przyłączenia cukrowe w określonych miejscach swojej struktury. Wcześniejsze badania na próbkach pacjentów sugerowały, że guzy z wyższą zawartością EpCAM wykazywały także więcej określonych rodzajów cukrów, co sugerowało, że ta cukrowa otoczka może wpływać na zachowanie EpCAM w procesie przerzutowania. Bezpośrednie wyłączenie przyłączania cukrów tylko na jednym białku jest technicznie trudne, więc badacze zastosowali inżynierię genetyczną, by obejść ten problem. Pracując na linii komórkowej raka piersi potrójnie ujemnej MDA-MB-468, najpierw stworzyli komórki, w których normalny gen EpCAM został całkowicie usunięty. Następnie wprowadzili albo normalną, zdolną do glikozylacji wersję EpCAM, albo subtelnie zmienioną wersję, w której trzy miejsca akceptujące cukry zostały zmienione tak, że cukry nie mogły się już przyłączyć.
Co się dzieje po usunięciu cukrowych znaczników
Dysponując tym czystym systemem, zespół zmierzył, co dzieje się z samym białkiem EpCAM. Usunięcie miejsc przyłączenia cukrów znacząco obniżyło stabilność EpCAM: po zahamowaniu syntezy nowych białek wersja pozbawiona cukrów degradowała zauważalnie szybciej niż normalne EpCAM. Mikroskopia pokazała też, że wersja bez cukrów nie trafiała tak efektywnie na powierzchnię komórki. Zamiast tego miała tendencję do zatrzymywania się wewnątrz komórki, szczególnie w retikulum endoplazmatycznym — pofałdowanym układzie wewnętrznych błon, gdzie białka są fałdowane i kontrolowane pod kątem jakości. Normalne EpCAM, przeciwnie, koncentrowało się w błonie komórkowej, gdzie może kontaktować się z komórkami sąsiednimi i wchodzić w interakcje z partnerami sygnałowymi.
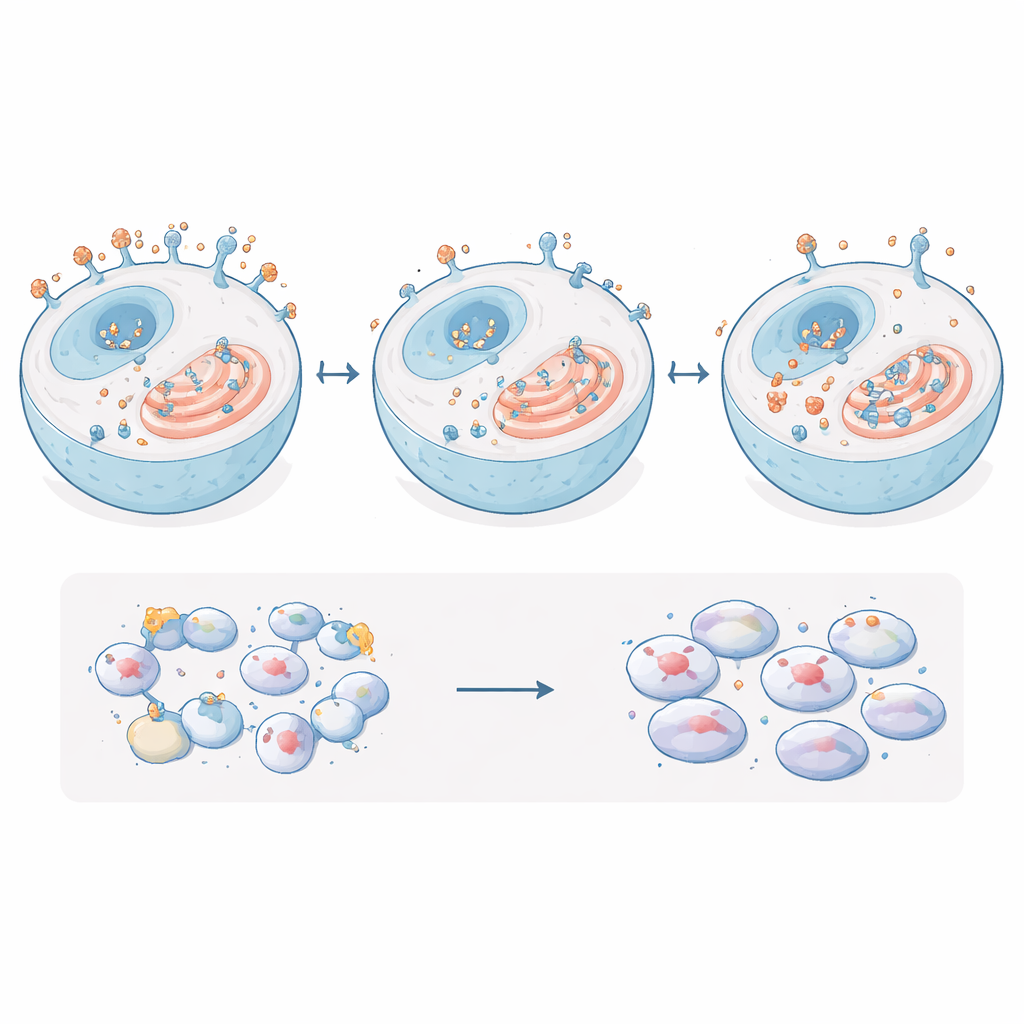
Co w komórkach nowotworowych się nie zmienia
Ponieważ EpCAM wiązane jest z wieloma szlakami wzrostu i przeżycia, badacze zapytali następnie, czy pozbawienie jego cukrów zmienia kluczowe cząsteczki pośredniczące lub zachowania przypominające nowotwór. Zmierzyli zestaw białek i genów często kontrolowanych przez EpCAM, w tym główne regulatory wzrostu i cząsteczki adhezyjne, i nie stwierdzili istotnych zmian przy porównaniu komórek z normalnym EpCAM, bez EpCAM, nadmiernie produkujących EpCAM oraz z EpCAM pozbawionym cukrów. Zespół przeprowadził także standardowe testy laboratoryjne cech związanych z przerzutami: tempo wzrostu komórek, zdolność do przechodzenia przez porowatą barierę, inwazję w żel imitujący tkankę otaczającą oraz siłę adhezji między komórkami. Wszystkie te właściwości pozostały w zasadzie niezmienione po utracie cukrów EpCAM. Tylko gdy EpCAM był silnie nadmiernie eksprymowany, zaobserwowano niewielki wzrost skłonności komórek do zlepiania się.
Co to oznacza dla rozumienia i celowania w EpCAM
Mówiąc wprost, badanie pokazuje, że cukrowa otoczka EpCAM mocno wpływa na stabilność białka i jego lokalizację w komórkach raka piersi, ale sama w sobie nie przekształca tych komórek w bardziej lub mniej agresywne w tym modelu. W komórkach MDA-MB-468 usunięcie cukrów EpCAM czyni białko mniej trwałym i zatrzymuje większą jego część wewnątrz komórki, jednak podstawowe zachowania związane z rozprzestrzenianiem się guza pozostają w dużej mierze takie same. Sugeruje to, że chociaż EpCAM i jego cukrowe dekoracje są istotnymi elementami molekularnej układanki, ich funkcjonalny wpływ może silnie zależeć od typu komórki i kontekstu. Dla projektowania terapii praca podkreśla, że zmiana lub celowanie w wzór glikozylacji EpCAM może modyfikować samo białko bez konieczności wywoływania dramatycznej, przewidywalnej zmiany w zachowaniu niektórych komórek raka piersi.
Cytowanie: Jenkinson, N.M., Oza, H., Yarema, K.J. et al. Functional effects of EpCAM N-glycosylation in MDA-MB-468 breast cancer cells. Sci Rep 16, 10021 (2026). https://doi.org/10.1038/s41598-026-38920-x
Słowa kluczowe: EpCAM, rak piersi, adhezja komórkowa, glikozylacja białek, przerzuty