Clear Sky Science · it
Effetti funzionali della N-glicosilazione di EpCAM nelle cellule di carcinoma mammario MDA-MB-468
Perché piccoli tag zuccherini sulle cellule tumorali contano
La maggior parte di noi pensa allo zucchero come a qualcosa nella dieta, ma le cellule usano anche catene zuccherine complesse come piccole decorazioni sulle loro proteine. Questi tag zuccherini possono modificare il comportamento delle proteine e sono spesso alterati nel cancro. Questo studio pone una domanda mirata: specifici tag zuccherini su un noto marcatore del cancro chiamato EpCAM modificano effettivamente l’aggressività delle cellule del carcinoma mammario, oppure influenzano principalmente la proteina stessa senza rimodellare la malattia?
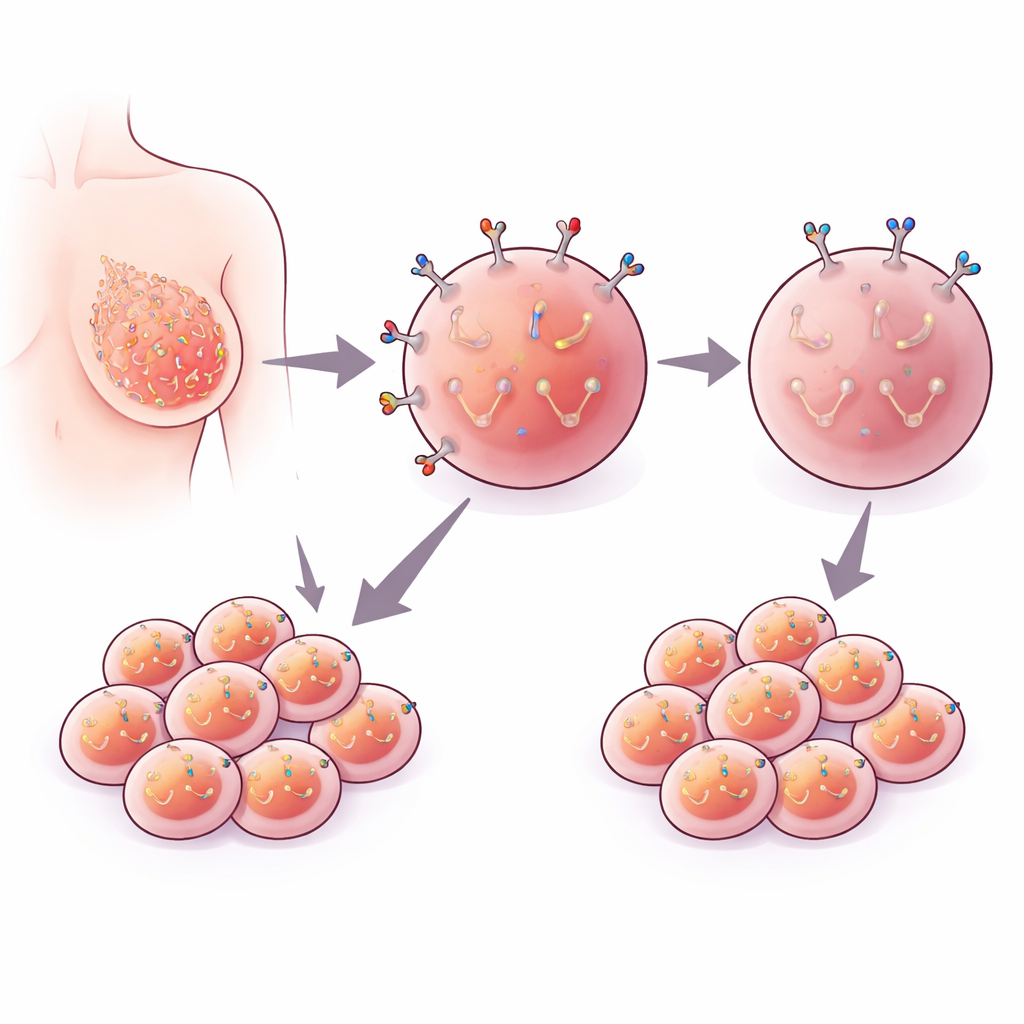
Un marcatore sulla superficie della cellula tumorale
EpCAM è una proteina che si trova nella membrana esterna di molte cellule epiteliali, incluse quelle mammarie. In diversi tumori, le cellule tumorali esprimono molta più EpCAM in superficie rispetto alle cellule sane, e i pazienti i cui tumori presentano alti livelli di EpCAM tendono ad avere una prognosi peggiore. Per questo motivo EpCAM è diventata un bersaglio popolare per test diagnostici e terapie sperimentali. Tuttavia gli scienziati non concordano ancora pienamente sul fatto che EpCAM guidi attivamente la diffusione del cancro o sia semplicemente un marcatore associato ad altri cambiamenti dannosi.
Avvicinarsi al mantello zuccherino di EpCAM
EpCAM porta naturalmente tre piccoli legami zuccherini in posizioni precise della sua struttura. Studi precedenti su pazienti avevano suggerito che i tumori con più EpCAM mostrassero anche un aumento di certi tipi di zuccheri, suggerendo che questo rivestimento zuccherino potesse influenzare il ruolo di EpCAM nelle metastasi. Interrompere direttamente l’aggiunta di zuccheri su una singola proteina è tecnicamente difficile, quindi i ricercatori hanno usato l’ingegneria genetica per aggirare il problema. Lavorando in una linea di carcinoma mammario triplo-negativo chiamata MDA-MB-468, hanno prima creato cellule in cui il gene EpCAM normale era completamente rimosso. Hanno poi reintrodotto o una versione normale, pronta per la glicosilazione, o una versione lievemente modificata in cui i tre siti accettori di zucchero erano cambiati in modo che non potessero più essere glicosilati.
Cosa succede quando i tag zuccherini vengono rimossi
Con questo sistema pulito a disposizione, il gruppo ha misurato cosa accadeva alla proteina EpCAM stessa. La rimozione dei siti di glicosilazione rese EpCAM molto meno stabile: quando alle cellule fu impedita la produzione di nuove proteine, la versione priva di zuccheri di EpCAM si degradò visibilmente più rapidamente rispetto all’EpCAM normale. La microscopia mostrò inoltre che la versione senza zuccheri non raggiungeva la superficie cellulare con la stessa efficienza. Per lo più tendeva a rimanere all’interno della cellula, in particolare nel reticolo endoplasmatico, un sistema membranoso interno dove le proteine vengono piegate e controllate per la qualità. L’EpCAM normale, al contrario, era concentrata nella membrana cellulare dove può contattare le cellule vicine e interagire con partner di segnalazione.
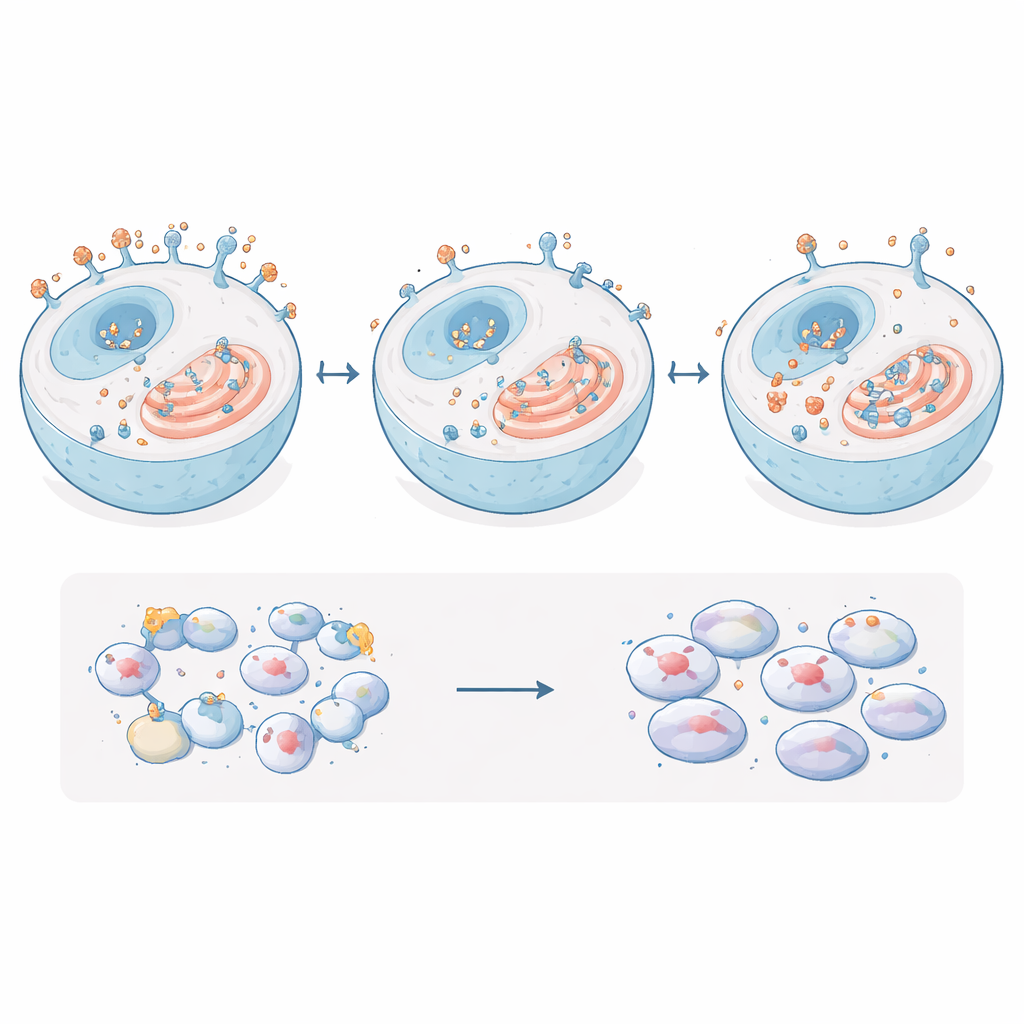
Cosa non cambia all’interno delle cellule tumorali
Poiché EpCAM è stata collegata a molte vie di crescita e sopravvivenza, i ricercatori hanno poi chiesto se la rimozione dei suoi tag zuccherini altersse molecole chiave a valle o comportamenti simili a quelli tumorali. Hanno misurato un insieme di proteine e geni spesso regolati da EpCAM, inclusi importanti regolatori della crescita e molecole di adesione, e non hanno trovato cambiamenti significativi confrontando cellule normali, prive di EpCAM, sovraesprimenti di EpCAM e con EpCAM priva di zuccheri. Il gruppo ha inoltre eseguito test di laboratorio standard per tratti legati alle metastasi: la velocità di crescita delle cellule, la loro capacità di migrare attraverso una barriera porosa, l’attitudine a invadere un gel che imita il tessuto circostante e la forza con cui si aggregano. Tutte queste proprietà rimasero sostanzialmente invariate dalla perdita degli zuccheri di EpCAM. Solo quando EpCAM stessa era fortemente sovraespressa si osservò un incremento modesto nella compattezza dell’aggregazione cellulare.
Cosa significa questo per comprendere e mirare EpCAM
In sintesi, lo studio mostra che il rivestimento zuccherino di EpCAM influenza fortemente la stabilità della proteina e la sua localizzazione nelle cellule di carcinoma mammario, ma di per sé non trasforma queste cellule in uno stato più o meno aggressivo in questo modello. Nelle cellule MDA-MB-468, rimuovere gli zuccheri di EpCAM rende la proteina meno durevole e ne trattiene una quota maggiore all’interno della cellula, tuttavia i comportamenti di base legati alla diffusione tumorale restano per lo più gli stessi. Ciò suggerisce che, sebbene EpCAM e le sue decorazioni zuccherine siano pezzi importanti del puzzle molecolare, il loro impatto funzionale può dipendere fortemente dal tipo cellulare e dal contesto. Per la progettazione di terapie, il lavoro sottolinea che modificare o mirare il profilo zuccherino di EpCAM può alterare la proteina stessa senza produrre necessariamente un cambiamento drammatico e prevedibile nel comportamento di certe cellule di carcinoma mammario.
Citazione: Jenkinson, N.M., Oza, H., Yarema, K.J. et al. Functional effects of EpCAM N-glycosylation in MDA-MB-468 breast cancer cells. Sci Rep 16, 10021 (2026). https://doi.org/10.1038/s41598-026-38920-x
Parole chiave: EpCAM, carcinoma mammario, adesione cellulare, glicosilazione delle proteine, metastasi