Clear Sky Science · fr
Effets fonctionnels de la N-glycosylation d’EpCAM dans les cellules de cancer du sein MDA-MB-468
Pourquoi de petits ornements sucrés sur les cellules cancéreuses comptent
La plupart d’entre nous associent le sucre à notre alimentation, mais les cellules utilisent aussi des chaînes de sucres complexes comme petites décorations sur leurs protéines. Ces étiquettes sucrées peuvent modifier le comportement des protéines et elles sont souvent altérées dans le cancer. Cette étude pose une question ciblée : est-ce que des marques sucrées spécifiques sur un marqueur tumoral bien connu, EpCAM, modifient réellement l’agressivité des cellules du cancer du sein, ou ajustent-elles surtout la protéine elle‑même sans remodeler la maladie ?
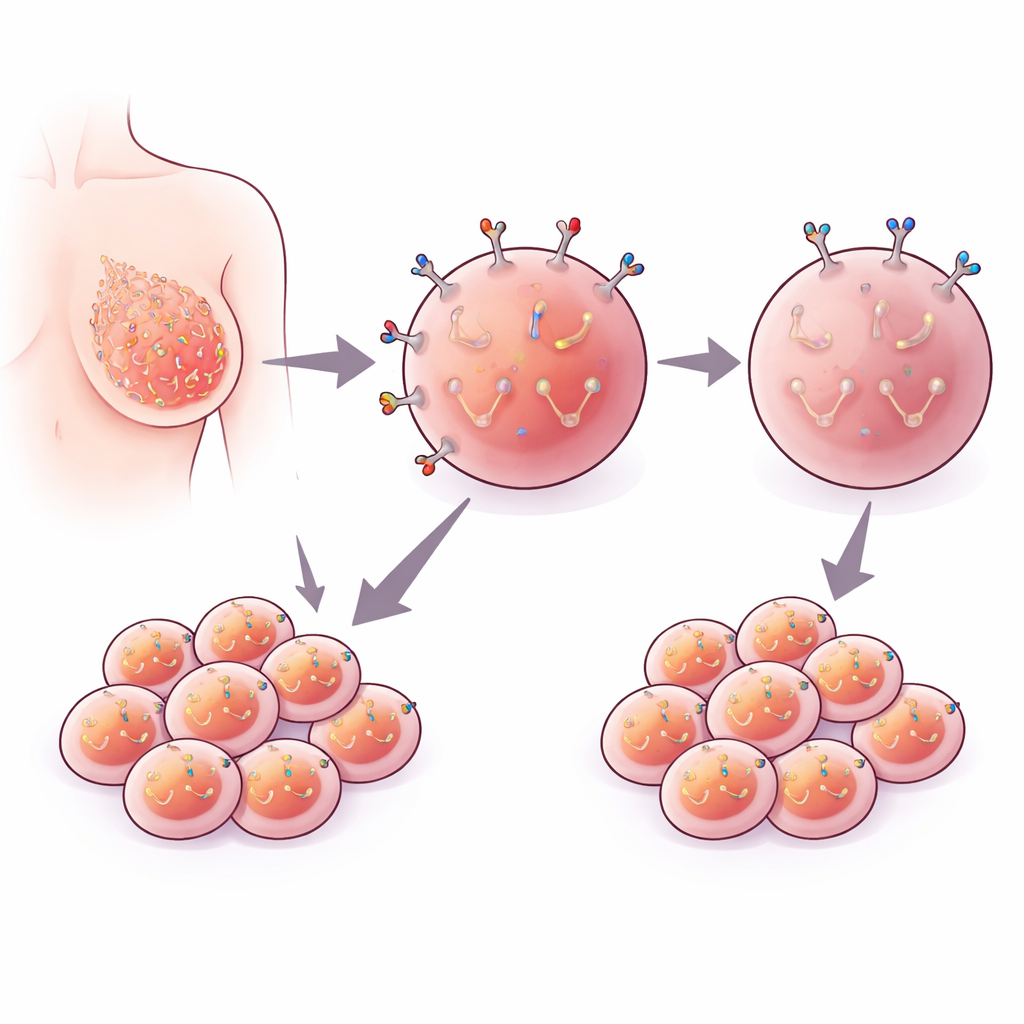
Un marqueur à la surface des cellules cancéreuses
EpCAM est une protéine ancrée dans la membrane externe de nombreuses cellules épithéliales, y compris les cellules mammaires. Dans plusieurs cancers, les cellules tumorales présentent beaucoup plus d’EpCAM à leur surface que les cellules saines, et les patients dont les tumeurs affichent des niveaux élevés d’EpCAM ont souvent un pronostic plus mauvais. Pour cette raison, EpCAM est devenu une cible prisée pour des tests diagnostiques et des thérapies expérimentales. Pourtant, les scientifiques ne s’accordent pas entièrement sur le fait qu’EpCAM pilote activement la dissémination tumorale ou qu’il accompagne seulement d’autres altérations nuisibles en tant que témoin.
Zoom sur le manteau sucré d’EpCAM
EpCAM porte naturellement trois petites liaisons glycosidiques à des positions précises de sa structure. Des études antérieures chez des patients ont suggéré que les tumeurs riches en EpCAM présentaient aussi davantage de certains types de sucres, laissant penser que cette couche sucrée pourrait influencer le rôle d’EpCAM dans la métastase. Éteindre directement l’ajout de sucres sur une seule protéine est techniquement difficile, aussi les chercheurs ont‑ils contourné ce problème par génie génétique. Travaillant sur une lignée de cancer du sein triple négatif, MDA‑MB‑468, ils ont d’abord créé des cellules dont le gène EpCAM avait été complètement supprimé. Ils y ont ensuite réintroduit soit une version normale d’EpCAM capable d’être glycosylée, soit une version subtilement modifiée où les trois sites accepteurs de sucres avaient été altérés pour empêcher l’attachement des sucres.
Que se passe‑t‑il quand les étiquettes sucrées sont retirées
Avec ce système propre en main, l’équipe a mesuré ce qu’il advient de la protéine EpCAM elle‑même. La suppression des sites de glycosylation rend EpCAM beaucoup moins stable : lorsque les cellules ont été traitées pour arrêter la synthèse de nouvelles protéines, la forme dépourvue de sucres d’EpCAM s’est dégradée nettement plus vite que l’EpCAM normale. La microscopie a montré en outre que la version sans sucres n’atteignait pas aussi efficacement la surface cellulaire. Elle avait plutôt tendance à stagner à l’intérieur de la cellule, en particulier dans le réticulum endoplasmique, ce réseau membranaire interne où les protéines sont repliées et contrôlées. L’EpCAM normale, en revanche, se concentrait à la membrane cellulaire où elle peut entrer en contact avec les cellules voisines et interagir avec des partenaires de signalisation.
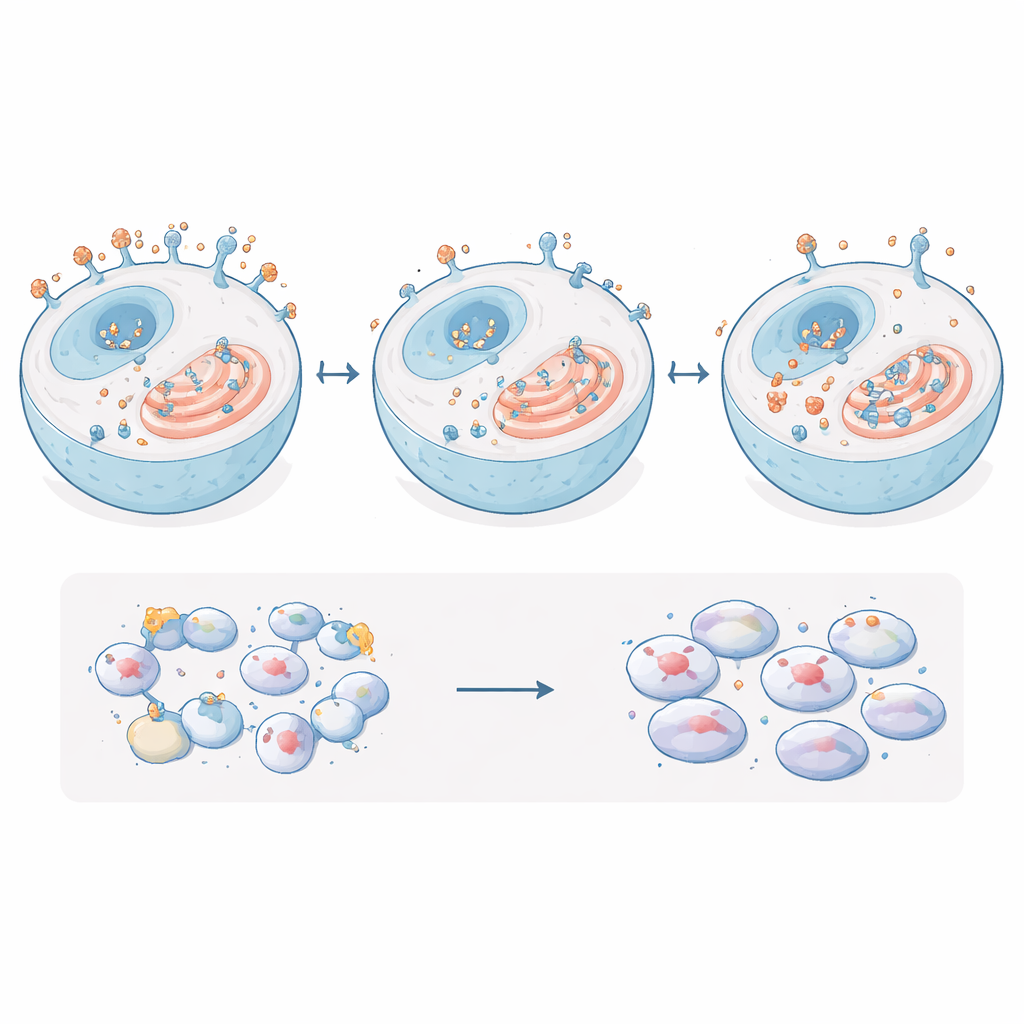
Ce qui ne change pas à l’intérieur des cellules cancéreuses
Parce qu’EpCAM a été relié à de multiples voies de croissance et de survie, les chercheurs ont ensuite cherché à savoir si le retrait de ses sucres altérait des molécules clés en aval ou des comportements associés au cancer. Ils ont mesuré un ensemble de protéines et de gènes souvent contrôlés par EpCAM, y compris des régulateurs majeurs de la croissance et des molécules d’adhésion, et n’ont trouvé aucun changement significatif en comparant les cellules normales, dépourvues d’EpCAM, surexprimant EpCAM, et exprimant l’EpCAM sans sucres. L’équipe a également réalisé des tests standards de laboratoire pour des traits liés à la métastase : vitesse de prolifération, capacité de migration à travers une barrière poreuse, aptitude à envahir un gel qui mime le tissu environnant, et force d’adhésion intercellulaire. Toutes ces propriétés sont restées essentiellement inchangées par la perte des sucres d’EpCAM. Ce n’est que lors d’une forte surexpression d’EpCAM que les chercheurs ont observé une augmentation modeste de la cohésion cellulaire.
Ce que cela signifie pour la compréhension et le ciblage d’EpCAM
En termes simples, l’étude montre que la couche sucrée d’EpCAM influence fortement la stabilité de la protéine et sa localisation dans les cellules de cancer du sein, mais qu’elle n’enclenche pas, à elle seule, un état plus ou moins agressif dans ce modèle. Dans les cellules MDA‑MB‑468, retirer les sucres d’EpCAM rend la protéine moins durable et augmente sa rétention intracellulaire, tandis que les comportements de base liés à la dissémination tumorale demeurent pour l’essentiel les mêmes. Cela suggère que, bien qu’EpCAM et ses décorations sucrées soient des éléments importants du puzzle moléculaire, leur impact fonctionnel dépend fortement du type cellulaire et du contexte. Pour la conception de thérapies, ce travail souligne que modifier ou cibler le profil glycannique d’EpCAM peut altérer la protéine elle‑même sans nécessairement produire un changement dramatique et prévisible du comportement de certaines cellules du cancer du sein.
Citation: Jenkinson, N.M., Oza, H., Yarema, K.J. et al. Functional effects of EpCAM N-glycosylation in MDA-MB-468 breast cancer cells. Sci Rep 16, 10021 (2026). https://doi.org/10.1038/s41598-026-38920-x
Mots-clés: EpCAM, cancer du sein, adhésion cellulaire, glycosylation des protéines, métastase