Clear Sky Science · sv
Dominanta kloner utnyttjar utvecklingsmässiga epigenomiska tillstånd för att driva ependymom
Varför barns hjärntumörer börjar så tidigt
Några av de svåraste barndomshjärntumörerna tycks uppstå ur intet och motstå dagens behandlingar. Denna studie ställer en förrädiskt enkel fråga: varför ger vissa genetiska olyckor upphov till aggressiva tumörer endast hos små barn, och endast i mycket specifika delar av hjärnan? Genom att spåra hur den utvecklande hjärnans ”epigenetiska” landskap — dess mönster av öppen och stängd DNA — samspelar med en kraftfull cancerframkallande genfusion, visar författarna hur tidiga tillväxtprogram kapras för att så ett livslångt sjukdomstillstånd.
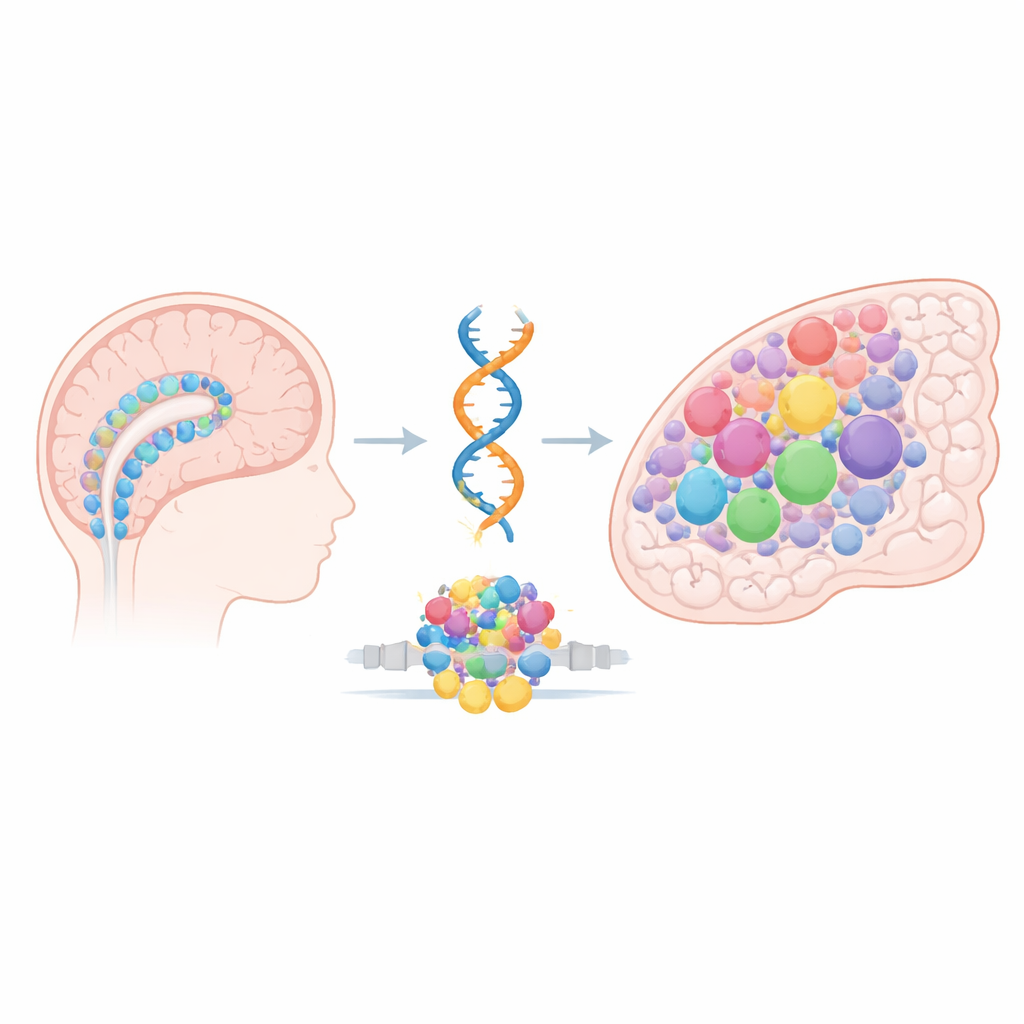
Tidiga hjärnbildare och en farlig fusion
Forskargruppen fokuserar på ependymom, en barndomshjärntumör som ofta uppstår i storhjärnsbarken och är ökänd för att vara svår att behandla. Många av dessa tumörer bär på samma genetiska fel: en fusion mellan två gener kallade ZFTA och RELA, som ger upphov till ett hybridprotein som kan slå på genprogram olämpligt. Ändå förekommer denna fusion, känd som ZFTA–RELA, nästan uteslutande hos barn och i ett trängt hjärnområde. Författarna misstänkte att svaret inte bara ligger i mutationen i sig, utan i vilka celler som finns — och hur deras DNA:s ”åtkomlighetskarta” ser ut — när fusionen uppstår. I det embryonala hjärnan fungerar radiella glialceller och andra cyklande progenitorer som huvudbyggare och ger upphov till neuroner och stödjeceller. Dessa celler bär tillfälliga epigenetiska tillstånd som håller många tillväxt- och utvecklingsgener i beredskap. Studien frågar om dessa kortlivade tillstånd skapar ett fönster av särskild sårbarhet för fusionen.
Kartläggning av sårbara tillstånd i den utvecklande hjärnan
För att undersöka detta fönster använde forskarna single-nucleus ”multiome”-sekvensering för att läsa både genaktivitet och kromatinåtkomlighet i tiotusentals musframhjärneceller från mitten av graviditeten till strax efter födseln. De fann att specifika DNA-ställen som känns igen av en familj transkriptionsfaktorer kallade PLAG/L var vida öppna i radiella glialceller och cyklande progenitorer, men blev mycket mindre tillgängliga när cellerna mognade till neuroner och oligodendrocyter. Med hjälp av en biokemisk screen visade de att ZFTA–RELA-fusionsproteinet starkt föredrar just dessa PLAG/L-typiska DNA-motiv. Slående nog, när de konstgjort introducerade fusionen i renade radiella glialceller, förändrades den globala kromatinåtkomligheten knappt, men tusentals nedströmsgener slog på. Detta tyder på att fusionen inte skapar nya vägar genom genomet; istället ”kopplar den in” i utvecklingsmoduler som redan är öppna i progenitorceller och återanvänder dem för onkogen tillväxt.
Från normal utveckling till störd tumörtillväxt
Författarna modellerade sedan ependymom i möss genom att introducera fusionen i embryonala kortikala progenitorer in utero och profilerade de resulterande tumörerna med samma multiome-ansats. Dessa tumörer var överraskande heterogena: vissa celler liknade radiell glia eller aktivt cyklande progenitorer, medan andra såg mer ut som omogna neuroner eller astrocyter. Till skillnad från ett fullständigt utvecklingsstopp reflekterade detta mönster en ofullständig marsch längs normala differentieringsvägar. Ändå visade endast en liten undergrupp av progenitorliknande och radiell glial–liknande celler stark cellcykelaktivitet; de flesta mer differentierade cellerna bar fusionens genuttryckssignatur men delade sig sällan. I parallella experiment misslyckades samma fusion att effektivt utlösa tumörer när den tvingades in i mer mogna oligodendrocytprekursorer, vilket förstärker idén att endast vissa utvecklingsstadier med rätt öppna kromatin är verkligt i riskzonen.
Gemensamma mekanismer över mänskliga tumörer
När teamet undersökte enskilda celler från mänskliga patienttumörer — inklusive ZFTA–RELA-ependymom, posteriora fossa-ependymom och besläktade tumörer drivna av PLAG/L-genfusioner — såg de en liknande bild. ZFTA–RELA- och PLAG/L-fusionstumörer klustrade tillsammans efter sina kromatinlandskap och visade en markant berikning av PLAG/L-typiska DNA-motiv i åtkomliga regioner, även om de exakta generna som slogs på kunde skilja sig åt. Inom ZFTA–RELA-tumörer spände de maligna cellerna återigen över ett spektrum av tillstånd, från progenitorliknande till neuronal-, astrocyt- och ependymal-liknande, med hög PLAG/L-motivaktivitet kvar även i celler som normalt skulle ha ”stängt” dessa utvecklingsmoduler. Denna persistens av ett embryonalt epigenetiskt program in i senare celltyper tycks vara ett centralt förenande tema.
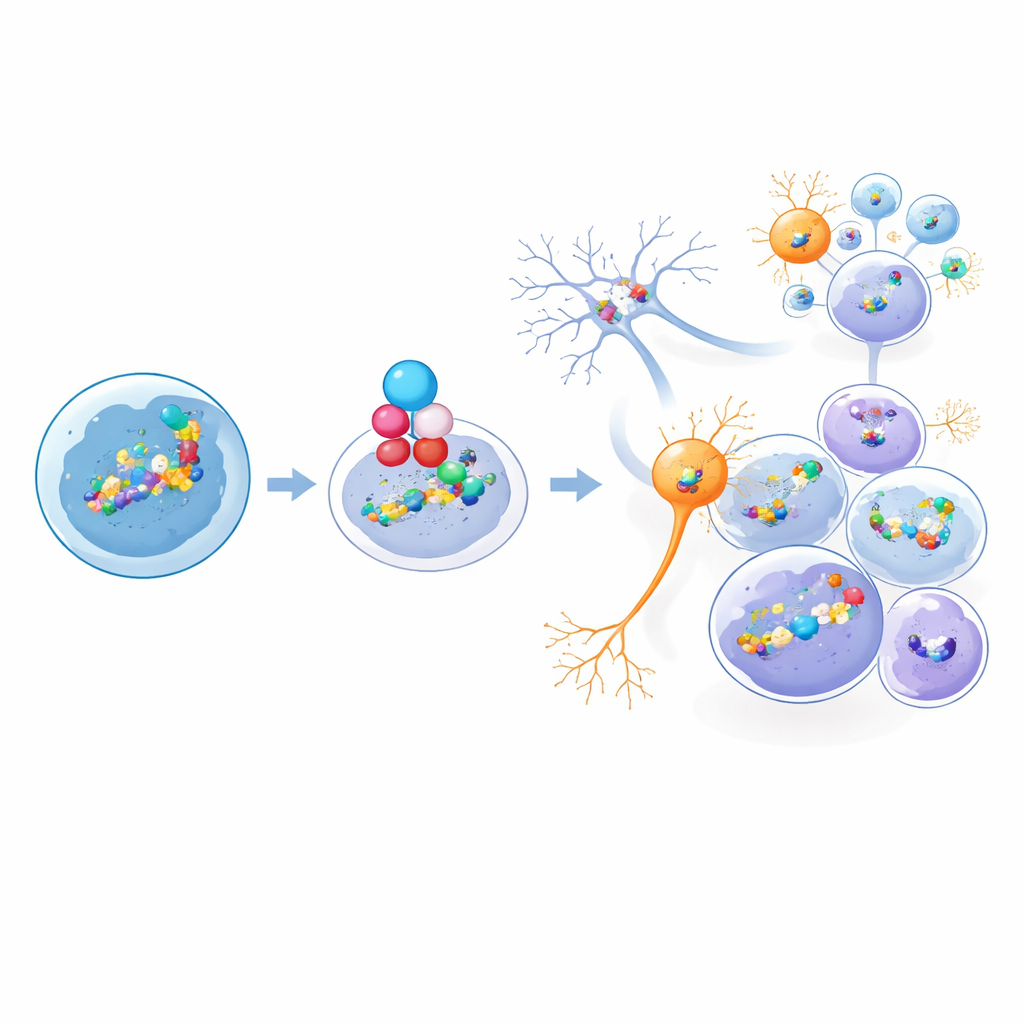
Hur ett fåtal kloner formar hela tumören
För att förstå hur denna mångfald uppstår över tid använde forskarna ett barcodingsystem som märker individuella celler i embryonala mus hjärna innan tumörer bildas. Att följa dessa barcodes in i fullskaliga tumörer visade att, även om många omvandlade celler dyker upp tidigt, tar en enda eller ett mycket litet antal ”dominanta” kloner typiskt över lesionen. Viktigt är att dessa dominanta kloner ger upphov till hela spektrat av tumörcelltyper, från proliferativa progenitorliknande celler till mer kviescenta neuronal- och astrocytliknande celler. Beräkningsmässiga ”pseudotids”-analyser i både mus- och människaprover stöder en hierarki där en minoritet av cyklande progenitorliknande celler sitter i toppen och matar in i dessa mångfacetterade, till största delen icke-delande grenar.
Vad detta betyder för barn med ependymom
Sammantaget visar arbetet att en barndomshjärntumör inte uppstår enbart på grund av en potent mutation, utan därför att mutationen hamnar i en cell vars utvecklingsmässiga epigenetiska tillstånd är förberett för att bli kaprat. ZFTA–RELA-fusionen hakar sig fast vid PLAG/L-styrda DNA-moduler som normalt bara är aktiva en kort tid i tidiga progenitorer, och håller tillväxtfrämjande gener påslagna medan cellerna försöker mogna. Några tidiga kloner som utnyttjar denna sårbarhet expanderar sedan och bildar ett komplext men övervägande icke-cykliskt tumörekosystem, vilket kan förklara varför standardbehandlingar som riktar sig mot delning ofta misslyckas. Genom att peka ut de specifika utvecklingsstadierna och kromatinmodulerna i riskzonen föreslår studien nya strategier som antingen stänger dessa epigenetiska fönster eller tvingar maligna progenitorer att fullständigt differentiera och lämna cellcykeln.
Citering: Kardian, A.S., Sun, H., Ippagunta, S. et al. Dominant clones leverage developmental epigenomic states to drive ependymoma. Nature 652, 1027–1037 (2026). https://doi.org/10.1038/s41586-026-10270-8
Nyckelord: barnhjärntumörer, ependymom, epigenetiska tillstånd, genfusion, radiella glialceller