Clear Sky Science · de
Dominante Klone nutzen entwicklungsbedingte epigenomische Zustände, um Ependymom voranzutreiben
Warum Hirntumoren bei Kindern so früh beginnen
Einige der schwierigsten kindlichen Hirntumoren tauchen scheinbar aus dem Nichts auf und widerstehen den heutigen Therapien. Diese Studie stellt eine trügerisch einfache Frage: Warum führen bestimmte genetische Unfälle zu aggressiven Tumoren nur bei Kleinkindern und nur in sehr spezifischen Hirnregionen? Indem die Autoren nachzeichnen, wie die „epigenetische“ Landschaft des sich entwickelnden Gehirns – das Muster offener und geschlossener DNA – mit einer potenten krebsverursachenden Genfusion interagiert, decken sie auf, wie frühe Wachstumsprogramme gekapert werden, um eine lebenslange Krankheit zu begründen.
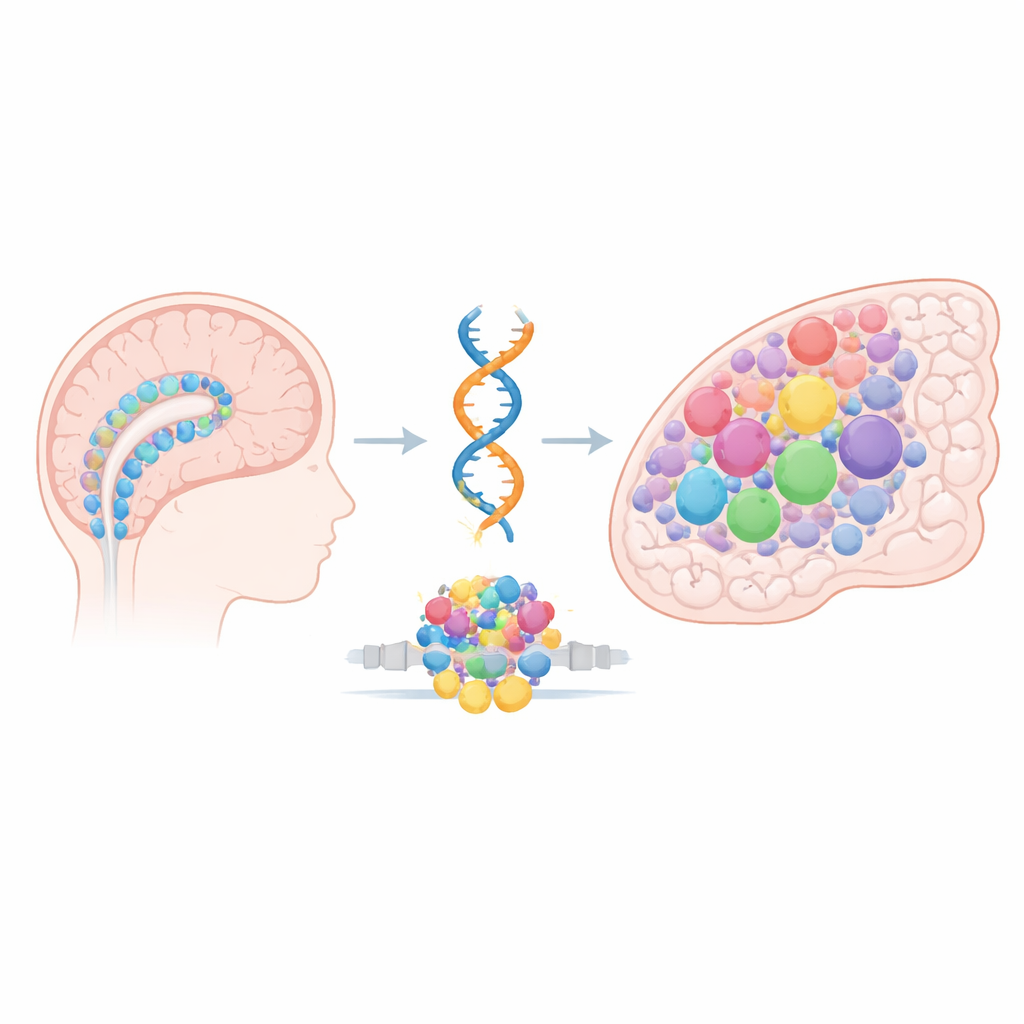
Frühe Hirnbaumeister und eine gefährliche Fusion
Das Team konzentriert sich auf Ependymom, einen pädiatrischen Hirntumor, der häufig im Kortex entsteht und bekanntlich schwer zu behandeln ist. Viele dieser Tumoren tragen denselben genetischen Defekt: eine Fusion zwischen zwei Genen namens ZFTA und RELA, die ein Hybridprotein erzeugt, das Genprogramme unangemessen einschalten kann. Doch diese Fusion, bekannt als ZFTA–RELA, tritt fast ausschließlich bei Kindern und in einer engen Hirnregion auf. Die Autoren vermuteten, dass die Antwort nicht nur in der Mutation selbst liegt, sondern darin, welche Zellen vorhanden sind – und wie deren DNA‑„Zugänglichkeitskarte“ aussieht –, wenn die Fusion entsteht. Im embryonalen Gehirn fungieren radiale Gliazellen und andere teilende Vorläufer als Baumeister und liefern Neuronen und Stützzellen. Diese Zellen tragen vorübergehende epigenetische Zustände, die viele Wachstums‑ und Entwicklungsgene in Bereitschaft halten. Die Studie fragt, ob diese kurzlebigen Zustände ein Fenster besonderer Verwundbarkeit gegenüber der Fusion schaffen.
Vulnerable Zustände im sich entwickelnden Gehirn kartieren
Um dieses Fenster zu untersuchen, nutzten die Forscher Einzelkern‑„Multiom“-Sequenzierung, um sowohl Genaktivität als auch Chromatinzugänglichkeit in Zehntausenden von Mäuse‑Vorderhirnzellen von der mittleren Gestation bis kurz nach der Geburt zu lesen. Sie fanden heraus, dass spezifische DNA‑Stellen, die von einer Familie von Transkriptionsfaktoren namens PLAG/L erkannt werden, in radialen Gliazellen und teilenden Vorläufern weit geöffnet waren, aber deutlich weniger zugänglich wurden, als sich die Zellen zu Neuronen und Oligodendrozyten differenzierten. Mithilfe eines biochemischen Screens zeigten sie, dass das ZFTA–RELA‑Fusionsprotein genau diese PLAG/L‑artigen DNA‑Motive stark bevorzugt. Auffällig war, dass bei künstlicher Einführung der Fusion in gereinigte radiale Gliazellen die globale Chromatinzugänglichkeit kaum veränderte, jedoch Tausende nachgeschalteter Gene aktiviert wurden. Das deutet darauf hin, dass die Fusion keine neuen Pfade im Genom aufreißt, sondern sich in bereits in Vorläuferzellen offene Entwicklungs‑Module „einsteckt“ und diese für onkogenes Wachstum umnutzt.
Von normaler Entwicklung zu gestörtem Tumorwachstum
Die Autoren modellierten dann Ependymom bei Mäusen, indem sie die Fusion in embryonale kortikale Vorläufer in utero einführten und die resultierenden Tumoren mit demselben Multiom‑Ansatz profilierten. Diese Tumoren waren überraschend heterogen: Einige Zellen ähnelten radialen Glia- oder aktiv teilenden Vorläufern, während andere unreiferen Neuronen oder Astrozyten glichen. Anders als bei einem vollständigen Entwicklungsstopp spiegelte dieses Muster einen unvollständigen Verlauf normaler Differenzierungswege wider. Doch nur eine kleine Untergruppe von vorläuferähnlichen und radial‑glialen Zellen zeigte starke Zellzyklusaktivität; die meisten differenziert wirkenden Zellen trugen zwar die Genexpressionssignatur der Fusion, teilten sich aber selten. In parallelen Experimenten scheiterte die erzwungene Einführung derselben Fusion in reifere Oligodendrozytenvorläufer daran, effizient Tumoren auszulösen, was die Idee stützt, dass nur bestimmte Entwicklungsstadien mit der richtigen offenen Chromatinlandschaft wirklich gefährdet sind.
Gemeinsame Mechanismen in humanen Tumoren
Als das Team Einzelzellen aus humanen Patiententumoren untersuchte – einschließlich ZFTA–RELA‑Ependymomen, posterior fossa Ependymomen und verwandten Tumoren, die durch PLAG/L‑Genfusionen angetrieben werden – sahen sie ein ähnliches Bild. ZFTA–RELA‑ und PLAG/L‑Fusions‑Tumoren gruppierten sich nach ihren Chromatinlandschaften und zeigten eine ausgeprägte Anreicherung von PLAG/L‑artigen DNA‑Motiven in zugänglichen Regionen, obwohl die exakt aktivierten Gene variieren konnten. Innerhalb von ZFTA–RELA‑Tumoren reichten die malignen Zellen erneut über ein Spektrum von Zuständen, von vorläuferähnlich bis neuronal‑, astrozyten‑ und ependymal‑ähnlich, wobei die PLAG/L‑Motivaktivität hoch blieb – selbst in Zellen, die diese Entwicklungsmodule normalerweise bereits „geschlossen“ hätten. Dieses Persistieren eines embryonalen epigenetischen Programms in spätere Zelltypen scheint ein zentrales, einigendes Thema zu sein.
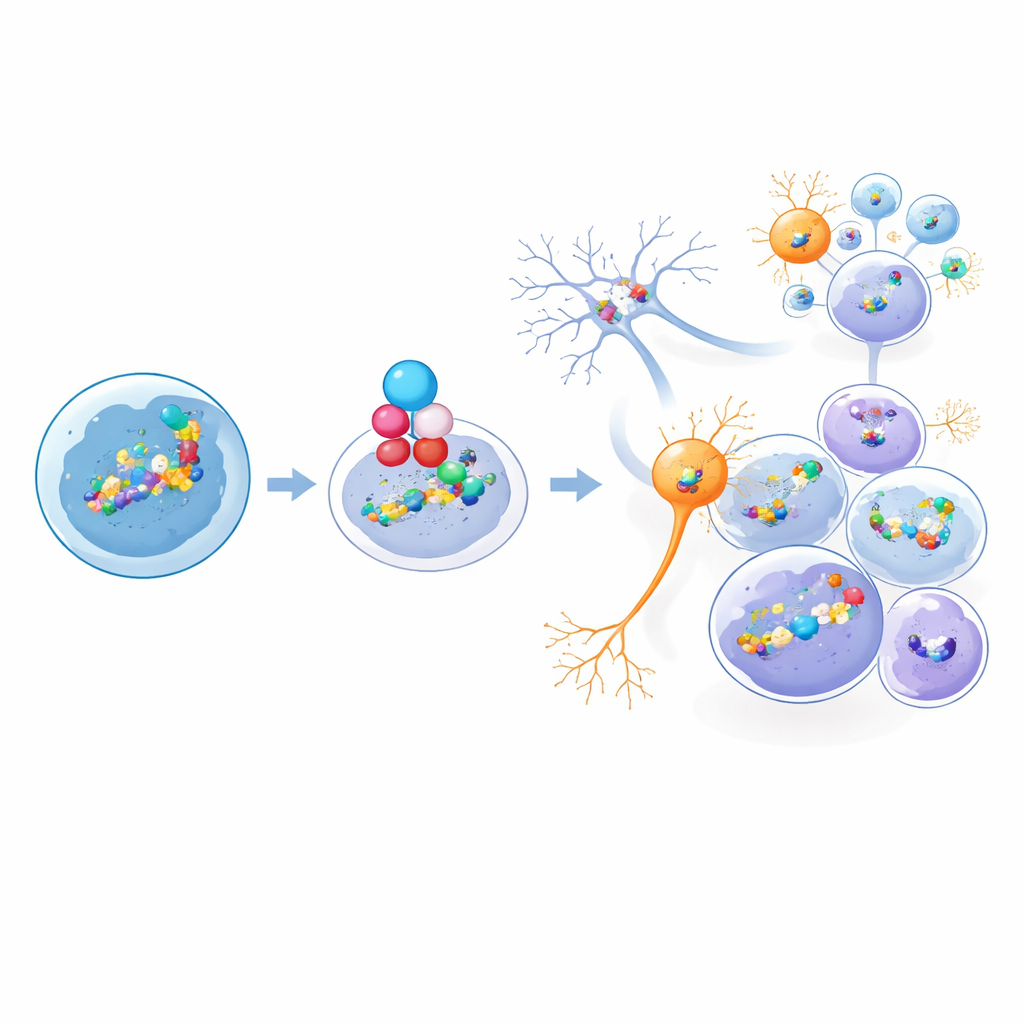
Wie wenige Klone den ganzen Tumor formen
Um zu verstehen, wie diese Vielfalt im Laufe der Zeit entsteht, nutzten die Forscher ein Barcoding‑System, das einzelne Zellen im embryonalen Mausgehirn markiert, bevor Tumoren entstehen. Die Nachverfolgung dieser Barcodes in ausgewachsene Tumoren zeigte, dass, obwohl viele transformierte Zellen früh auftauchen, typischerweise ein einzelner oder sehr wenige „dominante“ Klone die Läsion übernehmen. Wichtig ist, dass diese dominanten Klone die gesamte Bandbreite der Tumorzelltypen hervorbringen, von proliferativen vorläuferähnlichen Zellen bis zu ruhigeren neuronal‑ und astrozytenähnlichen Zellen. Computergestützte „Pseudotime“-Analysen in Maus‑ und Humanproben stützen eine Hierarchie, in der eine Minderheit zyklischer vorläuferähnlicher Zellen an der Spitze steht und in diese vielfältigen, größtenteils nicht teilenden Zweige speist.
Was das für Kinder mit Ependymom bedeutet
Zusammengefasst zeigt die Arbeit, dass ein kindlicher Hirntumor nicht allein wegen einer potenten Mutation entstehen kann, sondern weil diese Mutation in einer Zelle landet, deren entwicklungsbedingter epigenetischer Zustand darauf vorbereitet ist, gekapert zu werden. Die ZFTA–RELA‑Fusion heftet sich an PLAG/L‑kontrollierte DNA‑Module, die normalerweise nur kurz in frühen Vorläufern aktiv sind, und hält wachstumsfördernde Gene eingeschaltet, während die Zellen sich zu differenzieren versuchen. Wenige frühe Klone, die diese Verwundbarkeit ausnutzen, expandieren dann und erzeugen ein komplexes, aber größtenteils nicht teilendes Tumorökosystem, was teilweise erklären könnte, warum Standardtherapien, die auf Zellteilung abzielen, oft versagen. Indem die Studie die spezifischen Entwicklungszustände und Chromatinmodule identifiziert, die gefährdet sind, legt sie nahe, neue Strategien zu verfolgen: entweder diese epigenetischen Fenster zu schließen oder maligne Vorläufer dazu zu bringen, vollständig zu differenzieren und den Zellzyklus zu verlassen.
Zitation: Kardian, A.S., Sun, H., Ippagunta, S. et al. Dominant clones leverage developmental epigenomic states to drive ependymoma. Nature 652, 1027–1037 (2026). https://doi.org/10.1038/s41586-026-10270-8
Schlüsselwörter: pädiatrische Hirntumoren, Ependymom, epigenetische Zustände, Genfusion, radiale Gliazellen