Clear Sky Science · it
I cloni dominanti sfruttano stati epigenomici dello sviluppo per guidare l’ependimoma
Perché i tumori cerebrali nei bambini iniziano così presto
Alcuni dei tumori cerebrali infantili più difficili da trattare sembrano comparire dal nulla e resistere alle terapie attuali. Questo studio pone una domanda apparentemente semplice: perché certi incidenti genetici provocano tumori aggressivi solo nei bambini piccoli e solo in regioni molto specifiche del cervello? Seguendo come il paesaggio «epigenetico» del cervello in sviluppo—il modello di DNA aperto e chiuso—interagisce con una potente fusione genica oncogenica, gli autori rivelano come i programmi di crescita precoci vengano dirottati per fare nascere una malattia che dura tutta la vita.
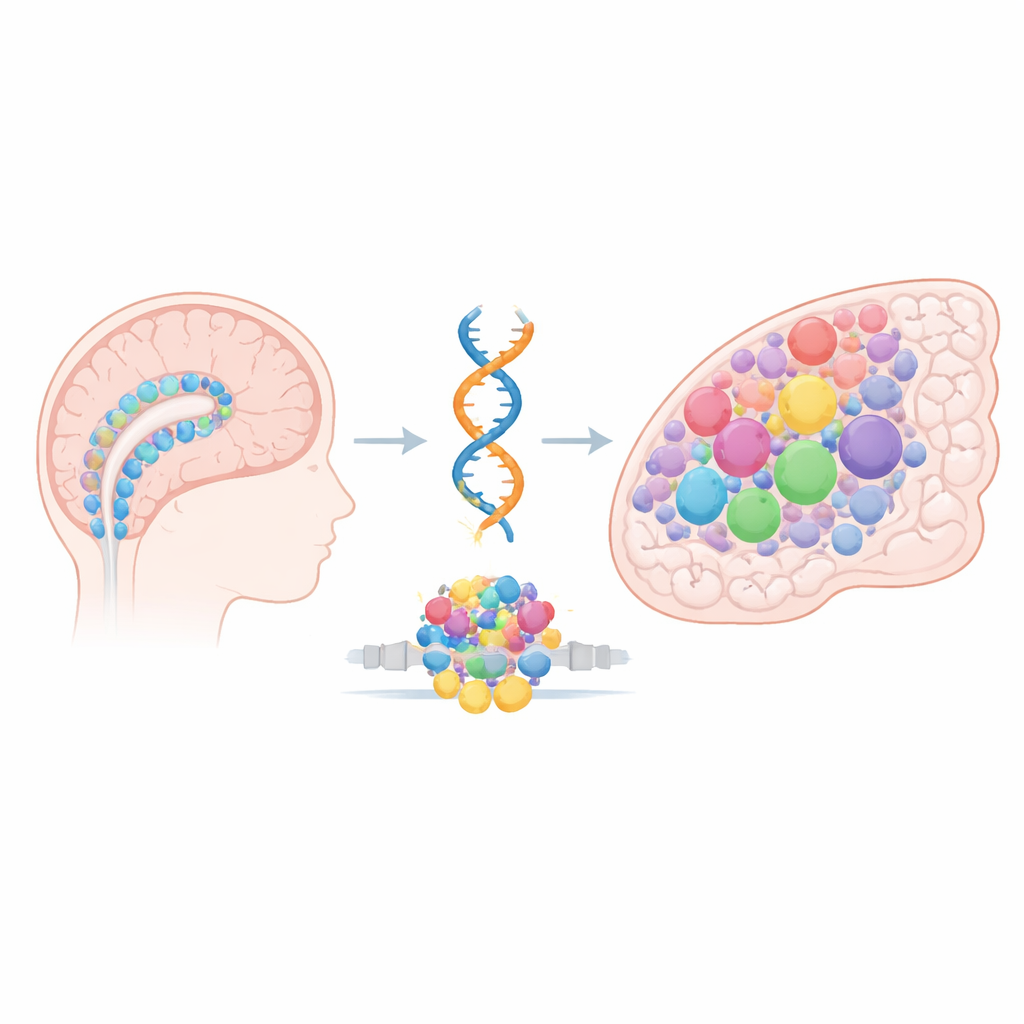
I primi costruttori cerebrali e una fusione pericolosa
Il gruppo si concentra sull’ependimoma, un tumore cerebrale pediatrico che spesso insorge nella corteccia cerebrale ed è notoriamente difficile da trattare. Molti di questi tumori presentano lo stesso difetto genetico: una fusione tra due geni chiamati ZFTA e RELA, che produce una proteina ibrida capace di attivare in modo inappropriato programmi genici. Tuttavia questa fusione, nota come ZFTA–RELA, compare quasi esclusivamente nei bambini e in una regione cerebrale ristretta. Gli autori hanno ipotizzato che la risposta non risieda soltanto nella mutazione, ma nelle cellule presenti—e nella «mappa di accessibilità» del loro DNA—quando la fusione si verifica. Nel cervello embrionale, le cellule gliali radiali e altri progenitori in ciclo fungono da principali costruttori, dando origine a neuroni e cellule di supporto. Queste cellule presentano stati epigenetici temporanei che mantengono molti geni di crescita e sviluppo pronti per l’attivazione. Lo studio indaga se questi stati di breve durata creino una finestra di vulnerabilità speciale alla fusione.
Mappare gli stati vulnerabili nel cervello in sviluppo
Per sondare quella finestra, i ricercatori hanno usato il sequenziamento «multiome» a singolo nucleo per leggere sia l’attività genica sia l’accessibilità della cromatina in decine di migliaia di cellule del prosencefalo di topo dalla metà della gestazione fino a poco dopo la nascita. Hanno scoperto che siti di DNA specifici riconosciuti da una famiglia di fattori di trascrizione chiamata PLAG/L erano ampiamente aperti nelle cellule gliali radiali e nei progenitori in ciclo, ma diventavano molto meno accessibili man mano che le cellule maturavano in neuroni e oligodendrociti. Utilizzando uno screening biochimico, hanno dimostrato che la proteina di fusione ZFTA–RELA preferisce fortemente proprio questi motivi di DNA di tipo PLAG/L. Sorprendentemente, quando hanno introdotto artificialmente la fusione in cellule gliali radiali purificate, l’accessibilità globale della cromatina è cambiata appena, eppure migliaia di geni a valle sono stati attivati. Questo suggerisce che la fusione non traccia nuovi percorsi nel genoma; invece, si «inserisce» nei moduli di sviluppo già aperti nei progenitori e li riconverte per la crescita oncogenica.
Da uno sviluppo normale a una crescita tumorale disordinata
Gli autori hanno poi modellato l’ependimoma nei topi introducendo la fusione nei progenitori corticali embrionali in utero e profilando i tumori risultanti con lo stesso approccio multiome. Questi tumori si sono mostrati sorprendentemente eterogenei: alcune cellule somigliavano a glia radiale o a progenitori attivamente in ciclo, mentre altre avevano un aspetto più vicino a neuroni immaturi o astrociti. Piuttosto che un blocco completo dello sviluppo, questo schema rifletteva un avanzamento incompleto lungo le vie di differenziazione normali. Tuttavia solo un piccolo sottoinsieme di cellule di tipo progenitore e glia radiale mostrava intensa attività del ciclo cellulare; la maggior parte delle cellule dall’aspetto differenziato portava la firma di espressione genica della fusione ma si divideva di rado. In esperimenti paralleli, forzare la stessa fusione in precursori di oligodendrociti più maturi non è riuscito a innescare tumori in modo efficiente, rafforzando l’idea che soltanto certi stadi dello sviluppo con la cromatina aperta appropriata siano davvero a rischio.
Meccanismi condivisi nei tumori umani
Quando il gruppo ha esaminato singole cellule da tumori umani di pazienti—tra cui ependimomi ZFTA–RELA, ependimomi della fossa posteriore e tumori correlati guidati da fusioni geniche PLAG/L—ha osservato un quadro simile. I tumori con fusione ZFTA–RELA e quelli con fusioni PLAG/L si raggruppavano insieme in base ai loro paesaggi cromatinici, mostrando un’evidente arricchimento di motivi di tipo PLAG/L nelle regioni accessibili, anche se i geni attivati potevano variare. All’interno degli ependimomi ZFTA–RELA, le cellule maligne spaziavano nuovamente tra diversi stati, da progenitore-simili a neuronali-simili, astrocito-simili e ependimali-simili, con l’attività del motivo PLAG/L che rimaneva elevata anche in cellule che normalmente avrebbero «chiuso» questi moduli di sviluppo. Questa persistenza di un programma epigenetico embrionale in tipi cellulari più maturi sembra essere un tema unificante centrale.
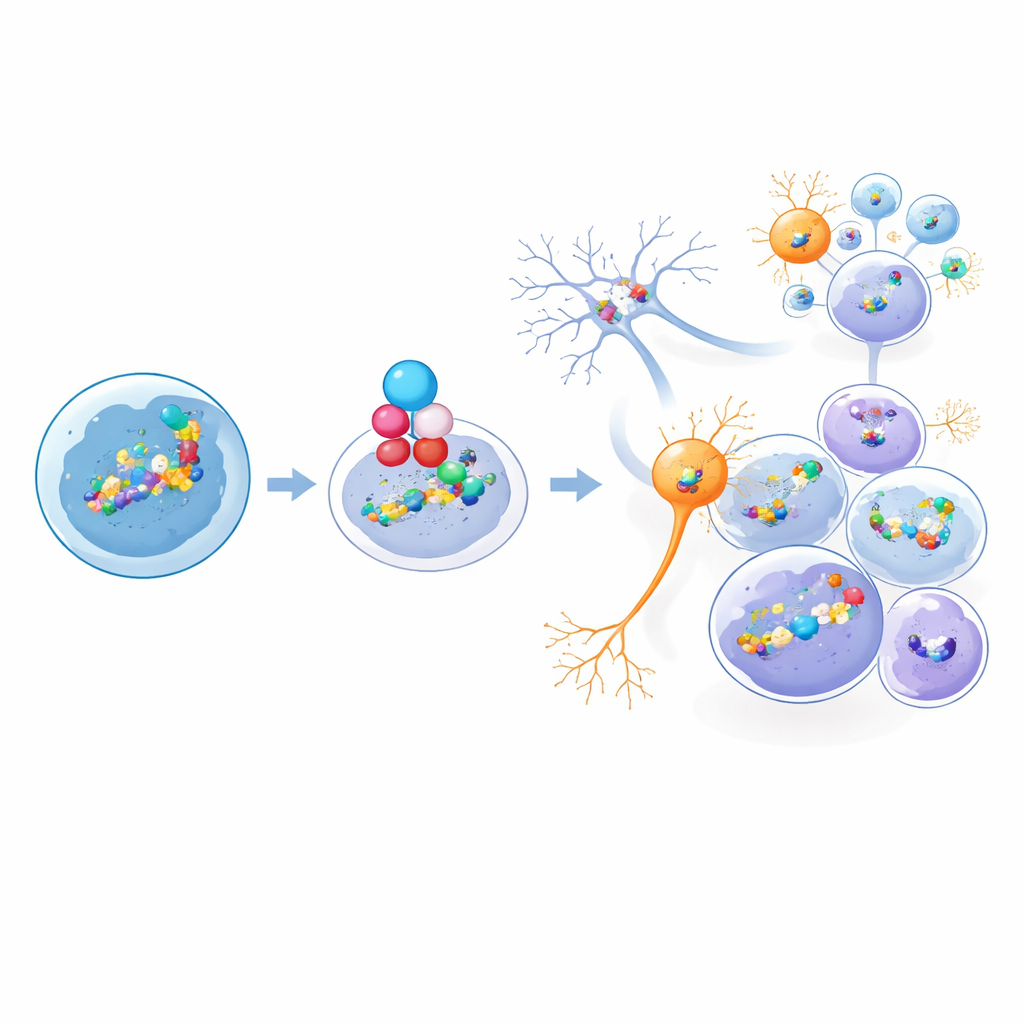
Come pochi cloni plasmano l’intero tumore
Per capire come questa diversità emergesse nel tempo, i ricercatori hanno usato un sistema di barcoding che marca singole cellule nel cervello embrionale del topo prima che i tumori si formino. Tracciando questi barcode nei tumori completamente sviluppati hanno scoperto che, sebbene molte cellule trasformate appaiano precocemente, un clone singolo o un numero molto piccolo di cloni «dominanti» tende tipicamente a imporsi sulla lesione. È importante che quei cloni dominanti diano origine all’intera gamma di tipi cellulari tumorali, dalle cellule progenitrici proliferative a cellule neuronali- e astrocitiche più quiescenti. Analisi computazionali di «pseudotempo» sia nei campioni murini sia umani supportano una gerarchia in cui una minoranza di cellule progenitrici in ciclo sta al vertice e alimenta questi rami diversi e per lo più non in divisione.
Cosa significa per i bambini con ependimoma
Nel complesso, il lavoro mostra che un tumore cerebrale infantile può nascere non semplicemente a causa di una mutazione potente, ma perché quella mutazione si verifica in una cellula il cui stato epigenetico di sviluppo è pronto per essere dirottato. La fusione ZFTA–RELA si ancora a moduli di DNA controllati da PLAG/L che sono normalmente attivi solo brevemente nei progenitori precoci, mantenendo attivati geni che promuovono la crescita mentre le cellule cercano di maturare. Pochi cloni precoci che sfruttano questa vulnerabilità si espandono poi e generano un ecosistema tumorale complesso ma per lo più non proliferante, il che può aiutare a spiegare perché le terapie standard che mirano alla divisione cellulare spesso falliscono. Identificando gli specifici stati di sviluppo e i moduli di cromatina a rischio, questo studio suggerisce nuove strategie che o chiudono queste finestre epigenetiche o inducono i progenitori maligni a differenziarsi completamente ed uscire dal ciclo cellulare.
Citazione: Kardian, A.S., Sun, H., Ippagunta, S. et al. Dominant clones leverage developmental epigenomic states to drive ependymoma. Nature 652, 1027–1037 (2026). https://doi.org/10.1038/s41586-026-10270-8
Parole chiave: tumori cerebrali pediatrici, ependimoma, stati epigenetici, fusione genica, cellule gliali radiali