Clear Sky Science · ar
العينات المهيمنة تستغل الحالات الإبيجنومية التطورية لدفع الأورام السحائية
لماذا تبدأ أورام دماغ الأطفال مبكراً جداً
بعض أصعب أورام دماغ الأطفال تبدو وكأنها تظهر من العدم وتقاوم العلاجات الحالية. يطرح هذا البحث سؤالاً بسيطاً في الظاهر: لماذا تتسبب حوادث جينية معينة في نشوء أورام عدوانية فقط لدى الأطفال الصغار، وفقط في أجزاء محددة جداً من الدماغ؟ من خلال تتبع كيف يتفاعل «المشهد الإبيجنومي» للدماغ النامي — نمط فتح وإغلاق الحمض النووي — مع اندماج جيني قوي مسبب للسرطان، يكشف الباحثون كيف تُختطف برامج النمو المبكرة لزرع مرض يدوم مدى الحياة.
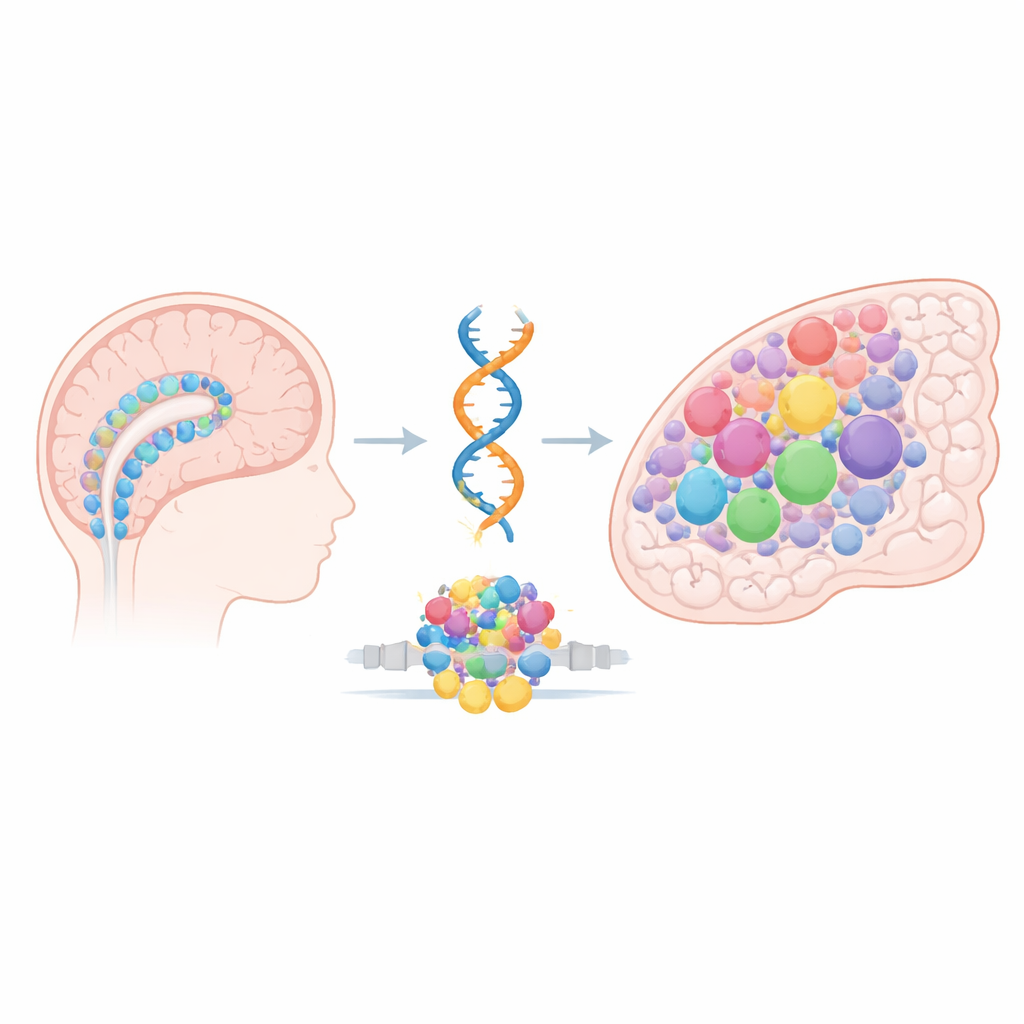
البنّاءون المبكرون واندماج خطر
ركّز الفريق على السحائيوم، وهو ورم دماغي أطفال غالباً ما ينشأ في قشرة المخ ويشتهر بصعوبة علاجه. يحمل العديد من هذه الأورام نفس الخلل الجيني: اندماج بين جينين يسمى ZFTA و RELA، منتجاً بروتيناً هجيناً يمكنه تشغيل برامج جينية بطريقة غير مناسبة. ومع ذلك، يظهر هذا الاندماج، المعروف باسم ZFTA–RELA، تقريباً حصرياً لدى الأطفال وفي منطقة دماغية ضيّقة. ظنّ المؤلفون أن الجواب لا يكمن في الطفرة وحدها، بل في أي الخلايا تكون موجودة — وما تبدو عليه «خريطة وصول» الحمض النووي الخاصة بها — عندما يظهر الاندماج. في الدماغ الجنيني، تعمل الخلايا الغليالية الشعاعية وغيرها من الخلايا الجذعية الدورية كبنّائين رئيسيين، مولدةً الخلايا العصبية وخلايا الدعم. تحمل هذه الخلايا حالات إبيجنومية مؤقتة تبقي العديد من جينات النمو والتطور في حالة استعداد للتشغيل. يسأل البحث عما إذا كانت هذه الحالات قصيرة العمر تخلق نافذة من القابلية الخاصة للاختطاف بواسطة الاندماج.
رسم خرائط الحالات المعرضة في الدماغ النامي
لاستكشاف تلك النافذة، استخدم الباحثون تسلسل «متعدد الأوم» للنواة الواحدة لقراءة كل من نشاط الجينات ووصول الكروماتين في عشرات الآلاف من خلايا مقدمة الدماغ لدى الفأر من منتصف الحمل إلى وقت قصير بعد الولادة. وجدوا أن مواقع حمض نووي معينة يتعرف عليها عائلة من عوامل النسخ تسمى PLAG/L كانت مفتوحة على نطاق واسع في الخلايا الغليالية الشعاعية والخلايا الجذعية الدورية، لكنها أصبحت أقل وصولاً بكثير مع نضوج الخلايا إلى خلايا عصبية وخلايا دبقية قليلة المحاور. باستخدام فحص بيوكيميائي، أظهروا أن بروتين الاندماج ZFTA–RELA يفضّل بقوة بالذات هذه الحوافز النمطية من نوع PLAG/L في الحمض النووي. والمثير أنه عندما أدخلوا الاندماج صناعياً في خلايا غليالية شعاعية منقاة، لم يتغير وصول الكروماتين عالمياً بكثير، ومع ذلك تم تشغيل آلاف الجينات اللاحقة. هذا يوحي بأن الاندماج لا يشق طرقاً جديدة عبر الجينوم؛ بل «يلتصق» بوحدات تطويرية مفتوحة بالفعل في الخلايا الجذعية ويعيد توظيفها للنمو الأورامي.
من التطور الطبيعي إلى نمو الأورام المعيب
بعد ذلك نمذج المؤلفون السحائيوم في الفئران عن طريق إدخال الاندماج في الخلايا الجذعية القشرية الجنينية داخل الرحم وتحليل الأورام الناتجة بنفس نهج المتعدد الأوم. كانت هذه الأورام متنوعة بشكل مفاجئ: شُبّهت بعض الخلايا بالخلايا الغليالية الشعاعية أو بالخلايا الجذعية النشطة دورياً، بينما بدا البعض الآخر أشبه بالخلايا العصبية غير الناضجة أو بالخلايا النجمية. وعلى عكس عائق تنموي كامل، عكست هذه البنية مسيرة غير مكتملة على طول مسارات التمايز الطبيعية. ومع ذلك، أظهر فقط جزء صغير من الخلايا الشبيهة بالخلايا الجذعية والغليالية نشاط دورة خلوية قوي؛ أما معظم الخلايا التي تبدو متمايزة فحملت توقيع التعبير الجيني للاندماج لكنها انقسمت نادراً. في تجارب موازية، فشل إجبار نفس الاندماج في مراحل أكثر نضجاً من مستقبلات الخلايا قليلة المحاور في تحفيز الأورام بفعالية، مما يعزز فكرة أن فقط مراحل تطورية معينة ذات كروماتين مفتوح هي المعرضة للخطر حقاً.
آليات مشتركة عبر أورام بشرية
عندما فحص الفريق خلايا مفردة من أورام مرضى بشريين — بما في ذلك سحائيومات ZFTA–RELA، وسحائيومات الحفرة الخلفية، وأورام ذات صلة يقودها اندماجات جينية من نوع PLAG/L — رأوا صورة مشابهة. تكتلت أورام ZFTA–RELA وأورام اندماج PLAG/L معاً بحسب مشاهدها الكروماتينية، مظهرةً ثراءً واضحاً في حوافز DNA من نوع PLAG/L في المناطق القابلة للوصول، حتى وإن اختلفت الجينات الدقيقة المشغلة. داخل أورام ZFTA–RELA، امتدت الخلايا الخبيثة مرة أخرى عبر مجموعة من الحالات، من شبيهة بالجذعية إلى شبيهة بالعصبونية والنجمية والإبنديمية، وظلت نشاطات نمط PLAG/L مرتفعة حتى في خلايا مفترض أن تكون قد «أغلقت» هذه الوحدات التطورية طبيعياً. يبدو أن استمرار برنامج إبيجنومي جنيني إلى أنواع خلوية لاحقة هو موضوع موحد مركزي.
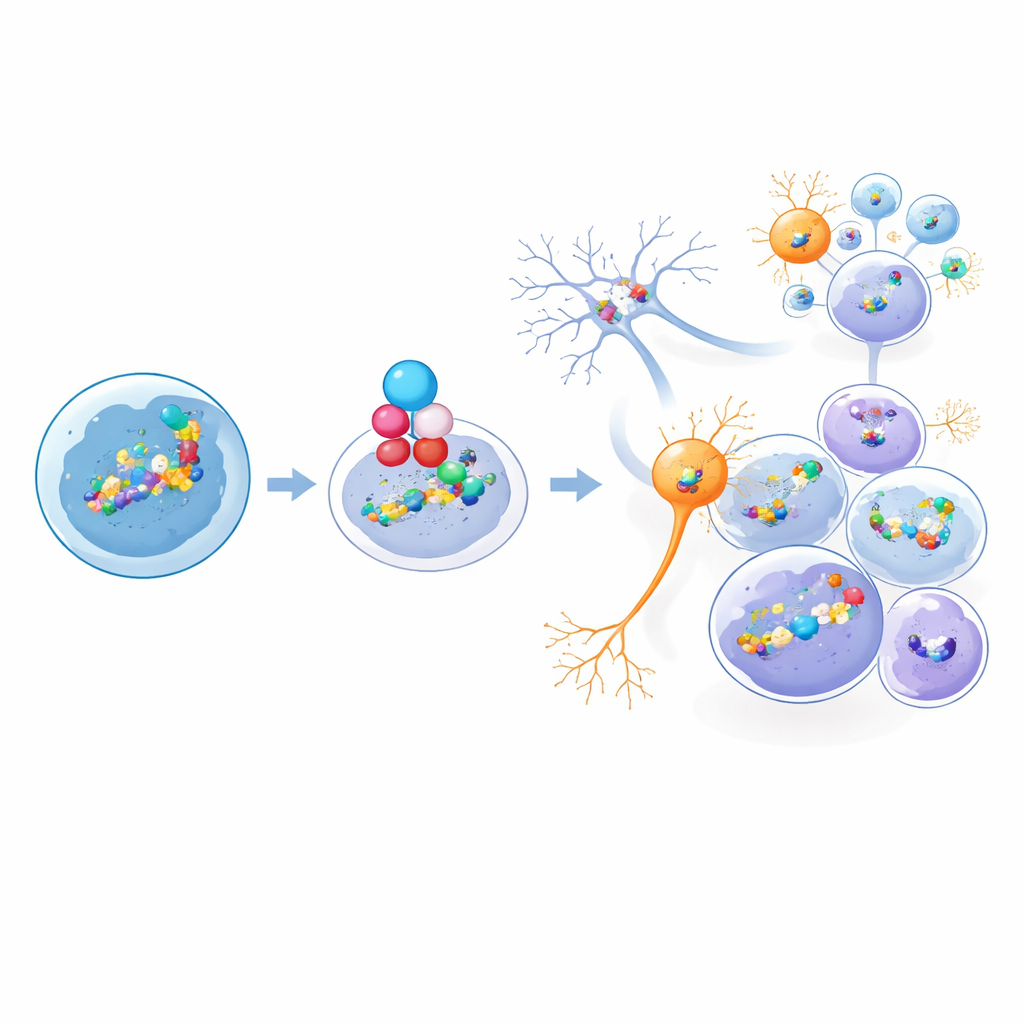
كيف تشكّل عدد قليل من النسائل الورم بأكمله
لفهم كيف تنشأ هذه التنوعات مع مرور الوقت، استخدم الباحثون نظام ترميز شريطي يعلّم الخلايا الفردية في دماغ الفأر الجنيني قبل تكوّن الأورام. أظهر تتبع هذه الرموز الشريطية داخل الأورام المتكاملة أنه، رغم ظهور العديد من الخلايا المتحوّلة مبكراً، فإن نسخة واحدة أو عدد صغير جداً من النسائل «المهيمنة» تسيطر عادة على الآفة. والأهم أن تلك النسائل المهيمنة تنتج النطاق الكامل لأنواع خلايا الورم، من خلايا شبيهة بالجذعية سريعة التكاثر إلى خلايا شبيهة بالعصبونات والنجمات أكثر سكوناً. تدعم تحليلات «الزمن الزائف» الحاسوبية في عينات الفأر والبشر هيكلة هرمية يكون فيها أقلية من الخلايا الجذعية الدورية في القمة وتغذي فروعاً متنوعة إلى حد كبير غير قابلة للانقسام.
ماذا يعني هذا للأطفال المصابين بالسحائيوم
تُظهر هذه الدراسة مجتمعة أن ورم الدماغ الطفولي قد ينشأ ليس ببساطة بسبب طفرة قوية، بل لأن تلك الطفرة تصيب خلية حالتها الإبيجنومية التطورية مهيأة ليتم اختطافها. يلتحم اندماج ZFTA–RELA بوحدات DNA الخاضعة لتحكم PLAG/L التي تكون نشطة طبيعياً لفترة وجيزة فقط في السلفيات المبكرة، محافظاً على تشغيل جينات معززة للنمو بينما تحاول الخلايا النضوج. ثم تتوسع بعض النسائل المبكرة التي تستغل هذه القابلية لتولد منظومة ورمية معقدة لكنها في الغالب غير منقسمة، مما قد يفسر فشل العلاجات القياسية المستهدفة للانقسام. من خلال تحديد الحالات التطورية ووحدات الكروماتين المعرضة للخطر تحديداً، يقترح هذا البحث استراتيجيات جديدة إما لسد هذه النوافذ الإبيجنومية أو لدفع السلفيات الخبيثة إلى التمايز الكامل والخروج من دورة الخلية.
الاستشهاد: Kardian, A.S., Sun, H., Ippagunta, S. et al. Dominant clones leverage developmental epigenomic states to drive ependymoma. Nature 652, 1027–1037 (2026). https://doi.org/10.1038/s41586-026-10270-8
الكلمات المفتاحية: أورام الدماغ الطفولية, السحائيوم, الحالات اللاجينية, الاندماج الجيني, خلايا الغليال الشعاعية