Clear Sky Science · sv
Thyrotropin‑frisättande hormon‑neuroner i olika hypotalamiska kärnor ökar energiförbrukningen
Varför hjärnceller som bränner kalorier är viktiga
De flesta tänker på ämnesomsättningen som något som styrs av hormoner från körtlar som sköldkörteln. Denna studie går djupare och undersöker små kluster av hjärnceller som frisätter en budbärare kallad thyrotropin‑frisättande hormon (TRH) hos möss. Forskarna visar att olika grupper av dessa celler fungerar som separata ”energihubbar”, där var och en finjusterar hur mycket värme kroppen producerar, hur mycket den rör sig och hur mycket den äter. Att förstå dessa kretsar kan peka på nya sätt att bekämpa fetma och diabetes genom att få kroppen att förbränna fler kalorier som värme istället för att lagra dem som fett.
Olika hjärnhubbar, ett gemensamt mål för bränsle
Teamet fokuserade på flera regioner i hypotalamus, ett centralt kontrollcentrum djupt i hjärnan, och på ett område i hjärnstammen. De undrade om TRH‑producerande neuroner i varje region hjälper till att kontrollera kroppens energianvändning. Genom att använda virus som spårämnen kartlade de kopplingar mellan dessa neuroner och brunt fett, en särskild typ av fett som förbränner energi för att producera värme. De använde sedan en kemogenetisk strömbrytare—en konstruerad receptor som aktiveras av ett ofarligt designerläkemedel—för att slå på och av utvalda TRH‑neurongrupper i levande möss medan de mätte kroppstemperatur, aktivitet i brunt fett, rörelse och födointag.
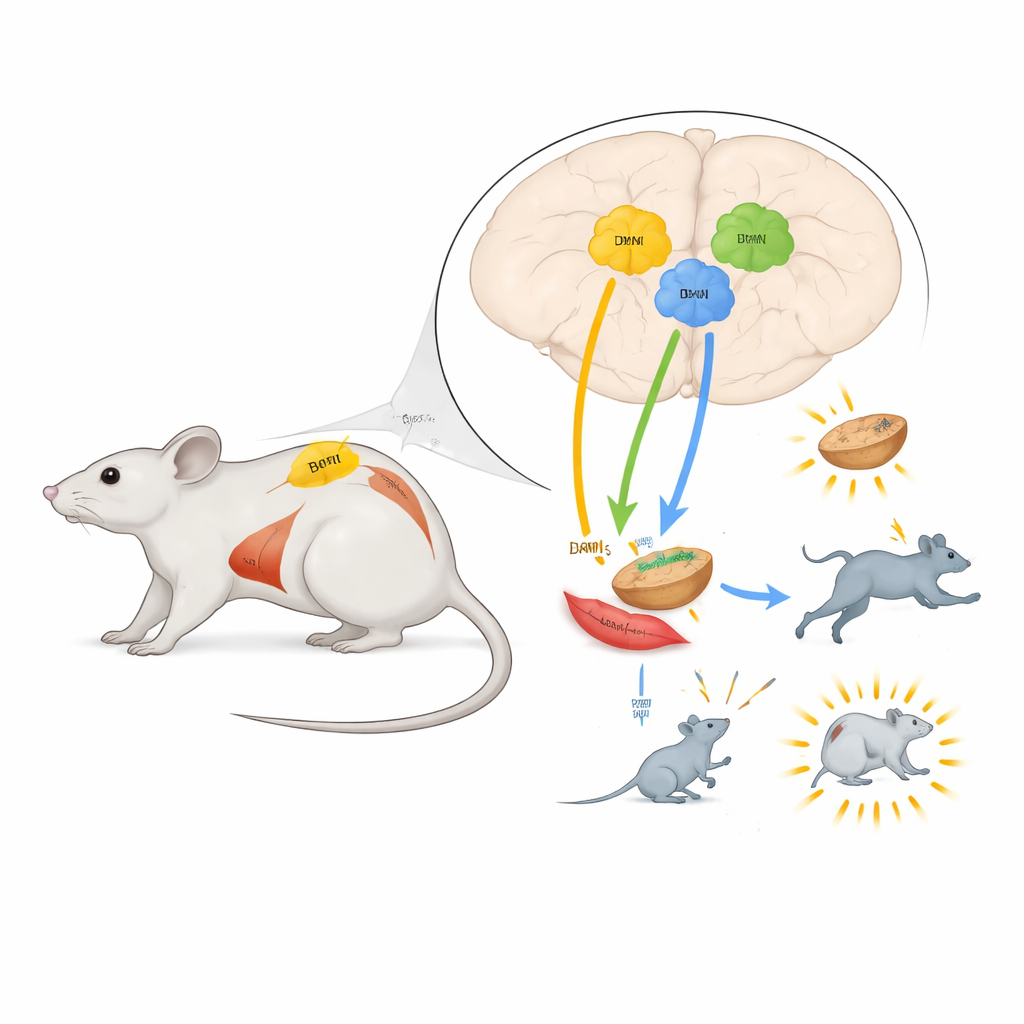
Brunfetts‑förbrännare i två nyckelregioner
I nucleus paraventricularis (PVN) och i dorsomediala hypotalamus (DMH) ökade aktivering av TRH‑neuron kraftigt hur många kalorier mössen förbrände och höjde deras kärntemperatur. Infraröd avbildning visade att bruna fettlager mellan skulderbladen blev varmare, och molekylära tester bekräftade att enzymer som är inblandade i fettnedbrytning i brunt fett aktiverades. Blockering av en specifik typ av adrenalinreceptor i fettceller förhindrade denna uppvärmning, vilket visar att dessa hjärnceller driver brunt fett via det sympatiska nervsystemet, samma system som förbereder kroppen för ”kamp eller flykt”. Dessa förändringar i energianvändning och temperatur kvarstod även när djuren inte tilläts äta, vilket visar att de inte bara var en bieffekt av ökat födointag.
En rörelse‑hub som skyddar mot kyla
En annan bild framträdde i det mediala preoptiska området (MPA), en region som länge är känd för att känna av kroppstemperatur. Att aktivera TRH‑neuroner här ökade också energianvändningen och kroppstemperaturen, men brunt fett förblev relativt tyst. Istället blev mössen mer aktiva: de rörde sig mer i sina burar, vilket tyder på att muskelarbete och allmän upphetsning stod för mycket av den extra värmen. När forskarna kroniskt tystade dessa MPA‑TRH‑neuroner och sedan utsatte mössen för en plötslig sänkning av rumstemperaturen, föll djurens kroppstemperatur brantare och de lyckades inte öka sin energiförbrukning. Detta visar att MPA‑TRH‑neuroner är avgörande för att sätta igång ett korrekt kylaförsvar, sannolikt genom att driva beteende och muskelaktivitet snarare än att direkt slå på brunt fett.
Inte alla TRH‑celler formar ämnesomsättningen
Forskarna undersökte också TRH‑neuroner i en hjärnstamsregion kallad rostral raphe pallidus, som tidigare misstänkts hjälpa till att kontrollera brunt fett. Överraskande nog hade aktivering av dessa celler liten effekt på energianvändning, rörelse, brunfettemperatur eller ätande. Detta antyder att det inte räcker att vara kopplad till brunt fett; bara vissa TRH‑positiva kretsar ändrar faktiskt hur mycket energi kroppen förbrukar.
Bortom klassiska sköldkörtelhormoner
TRH är mest känt för att trigga frisättning av tyreoideastimulerande hormon och sköldkörtelhormoner, som i stort höjer ämnesomsättningen. Här aktiverade endast PVN‑TRH‑neuroner denna hormonkedja. Ändå beroende inte de snabba ökningar i brunfettsvärme och energianvändning som drivs av PVN‑ och DMH‑TRH‑neuroner på den huvudsakliga TRH‑receptorn som kontrollerar frisättning av sköldkörtelhormon. Även när denna receptor genetiskt togs bort gjorde aktivering av PVN‑TRH‑neuroner fortfarande brunt fett varmare och höjde kroppstemperaturen. Ett TRH‑likt läkemedel, däremot, krävde den receptorn för att öka energianvändningen. Denna uppdelning visar att samma kemiska budbärare stöder åtminstone två system: ett långsammare, kroppsomfattande hormonellt system och ett snabbare, nervbaserat system som löper genom specifika TRH‑neurongrupper.
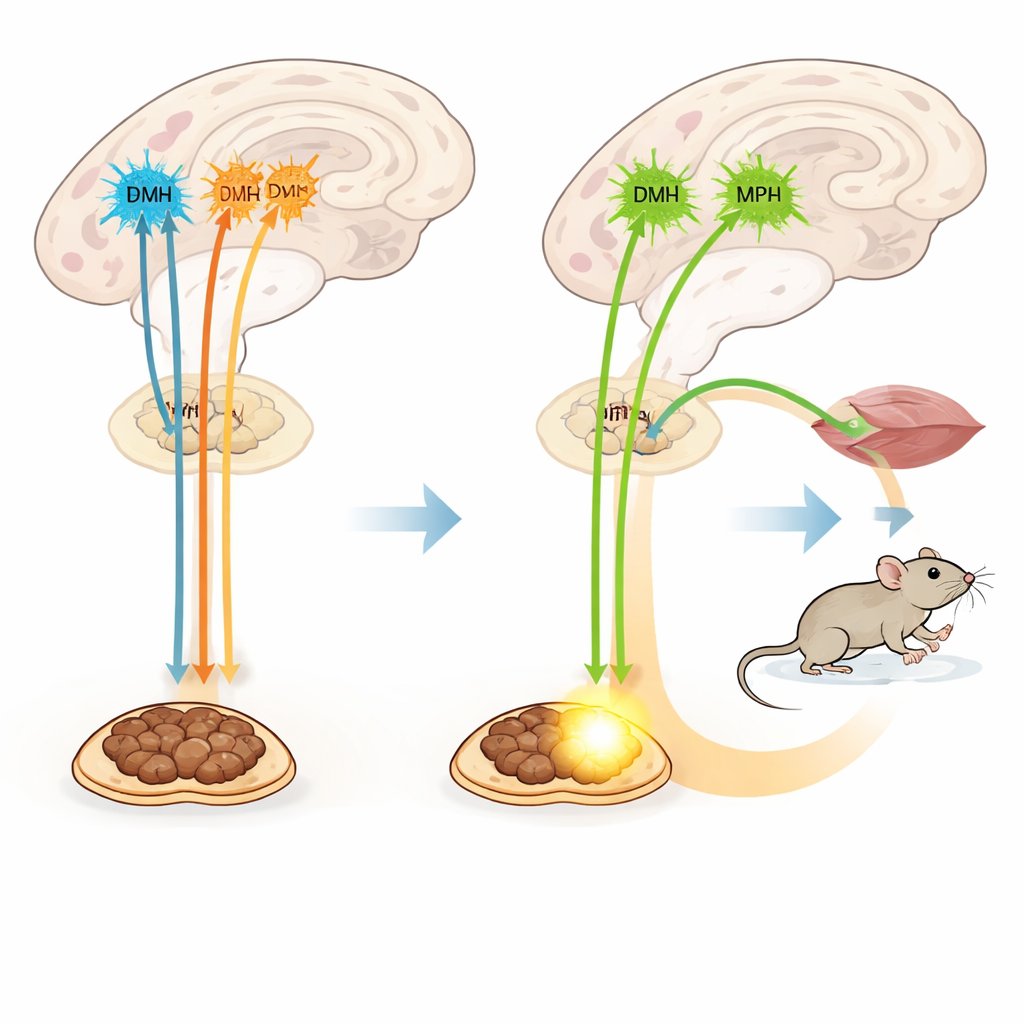
Vad detta betyder för människors hälsa
I enkla termer visar studien att flera små uppsättningar TRH‑frisättande hjärnceller samarbetar som specialiserade termostater och bränsleventiler. De i två hypotalamus‑hubbar driver direkt brunt fett att bränna kalorier som värme, medan de i en närliggande region ökar rörelse och hjälper kroppen att klara kyla. Alla tre hypotalamiska grupperna ökar också kortvarigt födointaget, sannolikt genom att excitera hungerrelaterade kretsar. Eftersom dessa effekter kan separeras från klassiska sköldkörtelhormoner kan riktade TRH‑vägar eller deras nervkopplingar en dag göra det möjligt för läkare att öka energiförbrukningen utan att utlösa de omfattande biverkningar som överdrivet sköldkörtelhormon ger.
Citering: Constantinescu, A., Chandrasekar, A., Kleindienst, L. et al. Thyrotropin-releasing hormone neurons of different hypothalamic nuclei increase energy expenditure. Nat Commun 17, 3499 (2026). https://doi.org/10.1038/s41467-026-71617-3
Nyckelord: termogenes i brunt fett, hypotalamus, thyrotropin‑frisättande hormon, energiförbrukning, kalltålighet