Clear Sky Science · it
Neuroni che rilasciano ormone di rilascio della tireotropina in diversi nuclei ipotalamici aumentano la spesa energetica
Perché contano le cellule cerebrali che bruciano calorie
La maggior parte delle persone pensa al metabolismo come a qualcosa controllato dagli ormoni prodotti da ghiandole come la tiroide. Questo studio scava più a fondo, in piccoli aggregati di neuroni che rilasciano un messaggero chiamato ormone di rilascio della tireotropina (TRH) nei topi. I ricercatori dimostrano che diversi gruppi di queste cellule funzionano come “hub energetici” separati, ciascuno modulando la quantità di calore prodotta dal corpo, il livello di attività e l’assunzione di cibo. Comprendere questi circuiti potrebbe indicare nuovi modi per combattere obesità e diabete spingendo il corpo a dissipare più calorie sotto forma di calore invece di immagazzinarle come grasso.
Hub cerebrali diversi, un obiettivo comune sul carburante
Il team si è concentrato su diverse regioni dell’ipotalamo, un centro di controllo chiave in profondità nel cervello, e su un’area del tronco encefalico. Hanno chiesto se i neuroni produttori di TRH in ciascuna regione contribuissero a regolare l’uso di energia del corpo. Usando virus come traccianti, hanno mappato le connessioni tra questi neuroni e il tessuto adiposo bruno, un tipo speciale di grasso che brucia energia per produrre calore. Hanno poi impiegato un interruttore chemiogenetico — un recettore ingegnerizzato attivato da un farmaco progettato innocuo — per attivare o disattivare gruppi selezionati di neuroni TRH nei topi vivi mentre misuravano la temperatura corporea, l’attività del grasso bruno, il movimento e l’assunzione di cibo.
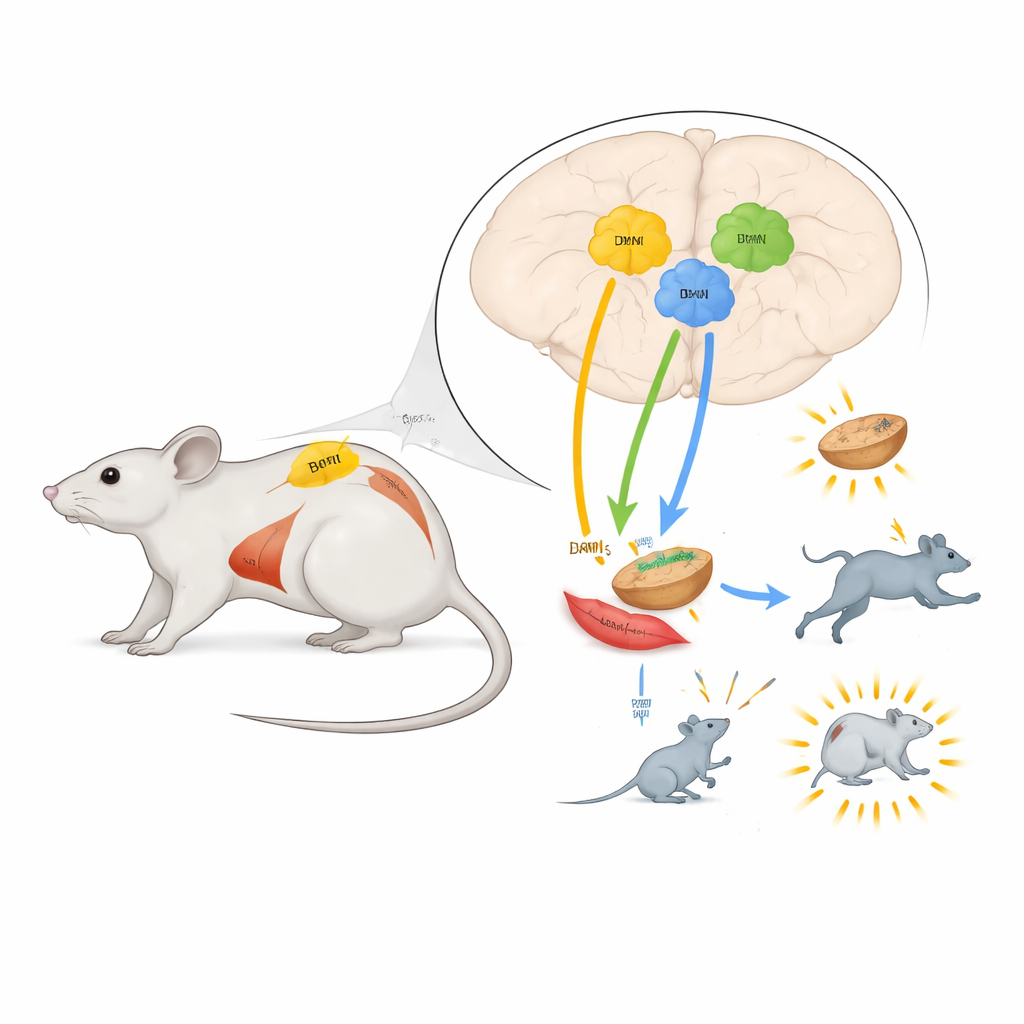
Accenditori del grasso bruno in due regioni chiave
Nel nucleo paraventricolare (PVN) e nell’ipotalamo dorsomediale (DMH), l’attivazione dei neuroni TRH ha aumentato nettamente quante calorie i topi bruciavano e ha innalzato la temperatura corporea centrale. L’imaging a infrarossi ha mostrato che le aree di grasso bruno tra le scapole si sono riscaldate e i test molecolari hanno confermato l’attivazione di enzimi coinvolti nella degradazione dei grassi all’interno del tessuto adiposo bruno. Il blocco di un tipo specifico di recettore adrenergico nelle cellule adipose ha impedito questo riscaldamento, indicando che questi neuroni cerebrali attivano il grasso bruno tramite i nervi simpatici, lo stesso sistema che prepara il corpo alla “lotta o fuga”. Questi cambiamenti nella spesa energetica e nella temperatura persistevano anche quando gli animali non potevano mangiare, dimostrando che non erano semplicemente un effetto collaterale di un aumento dell’assunzione di cibo.
Un hub del movimento che protegge dal freddo
Un quadro diverso è emerso nell’area preottica mediale (MPA), una regione nota da tempo per percepire la temperatura corporea. Accendere i neuroni TRH qui ha aumentato anch’esso la spesa energetica e la temperatura corporea, ma il grasso bruno è rimasto relativamente silenzioso. Al contrario, i topi sono diventati più attivi: si muovevano di più nelle loro gabbie, suggerendo che il lavoro muscolare e l’eccitazione generale fornivano gran parte del calore extra. Quando i ricercatori hanno silenziato cronicamente questi neuroni TRH dell’MPA ed esposto poi i topi a un improvviso abbassamento della temperatura ambiente, la temperatura corporea degli animali è scesa più ripidamente e non sono riusciti a aumentare la produzione di energia. Questo dimostra che i neuroni TRH dell’MPA sono essenziali per montare una risposta difensiva adeguata al freddo, probabilmente guidando il comportamento e l’attività muscolare piuttosto che attivando direttamente il grasso bruno.
Non tutte le cellule TRH modellano il metabolismo
Gli scienziati hanno anche esaminato i neuroni TRH in una regione del tronco encefalico chiamata nucleo del rafe pallido rostrale, sospettata in precedenza di contribuire al controllo del grasso bruno. Sorprendentemente, l’attivazione di queste cellule ha avuto poco effetto sulla spesa energetica, sul movimento, sulla temperatura del grasso bruno o sull’assunzione di cibo. Ciò suggerisce che il semplice fatto di essere connessi al grasso bruno non è sufficiente; solo alcuni circuiti positivi al TRH modificano effettivamente quanta energia il corpo spende.
Oltre gli ormoni tiroidei classici
Il TRH è meglio conosciuto per indurre il rilascio dell’ormone stimolante la tiroide e degli ormoni tiroidei, che aumentano il metabolismo in modo generale. Qui, solo i neuroni TRH del PVN hanno attivato questa catena ormonale. Eppure gli aumenti rapidi di calore nel grasso bruno e della spesa energetica guidati dai neuroni TRH del PVN e del DMH non dipendevano dal recettore TRH principale che controlla il rilascio degli ormoni tiroidei. Anche quando questo recettore è stato eliminato geneticamente, l’attivazione dei neuroni TRH del PVN ha comunque reso il grasso bruno più caldo e ha aumentato la temperatura corporea. Un farmaco simile al TRH, per contro, richiedeva quel recettore per incrementare la spesa energetica. Questa divisione mostra che lo stesso messaggero chimico sostiene almeno due sistemi: uno ormonale più lento a livello dell’intero organismo e uno nervoso più rapido instradato attraverso specifici gruppi di neuroni TRH.
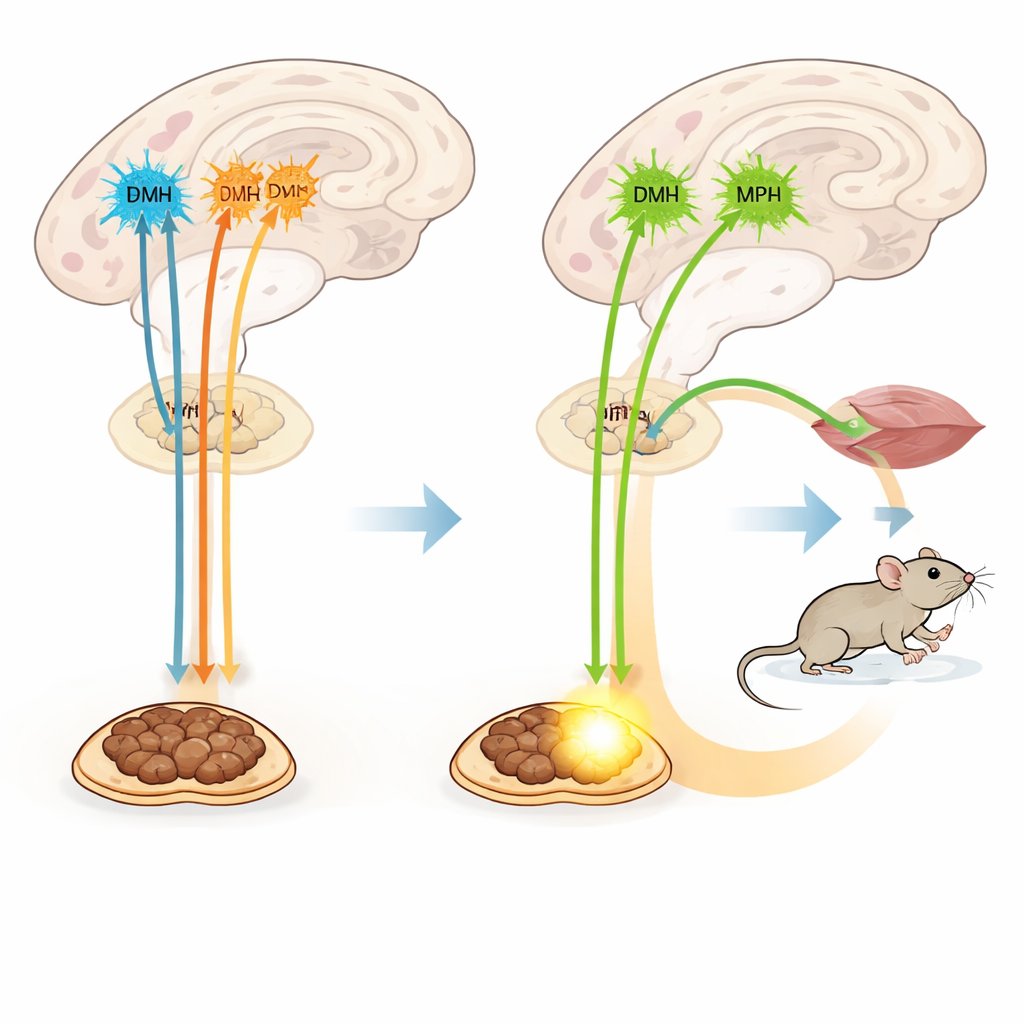
Cosa significa per la salute umana
In termini pratici, lo studio rivela che diversi piccoli gruppi di neuroni che rilasciano TRH lavorano insieme come termostati e valvole del carburante specializzati. Quelli in due hub ipotalamici spingono direttamente il grasso bruno a bruciare calorie come calore, mentre quelli in una regione vicina aumentano il movimento e aiutano il corpo a fronteggiare il freddo. Tutti e tre i gruppi ipotalamici aumentano anche temporaneamente l’assunzione di cibo, probabilmente eccitando circuiti legati alla fame. Poiché questi effetti possono essere separati dagli ormoni tiroidei classici, mirare ai giusti percorsi TRH o alle loro connessioni nervose potrebbe un giorno permettere ai medici di aumentare la spesa energetica senza scatenare gli effetti collaterali diffusi di un eccesso di ormoni tiroidei.
Citazione: Constantinescu, A., Chandrasekar, A., Kleindienst, L. et al. Thyrotropin-releasing hormone neurons of different hypothalamic nuclei increase energy expenditure. Nat Commun 17, 3499 (2026). https://doi.org/10.1038/s41467-026-71617-3
Parole chiave: termogenesi del grasso bruno, ipotalamo, ormone di rilascio della tireotropina, spesa energetica, tolleranza al freddo