Clear Sky Science · nl
Neuronen die thyreotropine‑afgevend hormoon produceren in verschillende hypothalamische kernen verhogen het energieverbruik
Waarom hersencellen die calorieën verbranden ertoe doen
De meeste mensen denken bij metabolisme aan hormonen uit klieren zoals de schildklier. Deze studie kijkt dieper, naar kleine clusters hersencellen die een boodschapper vrijgeven die thyreotropine‑afgevend hormoon (TRH) heet, onderzocht in muizen. De onderzoekers tonen aan dat verschillende groepen van deze cellen fungeren als afzonderlijke “energiehubs”, die elk bepalen hoeveel warmte het lichaam produceert, hoeveel het beweegt en hoeveel het eet. Inzicht in deze circuits kan wijzen op nieuwe manieren om obesitas en diabetes te bestrijden door het lichaam naar meer verbranding van calorieën als warmte te sturen in plaats van opslag als vet.
Verschillende hersenhubs, één gemeenschappelijk brandstofdoel
Het team richtte zich op meerdere regio’s in de hypothalamus, een belangrijk regelcentrum diep in de hersenen, en op een gebied in de hersenstam. Ze onderzochten of TRH‑producerende neuronen in elk gebied helpen het energiegebruik van het lichaam te beheersen. Met virussen als tracers brachten ze de verbindingen in kaart tussen deze neuronen en bruin vetweefsel, een speciaal vettype dat energie verbrandt om warmte te produceren. Vervolgens gebruikten ze een chemogenetische schakel—een ontworpen receptor die wordt geactiveerd door een onschadelijk designer‑geneesmiddel—om geselecteerde TRH‑neurongroepen aan of uit te zetten in levende muizen terwijl ze lichaamstemperatuur, bruine vetactiviteit, beweging en voedselinname maten.
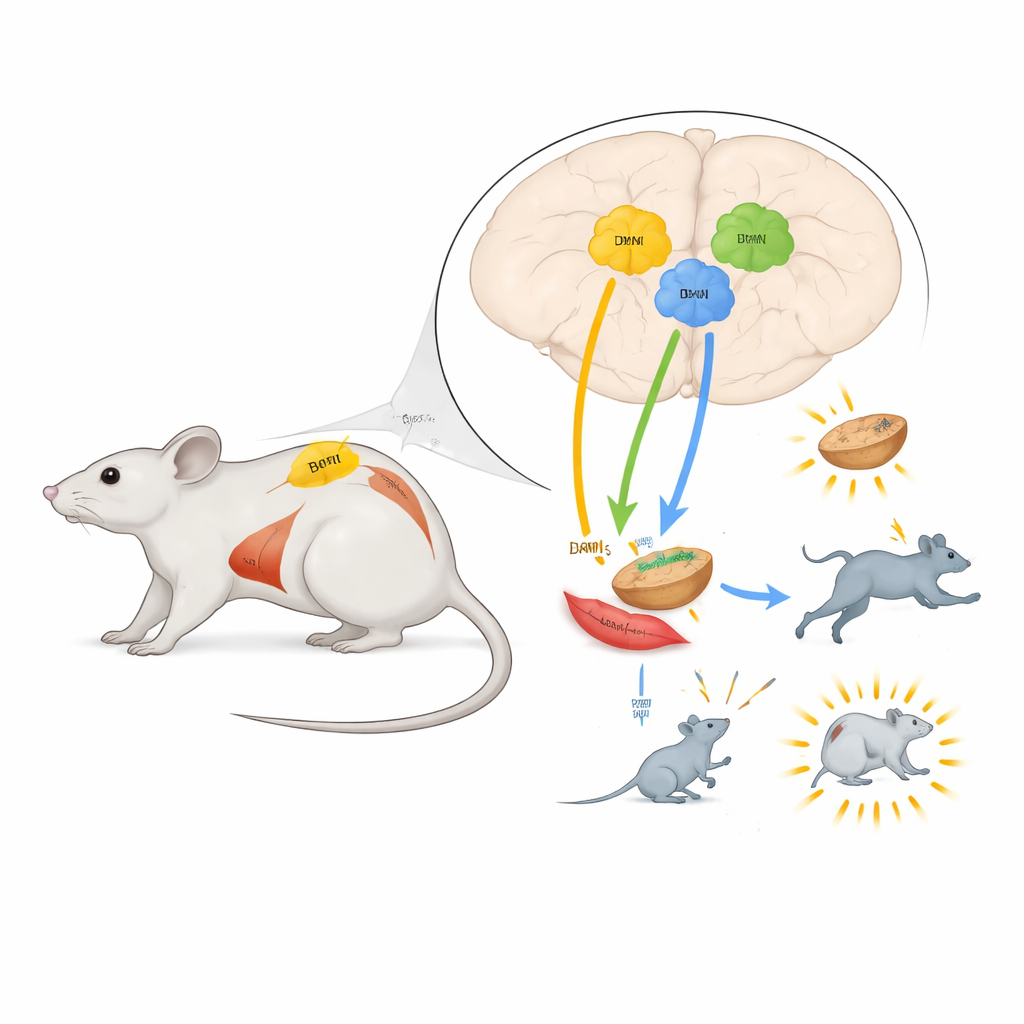
Bruine‑vetverbranders in twee belangrijke regio’s
In de paraventriculaire kern (PVN) en de dorsomediale hypothalamus (DMH) leidde activatie van TRH‑neuronen tot een sterke toename van het aantal verbrande calorieën en tot verhoging van de kerntemperatuur. Infraroodfoto’s toonden dat bruine‑vetvlekken tussen de schouderbladen opwarmden, en moleculaire tests bevestigden dat enzymen die betrokken zijn bij vetafbraak in bruin vet werden geactiveerd. Het blokkeren van een specifiek type adrenaline‑receptor in vetcellen verhinderde deze verhitting, wat aangeeft dat deze hersencellen bruin vet via sympathische zenuwen aansturen—hetzelfde systeem dat het lichaam voorbereidt op ‘‘vecht‑of‑vlucht’’. Deze veranderingen in energiegebruik en temperatuur hielden aan zelfs wanneer de dieren niet konden eten, wat laat zien dat het geen bijeffect was van toegenomen voedselinname.
Een bewegingshub die beschermt tegen de kou
Een ander beeld kwam naar voren in het mediale preoptische gebied (MPA), een regio die lang bekendstaat om het waarnemen van lichaamstemperatuur. Activatie van TRH‑neuronen hier verhoogde ook het energieverbruik en de lichaamstemperatuur, maar bruin vet bleef relatief rustig. In plaats daarvan werden de muizen actiever: ze bewogen meer in hun kooien, wat suggereert dat spierarbeid en algemene opwinding een groot deel van de extra warmte leverden. Toen de onderzoekers deze MPA‑TRH‑neuronen chronisch uitschakelden en de muizen vervolgens blootstelden aan een plotselinge daling van de kamertemperatuur, daalde de lichaamstemperatuur van de dieren sterker en slaagden ze er niet in hun energieverbruik te verhogen. Dit toont aan dat MPA‑TRH‑neuronen essentieel zijn voor een juiste koudeverdedigingsreactie, waarschijnlijk door gedrag en spieractiviteit aan te sturen in plaats van direct bruin vet te activeren.
Niet alle TRH‑cellen vormen het metabolisme
De wetenschappers onderzochten ook TRH‑neuronen in een hersenstamgebied dat de rostrale raphe pallidus wordt genoemd, waarvan gedacht werd dat het bruin vet zou helpen reguleren. Verrassend genoeg had activatie van deze cellen weinig effect op energieverbruik, beweging, temperatuur van bruin vet of eten. Dit suggereert dat alleen omdat een neuron verbonden is met bruin vet, dat nog niet betekent dat het daadwerkelijk het energieverbruik wijzigt; slechts sommige TRH‑positieve circuits doen dat daadwerkelijk.
Voorbij klassieke schildklierhormonen
TRH is vooral bekend vanwege het stimuleren van de afgifte van schildklierstimulerend hormoon en schildklierhormonen, die het metabolisme in brede zin verhogen. Hier activeerden alleen de PVN‑TRH‑neuronen deze hormoonketen. Toch waren de snelle toename in bruinvetwarmte en het energieverbruik veroorzaakt door PVN‑ en DMH‑TRH‑neuronen niet afhankelijk van de belangrijkste TRH‑receptor die de afgifte van schildklierhormoon reguleert. Zelfs wanneer deze receptor genetisch werd verwijderd, maakten het activeren van PVN‑TRH‑neuronen het bruin vet nog steeds heter en steeg de lichaamstemperatuur. Een TRH‑achtig medicijn daarentegen vereiste die receptor om het energieverbruik te verhogen. Deze scheiding toont aan dat dezelfde chemische boodschapper ten minste twee systemen ondersteunt: een langzamer, lichaam‑wijd hormonaal systeem en een sneller, zenuwgebonden systeem dat via specifieke TRH‑neurongroepen loopt.
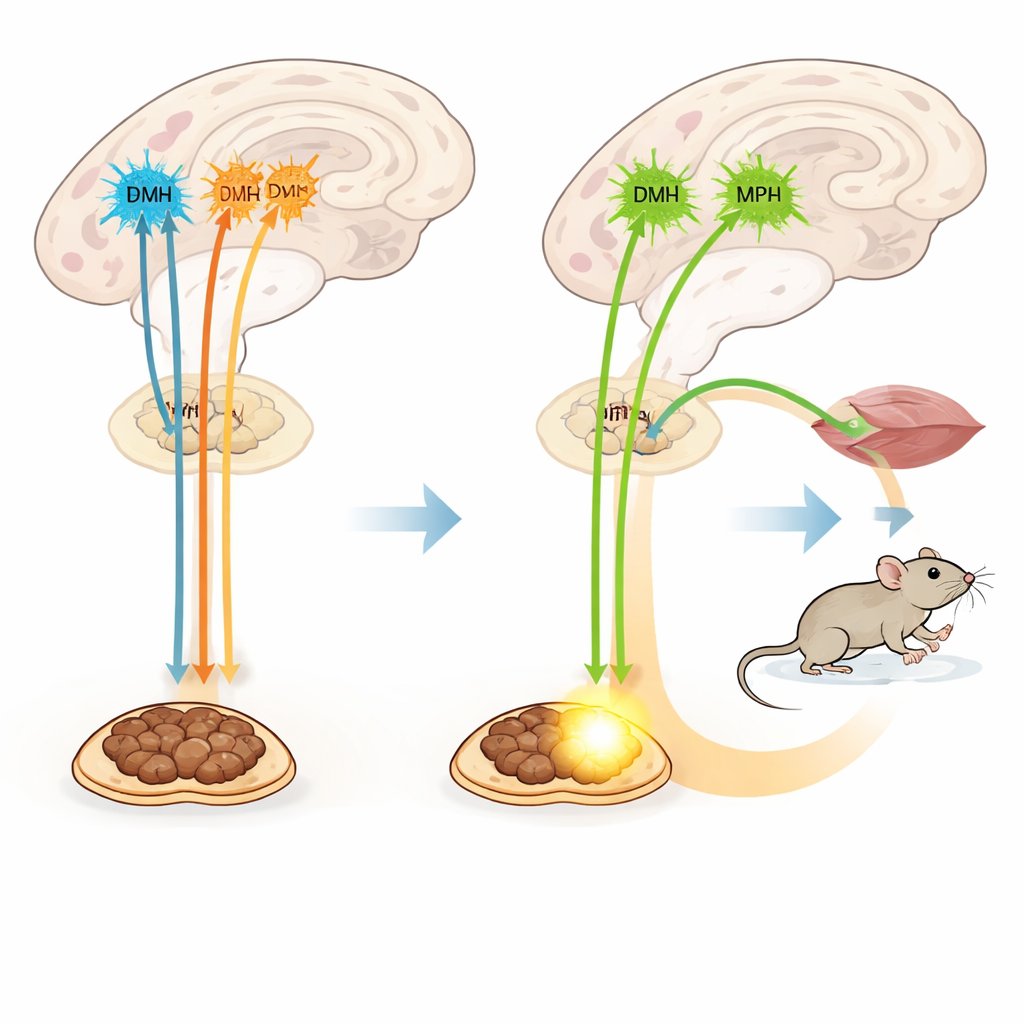
Wat dit betekent voor de menselijke gezondheid
In praktische termen onthult de studie dat meerdere kleine sets TRH‑afgevende hersencellen samenwerken als gespecialiseerde thermostaten en brandstofkleppen. Die in twee hypothalamische hubs zetten bruin vet rechtstreeks aan om calorieën als warmte te verbranden, terwijl die in een naburig gebied beweging stimuleren en het lichaam helpen omgaan met kou. Alle drie hypothalamische groepen verhogen ook kortdurend de voedselinname, waarschijnlijk door hongergerelateerde circuits te prikkelen. Omdat deze effecten te scheiden zijn van klassieke schildklierhormonen, zou gerichte aansturing van de juiste TRH‑routes of hun zenuwverbindingen artsen in de toekomst mogelijk in staat kunnen stellen het energieverbruik op te voeren zonder de verregaande bijwerkingen van overtollig schildklierhormoon te veroorzaken.
Bronvermelding: Constantinescu, A., Chandrasekar, A., Kleindienst, L. et al. Thyrotropin-releasing hormone neurons of different hypothalamic nuclei increase energy expenditure. Nat Commun 17, 3499 (2026). https://doi.org/10.1038/s41467-026-71617-3
Trefwoorden: thermogenese in bruin vet, hypothalamus, thyreotropine‑afgevend hormoon, energieverbruik, koudetolerantie