Clear Sky Science · fr
Les neurones à hormone de libération de la thyréostimuline de différents noyaux hypothalamiques augmentent la dépense énergétique
Pourquoi les cellules cérébrales qui brûlent des calories comptent
La plupart des gens considèrent le métabolisme comme quelque chose contrôlé par des hormones sécrétées par des glandes comme la thyroïde. Cette étude creuse plus profondément, dans de petits groupes de neurones qui libèrent un messager nommé hormone de libération de la thyréostimuline (TRH) chez la souris. Les chercheurs montrent que différents groupes de ces cellules fonctionnent comme des « plateformes énergétiques » distinctes, chacune réglant la production de chaleur corporelle, l’activité motrice et l’alimentation. Comprendre ces circuits pourrait indiquer de nouvelles voies pour lutter contre l’obésité et le diabète en incitant le corps à gaspiller davantage de calories sous forme de chaleur plutôt que de les stocker sous forme de graisse.
Différents centres cérébraux, un même objectif énergétique
L’équipe s’est concentrée sur plusieurs régions de l’hypothalamus, un centre de commande clé en profondeur du cerveau, ainsi que sur une zone du tronc cérébral. Ils ont cherché à savoir si les neurones producteurs de TRH dans chaque région contribuent à contrôler l’utilisation d’énergie de l’organisme. En utilisant des virus comme traceurs, ils ont cartographié les connexions entre ces neurones et le tissu adipeux brun, un type particulier de graisse qui brûle de l’énergie pour produire de la chaleur. Ils ont ensuite employé un interrupteur chimogénétique — un récepteur ingénieré activé par un médicament conçu inoffensif — pour activer ou désactiver des groupes sélectionnés de neurones TRH chez des souris vivantes tout en mesurant la température corporelle, l’activité du tissu adipeux brun, le mouvement et la prise alimentaire.
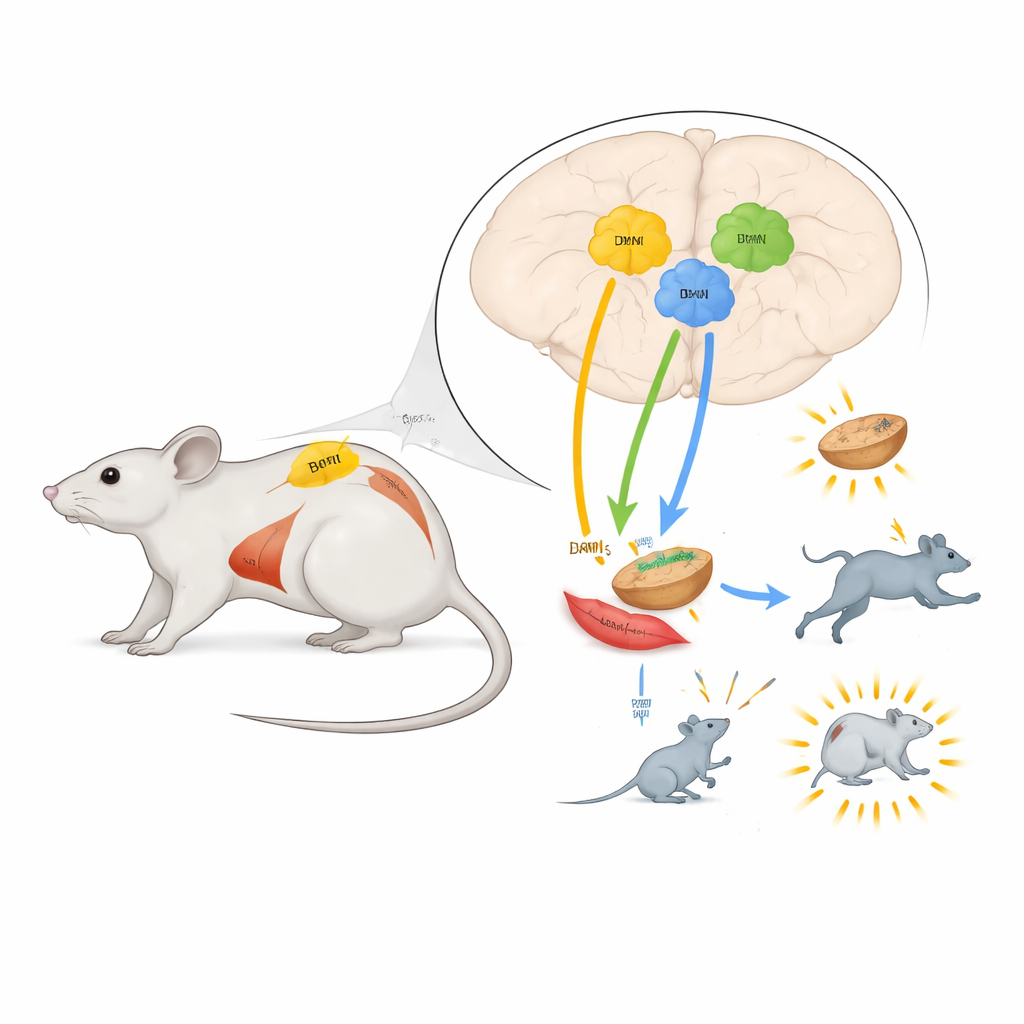
Des brûleurs de graisse brune dans deux régions clés
Dans le noyau paraventriculaire (PVN) et l’hypothalamus dorsomédial (DMH), l’activation des neurones TRH a fortement augmenté la dépense calorique des souris et élevé leur température corporelle centrale. L’imagerie infrarouge a montré que les plages de tissu adipeux brun entre les omoplates se sont réchauffées, et des tests moléculaires ont confirmé que des enzymes impliquées dans la dégradation des lipides au sein du tissu adipeux brun étaient activées. Le blocage d’un type spécifique de récepteur à l’adrénaline dans les cellules adipeuses a empêché ce réchauffement, indiquant que ces neurones agissent sur la graisse brune via les nerfs sympathiques, le même système qui prépare l’organisme à la « fuite ou au combat ». Ces changements de consommation d’énergie et de température ont persisté même lorsque les animaux étaient privés de nourriture, montrant qu’ils n’étaient pas simplement une conséquence d’une augmentation de la prise alimentaire.
Un centre moteur qui protège du froid
Un tableau différent est apparu dans la zone préoptique médiale (MPA), une région connue depuis longtemps pour détecter la température corporelle. L’activation des neurones TRH ici a également augmenté la dépense énergétique et la température corporelle, mais le tissu adipeux brun est resté relativement silencieux. À la place, les souris sont devenues plus actives : elles ont plus bougé dans leurs cages, suggérant que le travail musculaire et l’éveil général fournissaient une grande partie de la chaleur supplémentaire. Lorsque les chercheurs ont silencé de façon chronique ces neurones TRH de la MPA puis exposé les souris à une chute soudaine de la température ambiante, la température corporelle des animaux a chuté plus rapidement et ils n’ont pas réussi à augmenter leur production d’énergie. Cela montre que les neurones TRH de la MPA sont essentiels pour déclencher une réponse de défense contre le froid, probablement en stimulant le comportement et l’activité musculaire plutôt qu’en activant directement la graisse brune.
Tous les neurones TRH n’influencent pas le métabolisme
Les scientifiques ont aussi examiné les neurones TRH d’une région du tronc cérébral appelée le raphé pallidus rostral, qui était soupçonnée de participer au contrôle de la graisse brune. De manière surprenante, l’activation de ces cellules a eu peu d’effet sur la dépense énergétique, le mouvement, la température de la graisse brune ou l’alimentation. Cela suggère que le simple fait d’être connecté à la graisse brune ne suffit pas ; seuls certains circuits positifs pour la TRH modulent réellement la dépense énergétique de l’organisme.
Au-delà des hormones thyroïdiennes classiques
La TRH est surtout connue pour déclencher la libération de l’hormone stimulant la thyroïde et des hormones thyroïdiennes, qui augmentent globalement le métabolisme. Ici, seuls les neurones TRH du PVN ont activé cette voie hormonale. Pourtant, les accroissements rapides de chaleur du tissu adipeux brun et de la dépense énergétique induits par les neurones TRH du PVN et du DMH ne dépendaient pas du récepteur principal de la TRH qui contrôle la libération des hormones thyroïdiennes. Même lorsque ce récepteur était supprimé génétiquement, l’activation des neurones TRH du PVN réchauffait toujours la graisse brune et augmentait la température corporelle. En revanche, un médicament de type TRH nécessitait ce récepteur pour augmenter la dépense énergétique. Cette dissociation montre que le même messager chimique soutient au moins deux systèmes : l’un hormonal, plus lent et à l’échelle du corps entier, et un autre plus rapide, basé sur les nerfs et routé par des groupes neuronaux TRH spécifiques.
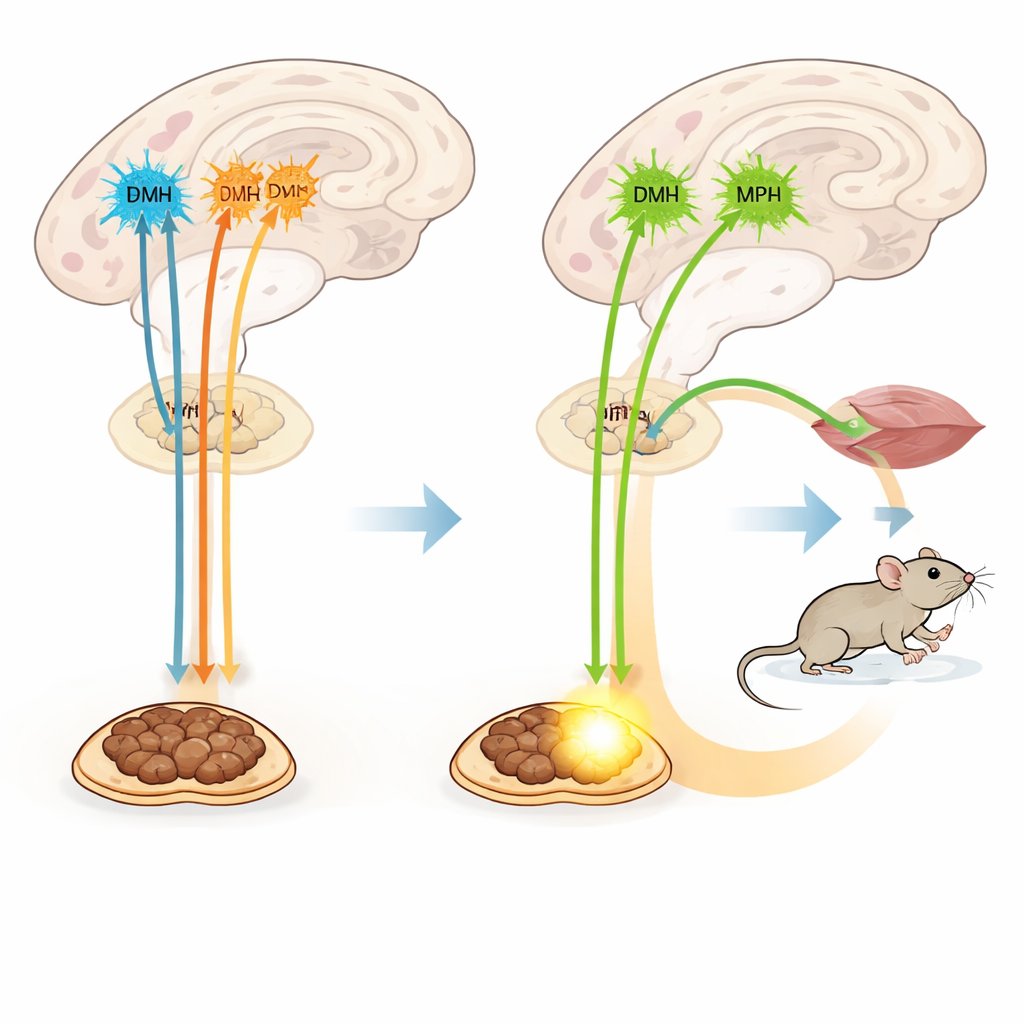
Ce que cela signifie pour la santé humaine
Concrètement, l’étude révèle que plusieurs petits ensembles de neurones libérant de la TRH fonctionnent ensemble comme des thermostats et des régulateurs de carburant spécialisés. Ceux de deux noyaux hypothalamiques poussent directement la graisse brune à brûler des calories sous forme de chaleur, tandis que ceux d’une région voisine augmentent le mouvement et aident l’organisme à faire face au froid. Les trois groupes hypothalamiques augmentent aussi brièvement l’alimentation, probablement en excitant des circuits liés à la faim. Parce que ces effets peuvent être dissociés des hormones thyroïdiennes classiques, cibler les voies TRH appropriées ou leurs connexions nerveuses pourrait un jour permettre aux médecins d’augmenter la dépense énergétique sans déclencher les effets secondaires étendus d’un excès d’hormones thyroïdiennes.
Citation: Constantinescu, A., Chandrasekar, A., Kleindienst, L. et al. Thyrotropin-releasing hormone neurons of different hypothalamic nuclei increase energy expenditure. Nat Commun 17, 3499 (2026). https://doi.org/10.1038/s41467-026-71617-3
Mots-clés: thermogenèse du tissu adipeux brun, hypothalamus, hormone de libération de la thyréostimuline, dépense énergétique, tolérance au froid