Clear Sky Science · sv
Kryo-EM-struktur av Chlamydomonas reinhardtii Photosystem I i komplex med cytokrom c6
Hur gröna alger håller solljuset i rörelse
Varje grönt blad och algcell är beroende av ett osynligt stafettlopp av elektroner som omvandlar solljus till användbar energi. Denna studie granskar en liten överlämning i det loppet: hur ett litet bärarprotein kallat cytokrom c6 levererar elektroner till en jättelik ljusfångande maskin känd som Fotosystem I i gröna alger. Genom att frysa dessa molekyler i aktion och avbilda dem med nästan atomär upplösning visar författarna hur detta avgörande möte går till och hur det knyter an till fotosyntesens evolutionära historia.
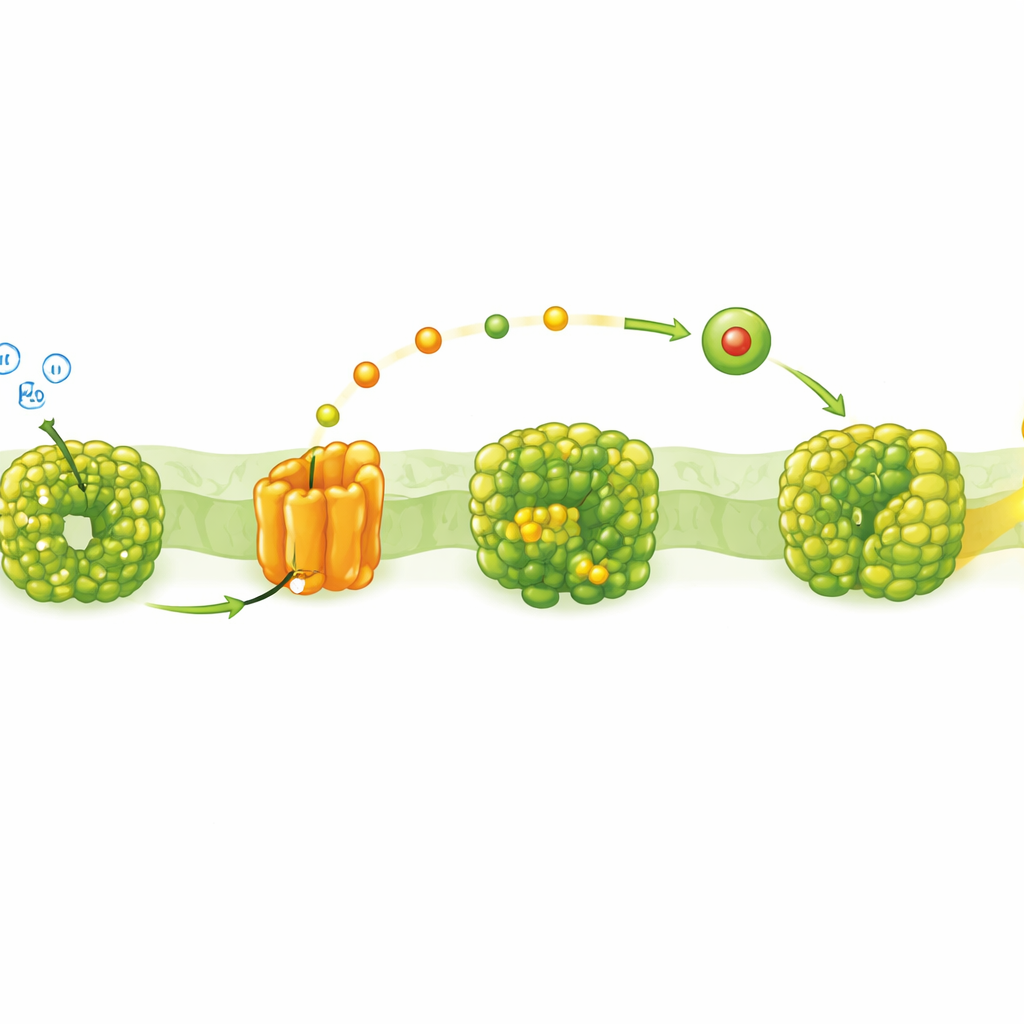
En noggrann kedja av energisteg
I den syreproducerande fotosyntesen flödar energi genom en kedja av stora proteinkomplex inbäddade i inre membran. Fotosystem II använder ljus för att spjälka vatten och föra elektroner till en mellanstation kallad cytokrom b6f-komplexet. Därifrån transporterar små lösliga bärare—antingen kopparbaserade plastocyanin eller järnbaserade cytokrom c6—elektroner genom den vattniga insidan till Fotosystem I. När Fotosystem I tar emot dessa elektroner bidrar det till att generera de elektriska och kemiska gradienter som slutligen driver cellens produktion av ATP, den universella energivalutan.
En uråldrig partner möter en modern maskin
Ur ett evolutionärt perspektiv tror man att de tidigaste versionerna av Fotosystem I främst arbetade med cytokrom c6. Med tiden bytte många organismer, särskilt växter, till att använda plastocyanin istället, delvis därför att det använder koppar i stället för järn, vilket kan vara knappare. Gröna alger som Chlamydomonas reinhardtii befinner sig mitt i denna berättelse: de kan använda båda bärare och ändra preferens beroende på metalltillgång. Att förstå exakt hur cytokrom c6 fäster vid Fotosystem I i dessa alger ger en inblick i hur urgamla och moderna strategier för elektronleverans samexisterar och hur de kan ha utvecklats.
Frysa kontaktögonblicket
Forskarnas skapade stabila komplex mellan cytokrom c6 och Fotosystem I genom att använda ett kortdistans kemiskt tvärbindemedel som binder de två partnerna bara när de naturligt är nära varandra. De använde sedan högupplöst kryo-elektronmikroskopi för att rekonstruera den tredimensionella strukturen av detta frusna möte med ungefär två ångströms detalj, tillräckligt fint för att placera individuella aminosyra-sidokedjor, pigmentmolekyler och till och med många vattenmolekyler. Strukturen visar cytokrom c6 inbäddad i en grund ficka som bildas där två kärnsubenheter i Fotosystem I möts, med en extra ythelix från en annan subenhet (PsaF) som når över som en liten arm för att hjälpa hålla den på plats.
En exakt passform för snabb elektronflöde
I denna ficka sitter cytokrom c6:s hemgrupp—delen som faktiskt bär elektronen—bara cirka elva ångström från det speciella klorofyllparet i Fotosystem I som tar emot elektronen. Gränssnittet stöds av ett tätt nätverk av interaktioner: negativt laddade ytor på cytokrom c6 attraherar positivt laddade regioner på PsaF, medan neutrala och aromatiska sidokedjor skapar täta, oljeliknande kontakter längre ner i fåra. En viss arginin på cytokrom c6 (R66), länge känd som viktig i bakterier, staplas med närliggande ringar både på cytokrom c6 och Fotosystem I och bildar en tredubbelslagerinteraktion som verkar hjälpa till att stabilisera dokningspositionen. Denna täta packning tränger också undan vatten från den direkta vägen mellan hem och klorofyll, vilket sannolikt minskar motståndet mot elektronflöde och förklarar varför elektronöverföringen sker på bara några miljoner delar av en sekund.
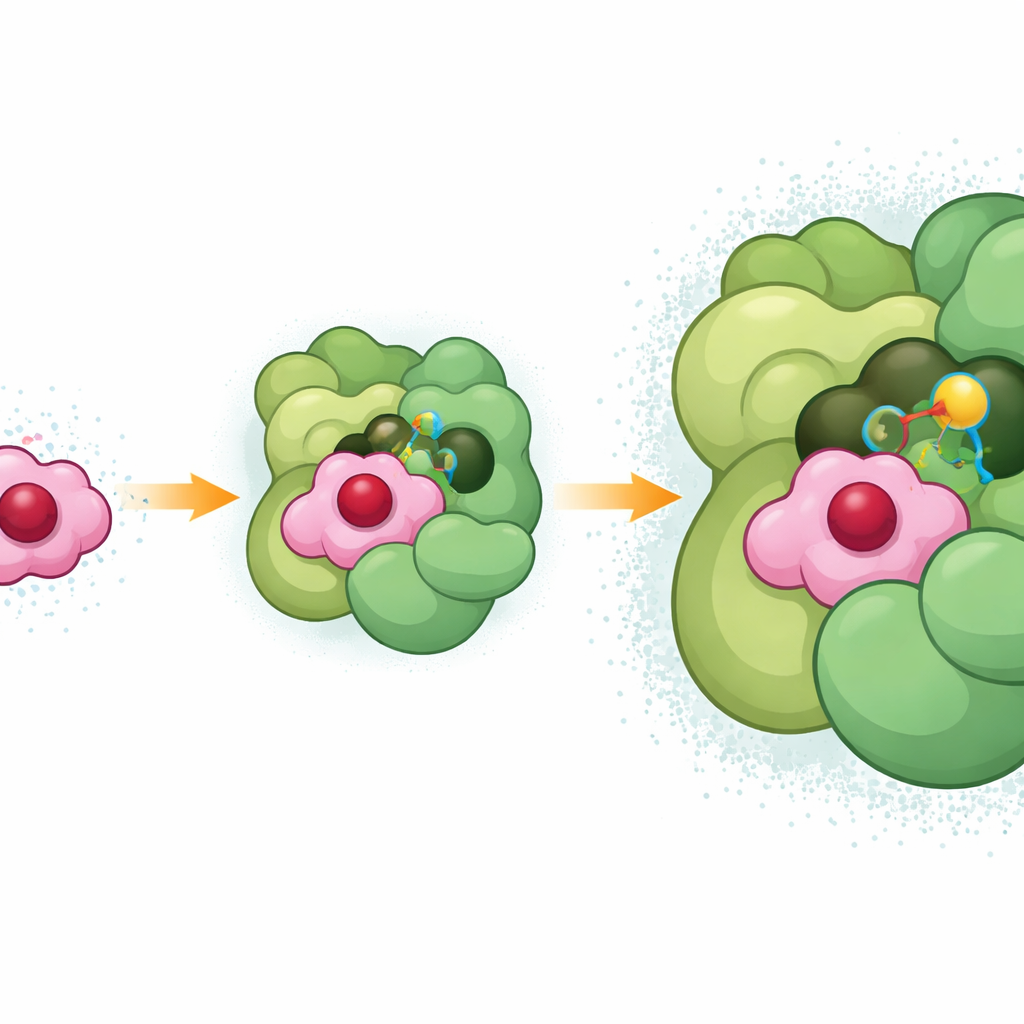
Testa de kritiska kontaktpunkterna
För att se vilka delar av cytokrom c6 som betyder mest introducerade teamet riktade förändringar i sura och basiska rester som förutsågs komma i kontakt med Fotosystem I. När de neutraliserade vissa negativa laddningar nära PsaF-”armen” eller ersatte den nyckelarginin, saktade omreduceringshastigheten av Fotosystem I avsevärt, och tvärbindningen mellan de två proteinerna försvagades. Vissa kombinationer av förändringar gav oväntat beteende, vilket antyder att cytokrom c6 och Fotosystem I ibland kan montera i alternativa, mindre effektiva arrangemang. Tillsammans bekräftar dessa tester att både PsaF-baserat elektrostatisk grepp och arginincentrerad stapling är avgörande för snabb och pålitlig elektronleverans.
Vad detta betyder för livets solmaskiner
Arbetet ger en detaljerad strukturell ritning för hur cytokrom c6 lämnar över elektroner till Fotosystem I i gröna alger och blandar egenskaper som ses i bakterier med dem hos mer utvecklade växter. Det visar hur ett litet bärarprotein och ett stort membrankomplex samevolverat ett fint avvägt gränssnitt som balanserar stark bindning, snabb elektronöverföring och snabb frigöring för nästa cykel. Genom att klargöra detta urgamla steg i fotosyntesens stafett hjälper studien att förklara hur organismer optimerat ljusdriven energiomvandling över evolutionär tid och ger designidéer för framtida försök att konstruera eller efterlikna naturens solenergiformer.
Citering: Ogawa, Y., Mahapatra, G.P., Milrad, Y. et al. Cryo-EM structure of Chlamydomonas reinhardtii Photosystem I complexed with cytochrome c6. Nat Commun 17, 3031 (2026). https://doi.org/10.1038/s41467-026-70944-9
Nyckelord: fotosyntes, Fotosystem I, cytokrom c6, elektronöverföring, kryo-EM