Clear Sky Science · pt
Estrutura por crio-ME do Fotossistema I de Chlamydomonas reinhardtii em complexo com citocromo c6
Como as algas verdes mantêm o fluxo da luz solar
Cada folha verde e célula de alga depende de uma corrida de revezamento invisível de elétrons para transformar a luz do sol em energia utilizável. Este estudo examina uma pequena passagem dessa corrida: como uma proteína transportadora diminuta chamada citocromo c6 entrega elétrons a uma gigantesca máquina coletora de luz conhecida como Fotossistema I em algas verdes. Ao congelar essas moléculas em ação e imagina-las em detalhe quase atômico, os autores revelam como esse encontro crucial funciona e como ele se conecta à história evolutiva da fotossíntese.
Uma cadeia cuidadosa de etapas energéticas
Na fotossíntese que produz oxigênio, a energia flui através de uma cadeia de grandes complexos proteicos enterrados em membranas internas. O Fotossistema II usa a luz para dividir a água e passar elétrons para uma estação intermediária chamada complexo citocromo b6f. A partir daí, pequenos transportadores solúveis—ou plastocianina à base de cobre ou citocromo c6 à base de ferro—transportam elétrons pelo interior aquoso até o Fotossistema I. Quando o Fotossistema I recebe esses elétrons, ele ajuda a gerar os gradientes elétricos e químicos que, em última instância, alimentam a produção de ATP pela célula, a moeda universal de energia.
Um parceiro antigo encontra uma máquina moderna
Do ponto de vista evolutivo, acredita-se que as primeiras versões do Fotossistema I funcionavam principalmente com citocromo c6. Com o tempo, muitos organismos, especialmente plantas, mudaram para usar plastocianina, em parte porque ela usa cobre em vez de ferro, que pode ser escasso. Algas verdes como Chlamydomonas reinhardtii situam-se no meio dessa história: elas podem usar ambos os transportadores, alterando a preferência conforme a disponibilidade de metais. Entender exatamente como o citocromo c6 se liga ao Fotossistema I nessas algas oferece uma janela sobre como estratégias antigas e modernas de entrega de elétrons coexistem e como podem ter evoluído.
Congelando o momento do contato
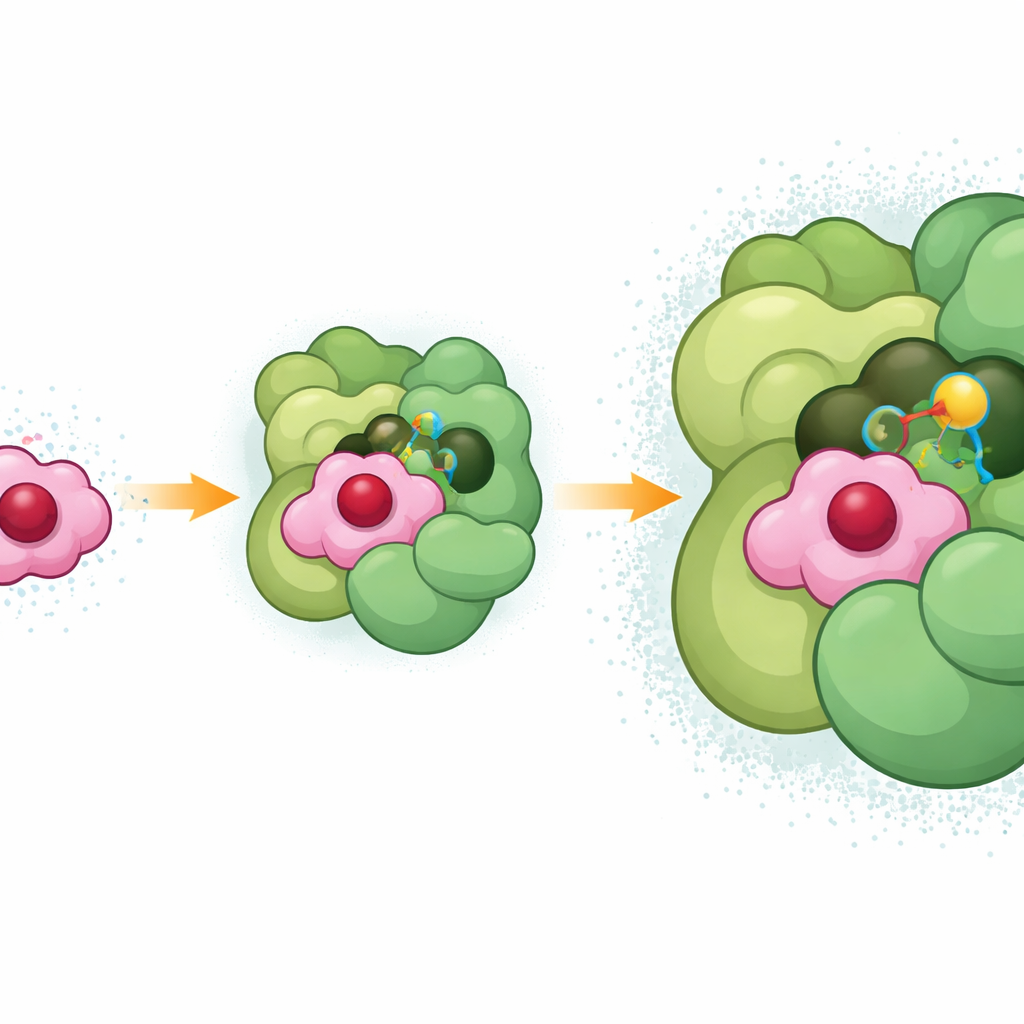
Os pesquisadores criaram complexos estáveis entre citocromo c6 e Fotossistema I usando uma reação química de reticulação de curto alcance que liga os dois parceiros somente quando estão naturalmente próximos. Em seguida, usaram crio-microscopia eletrônica de alta resolução para reconstruir a estrutura tridimensional desse encontro congelado com cerca de dois ângstrons de detalhe, fino o suficiente para posicionar cadeias laterais de aminoácidos individuais, moléculas pigmentares e até muitas moléculas de água. A estrutura mostra o citocromo c6 alojado em um bolso raso formado onde dois subunidades centrais do Fotossistema I se encontram, com uma hélice de superfície extra de outra subunidade (PsaF) estendendo-se como um pequeno braço para ajudar a mantê-lo no lugar.
Um encaixe preciso para fluxo rápido de elétrons
Dentro desse bolso, o grupo heme do citocromo c6—a parte que realmente carrega o elétron—senta-se a apenas cerca de onze ângstrons do par especial de clorofilas no Fotossistema I que recebe o elétron. A interface é sustentada por uma densa teia de interações: pontos carregados negativamente no citocromo c6 atraem regiões carregadas positivamente em PsaF, enquanto cadeias laterais neutras e aromáticas fazem contatos justos, semelhantes a interações oleosas, mais profundamente na ranhura. Uma arginina particular no citocromo c6 (R66), conhecida há muito tempo por ser vital em bactérias, empilha-se com anéis vizinhos tanto no citocromo c6 quanto no Fotossistema I, formando uma interação em três camadas que parece ajudar a estabilizar a posição de ancoragem. Esse empacotamento apertado também afasta a água do caminho direto entre o heme e a clorofila, provavelmente reduzindo a resistência ao fluxo de elétrons e explicando por que a transferência de elétrons ocorre em apenas alguns milionésimos de segundo.
Testando os pontos de contato críticos
Para ver quais partes do citocromo c6 mais importam, a equipe introduziu mudanças direcionadas em resíduos ácidos e básicos previstos para contatar o Fotossistema I. Quando neutralizaram certas cargas negativas perto do “braço” PsaF ou substituíram a arginina chave, a taxa na qual o Fotossistema I era reerduzido diminuiu marcadamente, e a reticulação entre as duas proteínas enfraqueceu. Algumas combinações de alterações produziram comportamentos inesperados, sugerindo que o citocromo c6 e o Fotossistema I às vezes podem se montar em arranjos alternativos e menos eficientes. Em conjunto, esses testes confirmam que tanto a fixação eletrostática baseada em PsaF quanto o empilhamento centrado na arginina são cruciais para a entrega de elétrons rápida e confiável.
O que isso significa para as máquinas solares da vida
O trabalho fornece um roteiro estrutural detalhado de como o citocromo c6 passa elétrons ao Fotossistema I em algas verdes, misturando características vistas em bactérias com as de plantas mais avançadas. Mostra como uma proteína transportadora pequena e um grande complexo de membrana coevoluíram uma interface finamente ajustada que equilibra uma forte ligação, transferência rápida de elétrons e liberação rápida para o próximo ciclo. Ao esclarecer esse passo antigo no revezamento fotossintético, o estudo ajuda a explicar como os organismos otimizaram a conversão de energia movida pela luz ao longo do tempo evolutivo e oferece pistas de projeto para esforços futuros de engenharia ou imitação dos sistemas solares da natureza.
Citação: Ogawa, Y., Mahapatra, G.P., Milrad, Y. et al. Cryo-EM structure of Chlamydomonas reinhardtii Photosystem I complexed with cytochrome c6. Nat Commun 17, 3031 (2026). https://doi.org/10.1038/s41467-026-70944-9
Palavras-chave: fotossíntese, Fotossistema I, citocromo c6, transferência de elétrons, crio-ME