Clear Sky Science · pl
Struktura Cryo-EM kompleksu Fotosystemu I z Chlamydomonas reinhardtii w kompleksie z cytochromem c6
Jak zielone algi utrzymują przepływ światła
Każdy zielony liść i komórka algi polegają na niewidocznym wyścigu przekaźników elektronów, który przekształca światło słoneczne w użyteczną energię. W tym badaniu przyglądamy się jednemu, drobnemu przekazaniu w tym wyścigu: jak mały białkowy nośnik zwany cytochromem c6 dostarcza elektrony do olbrzymiej maszyny zbierającej światło znanej jako Fotosystem I w zielonych algach. Zamrażając te cząsteczki w działaniu i obrazując je z niemal atomową dokładnością, autorzy ujawniają, jak przebiega to kluczowe spotkanie i jak łączy się ono z ewolucyjną historią fotosyntezy.
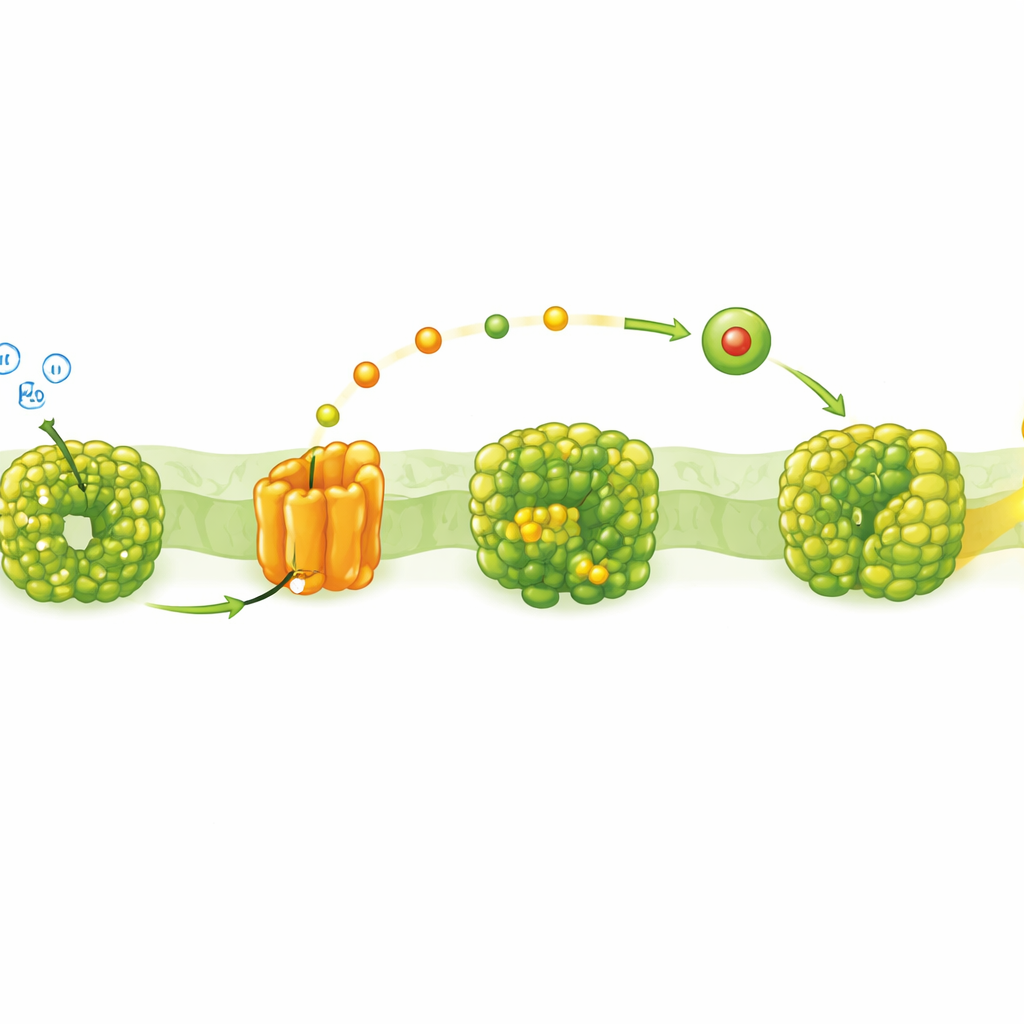
Staranna sekwencja etapów energetycznych
W fotosyntezie produkującej tlen energia przepływa przez łańcuch dużych kompleksów białkowych osadzonych w błonach wewnętrznych. Fotosystem II wykorzystuje światło do rozszczepienia wody i przekazania elektronów do pośredniej stacji zwanej kompleksem cytochromu b6f. Stamtąd małe rozpuszczalne nośniki — albo miedziowy plastocyjanin, albo zawierający żelazo cytochrom c6 — przemieszczają elektrony przez wodne wnętrze do Fotosystemu I. Gdy Fotosystem I otrzymuje te elektrony, pomaga wytworzyć gradienty elektryczne i chemiczne, które ostatecznie napędzają produkcję ATP w komórce, uniwersalnej waluty energetycznej.
Starożytny partner spotyka nowoczesną maszynę
Z ewolucyjnego punktu widzenia uważa się, że najwcześniejsze wersje Fotosystemu I współpracowały głównie z cytochromem c6. Z czasem wiele organizmów, zwłaszcza rośliny, przeszło na użycie plastocyjaniny — częściowo dlatego, że wykorzystuje ona miedź zamiast żelaza, które może być rzadkie. Zielone algi, takie jak Chlamydomonas reinhardtii, znajdują się pośrodku tej historii: potrafią korzystać z obu nośników, zmieniając preferencje w zależności od dostępności metali. Zrozumienie dokładnie, jak cytochrom c6 przyłącza się do Fotosystemu I w tych algach, daje wgląd w to, jak starożytne i nowoczesne strategie dostarczania elektronów współistnieją i jak mogły ewoluować.
Zamrażając moment kontaktu
Naukowcy stworzyli stabilne kompleksy między cytochromem c6 a Fotosystemem I, stosując krótkodystansowe chemiczne sieciowanie, które wiąże obie cząsteczki tylko gdy znajdują się one naturalnie blisko siebie. Następnie użyli wysokorozdzielczej krioelektronowej mikroskopii, aby zrekonstruować trójwymiarową strukturę tego zamrożonego spotkania z rozdzielczością około dwóch angstremów — na tyle szczegółową, by umieścić poszczególne łańcuchy boczne aminokwasów, cząsteczki pigmentów, a nawet wiele cząsteczek wody. Struktura pokazuje cytochrom c6 wciśnięty w płytkie zagłębienie utworzone tam, gdzie spotykają się dwie podjednostki rdzeniowe Fotosystemu I, z dodatkową powierzchniową helisą innej podjednostki (PsaF) sięgającą nad nią jak małe ramię, pomagające utrzymać go na miejscu.
Precyzyjne dopasowanie dla szybkiego przepływu elektronów
W tym zagłębieniu grupa hemowa cytochromu c6 — część, która faktycznie przenosi elektron — znajduje się zaledwie około jedenastu angstremów od specjalnej pary chlorofili w Fotosystemie I, która odbiera elektron. Interfejs wspierany jest przez gęstą sieć oddziaływań: ujemnie naładowane miejsca na cytochromie c6 przyciągają dodatnio naładowane regiony PsaF, podczas gdy obojętne i aromatyczne łańcuchy boczne tworzą szczelne, hydrofobowe kontakty głębiej w rowku. Szczególna arginina na cytochromie c6 (R66), od dawna uznawana za istotną u bakterii, układa się równolegle z sąsiednimi pierścieniami zarówno na cytochromie c6, jak i na Fotosystemie I, tworząc trzywarstwowe oddziaływanie, które wydaje się stabilizować pozycję dokowania. To ciasne upakowanie wypiera też wodę z bezpośredniej ścieżki między hemem a chlorofilem, prawdopodobnie obniżając opór dla przepływu elektronów i wyjaśniając, dlaczego transfer elektronów zachodzi w zaledwie kilka milionowych części sekundy.
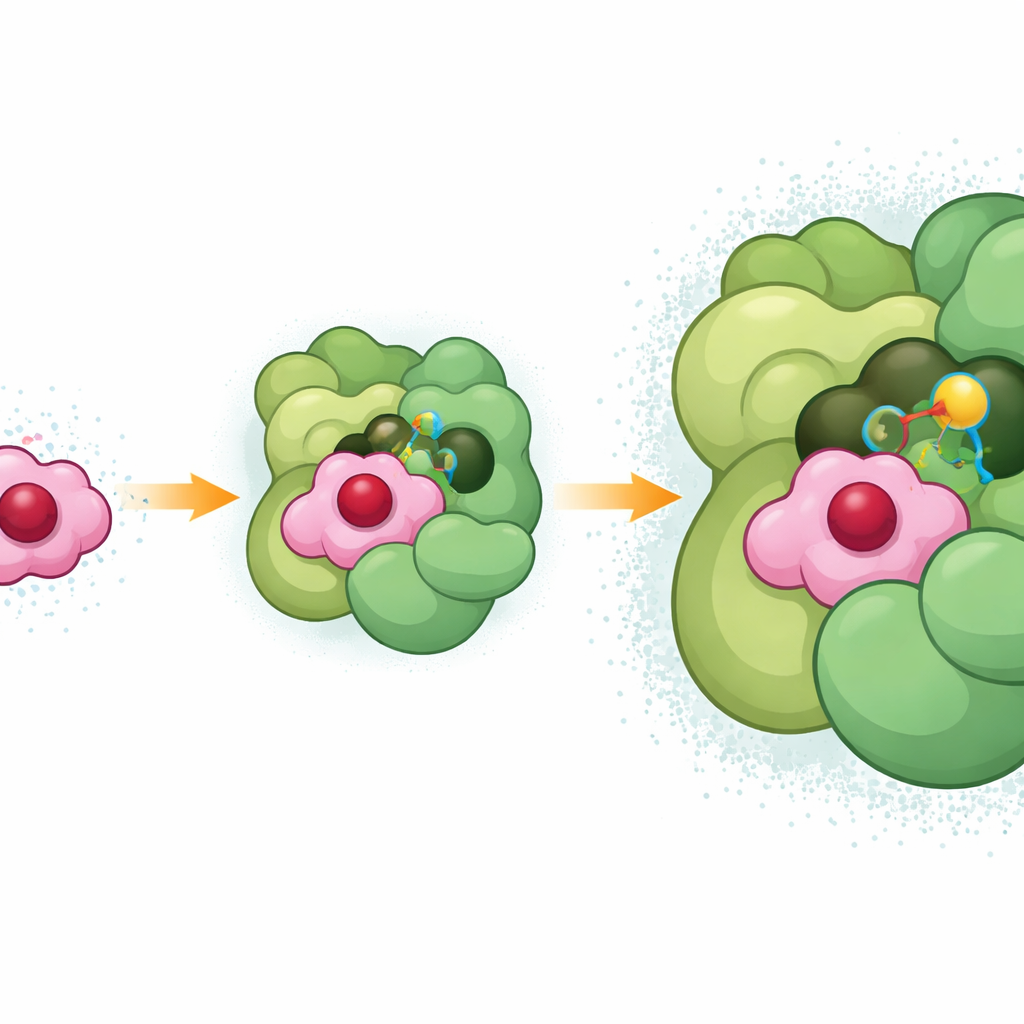
Testowanie krytycznych punktów kontaktu
Aby sprawdzić, które części cytochromu c6 są najważniejsze, zespół wprowadził celowane zmiany w kwaśnych i zasadowych resztach przewidywanych jako stykające się z Fotosystemem I. Gdy zneutralizowali niektóre ujemne ładunki w pobliżu „ramienia” PsaF lub zastąpili kluczową argininę, tempo ponownego redukowania Fotosystemu I wyraźnie spadło, a sieciowanie między dwoma białkami osłabło. Niektóre kombinacje zmian wykazały niespodziewane zachowanie, sugerując, że cytochrom c6 i Fotosystem I czasami mogą składać się w alternatywne, mniej wydajne układy. Razem te testy potwierdzają, że zarówno elektrostatyczny uchwyt oparty na PsaF, jak i układ warstwowy koncentrujący się na argininie są kluczowe dla szybkiego i niezawodnego dostarczania elektronów.
Co to znaczy dla biologicznych maszyn słonecznych
Praca dostarcza szczegółowego planu strukturalnego tego, jak cytochrom c6 przekazuje elektrony do Fotosystemu I w zielonych algach, łącząc cechy obserwowane u bakterii z cechami bardziej zaawansowanych roślin. Pokazuje, jak małe białko nośnikowe i duży kompleks błonowy współewoluowały, tworząc precyzyjnie wyregulowany interfejs łączący silne wiązanie, szybki transfer elektronów i szybkie uwalnianie na kolejny cykl. Poprzez wyjaśnienie tego starożytnego etapu w fotosyntetycznym przekaźniku, badanie pomaga zrozumieć, jak organizmy optymalizowały przetwarzanie światła na energię w toku ewolucji i daje wskazówki projektowe dla przyszłych wysiłków mających na celu zaprojektowanie lub naśladowanie naturalnych systemów słonecznej energii.
Cytowanie: Ogawa, Y., Mahapatra, G.P., Milrad, Y. et al. Cryo-EM structure of Chlamydomonas reinhardtii Photosystem I complexed with cytochrome c6. Nat Commun 17, 3031 (2026). https://doi.org/10.1038/s41467-026-70944-9
Słowa kluczowe: fotosynteza, Fotosystem I, cytochrom c6, transfer elektronów, cryo-EM