Clear Sky Science · sv
Att rikta in sig på NAT10 lindrar kolonsenescent och åldersutlöst kolit genom att störa N4-acetylering av DYRK1A
Varför åldrande tarmar är viktiga
När människor lever längre drabbas fler av matsmältningsproblem som tidigare var sällsynta i hög ålder. Ett sådant problem är ulcerös kolit som först visar sig hos äldre, med smärta, blödningar och en ökad risk för koloncancer. Denna studie ställer en enkel men kraftfull fråga: kan vi sakta ner eller till och med vända åldersrelaterad skada i kolonets slemhinna genom att rikta in oss på en enda molekylär ”brytare”, och därigenom göra åldersutlöst kolit mindre allvarlig?
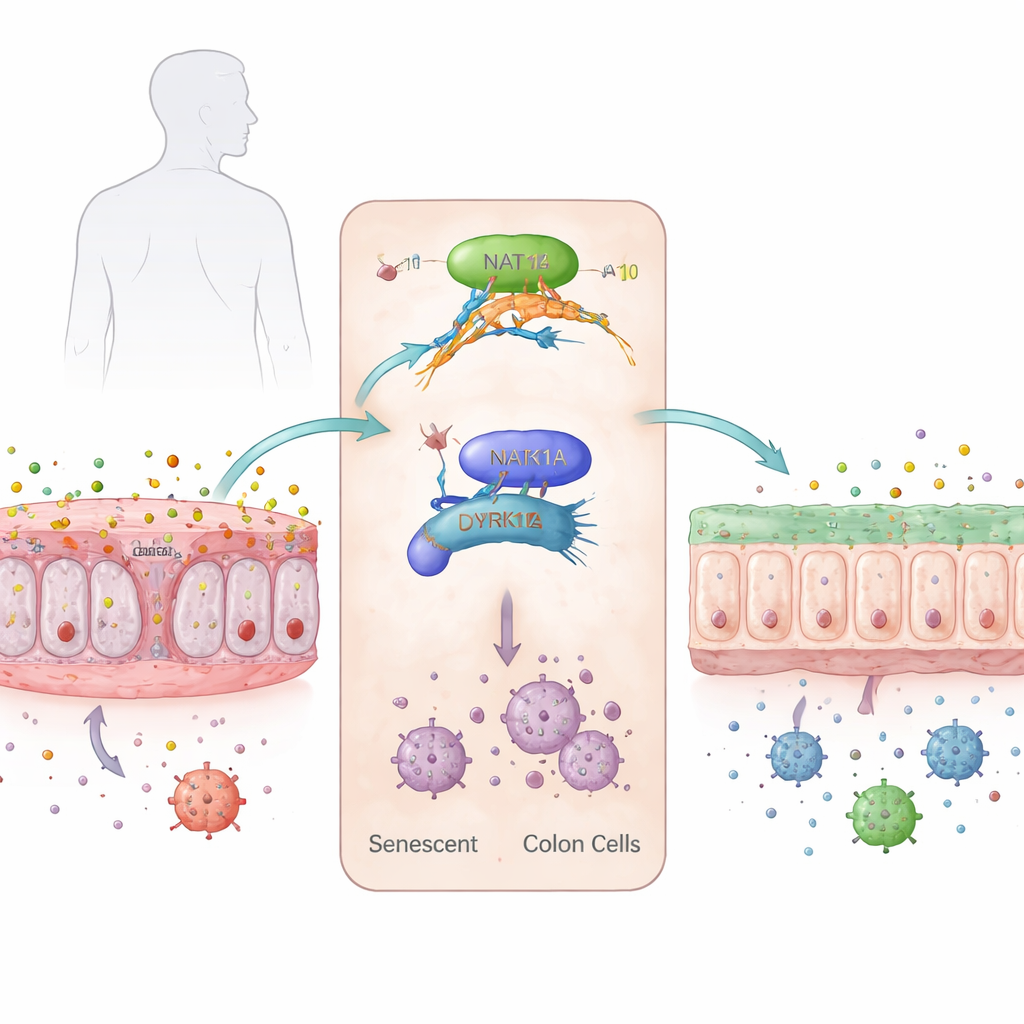
Åldrande celler i kolonets främsta linje
Kolonens inre yta är täckt av ett enda lager epitelceller som ständigt förnyar sig och bildar en barriär mellan vår kropp och den myllrande världen av tarmmikrober. Med åldern försvagas denna barriär: slemlaget blir tunnare, stamceller tappar kraft och många celler går in i ett tillstånd som kallas senescens, där de slutar dela sig men vägrar dö. Dessa senescenta celler läcker inflammatoriska ämnen som gör tarmen skörare och mer mottaglig för sjukdomar som ulcerös kolit, särskilt hos äldre vuxna vars behandlingsalternativ begränsas av andra hälsoproblem.
En kemisk markering på RNA som en dold drivkraft
Forskarna fokuserade på en subtil kemisk dekoration på RNA kallad N4‑acetylerad cytidin, eller ac4C, som kan göra vissa budskap i cellerna mer stabila och lättare att översätta till protein. De upptäckte att denna markering, och dess huvudenzym som skriver den, NAT10, ökar i gamla och konstgjort åldrade mänskliga kolonceller. När celler drevs in i senescens i laboratoriet steg nivåerna av ac4C, NAT10 blev mer förekommande, och klassiska åldersmarkörer och inflammatoriska gener slog på. I muskolon ökade NAT10‑nivåerna stadigt från ung till gammal ålder, i takt med en ökning av inflammationssignaler och tecken på DNA‑skada.
En enda väg som länkar märkt RNA till gamla celler
För att utröna hur denna RNA‑markering driver åldrande skannade teamet hela uppsättningen RNA‑molekyler i kolonceller och frågade vilka som fick mer ac4C när celler blev senescenta och förlorade det när NAT10 minskades. Ett tydligt uppstickande exempel var DYRK1A, ett proteinkinas som hjälper till att styra cellcykeln och DNA‑skaderesponsen. I senescenta kolonceller var DYRK1A:s RNA kraftigt dekorerat med ac4C längs kodningsregionen, vilket gjorde budskapet mer stabilt och mer effektivt översatt till protein. NAT10 band fysiskt till DYRK1A‑RNA, och att blockera NAT10 gjorde att DYRK1A‑budskapet bröts ner snabbare och användes mindre, vilket sänkte DYRK1A‑proteinhalten. Att återställa DYRK1A i NAT10‑utarmade celler återförde det senescenta, inflammatoriska tillståndet, vilket pekar på att det är en viktig downstream‑drivkraft.
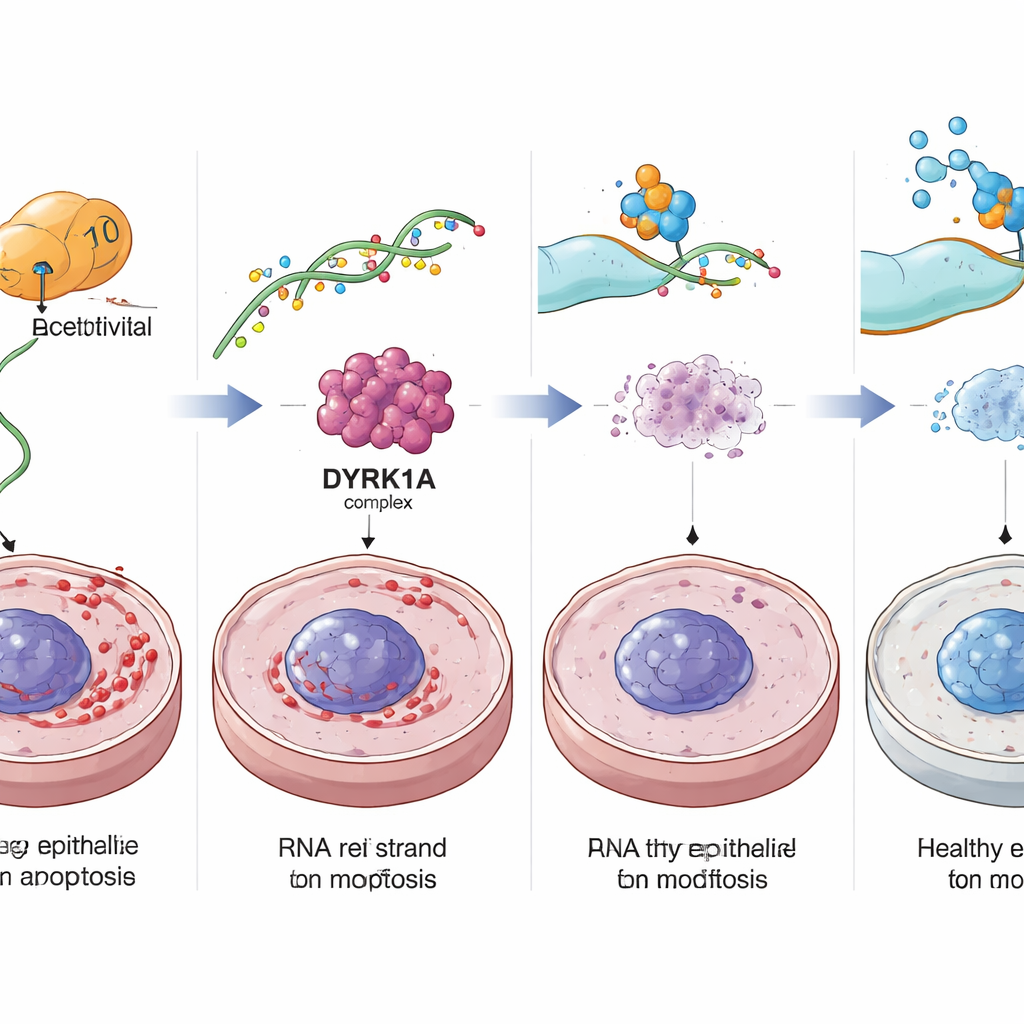
Föryngring av det åldrande kolon hos möss
Författarna testade sedan om nedreglering av denna NAT10–DYRK1A‑väg faktiskt kunde föryngra kolon i levande djur. Möss som bar bara en fungerande kopia av Nat10‑genen, eller gamla möss behandlade med ett NAT10‑hämmande läkemedel kallat Remodelin, visade färre senescenta celler, fler delande stamliknande celler, tjockare mukosalagren och förbättrade barriärproteiner i kolon. Små kolonorganoider odlade från dessa möss bildade fler knoppningsstrukturer och stod emot stress bättre, vilket tyder på starkare regenerativ kapacitet. När åldrade möss gavs en kemikalie som inducerar kolit ledde minskad Nat10 eller hämning av DYRK1A med läkemedlet Harmine till mindre viktnedgång, mildare koloninflammation, bättre sårläkning av sår och lägre markörer för DNA‑skada.
Signaler från mänskliga patienter
För att se om denna mekanism spelar roll hos människor undersökte teamet kolonbiopsier från friska unga vuxna, friska äldre individer och patienter med ulcerös kolit. Både NAT10 och DYRK1A var mer rikligt förekommande i kolonen hos äldre individer, och deras nivåer var ännu högre hos äldre patienter med ulcerös kolit. Dessutom tenderade de två proteinerna att öka tillsammans, och patienter med mer aktiv sjukdom hade de högsta nivåerna. Dessa observationer tyder på att NAT10–DYRK1A‑axeln inte bara är en egendomlighet hos modellmöss utan också är aktiv vid mänskligt åldrande och sjukdom.
Vad detta kan betyda för framtida behandlingar
Sammantaget målar studien upp en bild där ett RNA‑modifierande enzym, NAT10, bidrar till att föra kolonceller in i ett skadligt, långlivat senescent tillstånd genom att stabilisera DYRK1A‑RNA. I åldrande kolon och vid åldersutlöst ulcerös kolit verkar denna väg vara överaktiv, vilket försvagar barriären och förstärker inflammationen. Genom att dämpa NAT10 eller DYRK1A kunde forskarna föryngra kolonslemhinnan och lindra kolit hos åldrade möss. För icke‑specialister är huvudbudskapet att en reversibel kemisk markering på RNA kan vara ett nytt grepp för terapier som skyddar den åldrande tarmen och förbättrar utfall för äldre patienter med inflammatorisk tarmsjukdom.
Citering: Chen, J., Xue, M., Mi, S. et al. Targeting NAT10 alleviates colonic senescence and elderly-onset colitis by disrupting N4-acetylation of DYRK1A. Nat Commun 17, 3311 (2026). https://doi.org/10.1038/s41467-026-70220-w
Nyckelord: intestinal åldrande, ulcerös kolit, RNA‑modifiering, NAT10, cellulär senescens