Clear Sky Science · nl
Het remmen van NAT10 vermindert colonaal senescentie en bij ouderen optredende colitis door verstoring van N4-acetylatie van DYRK1A
Waarom verouderende darmen ertoe doen
Naarmate mensen langer leven, krijgt een groeiend deel van de bevolking te maken met spijsverteringsproblemen die vroeger zeldzaam waren op hoge leeftijd. Eén van die aandoeningen is colitis ulcerosa die voor het eerst bij ouderen optreedt, met pijn, bloedingen en een verhoogd risico op dikkedarmkanker tot gevolg. Deze studie stelt een eenvoudige maar krachtige vraag: kunnen we leeftijdsgebonden schade aan het darmslijmvlies vertragen of zelfs omkeren door één moleculaire "schakelaar" te richten, en zo colitis die op latere leeftijd begint minder ernstig maken?
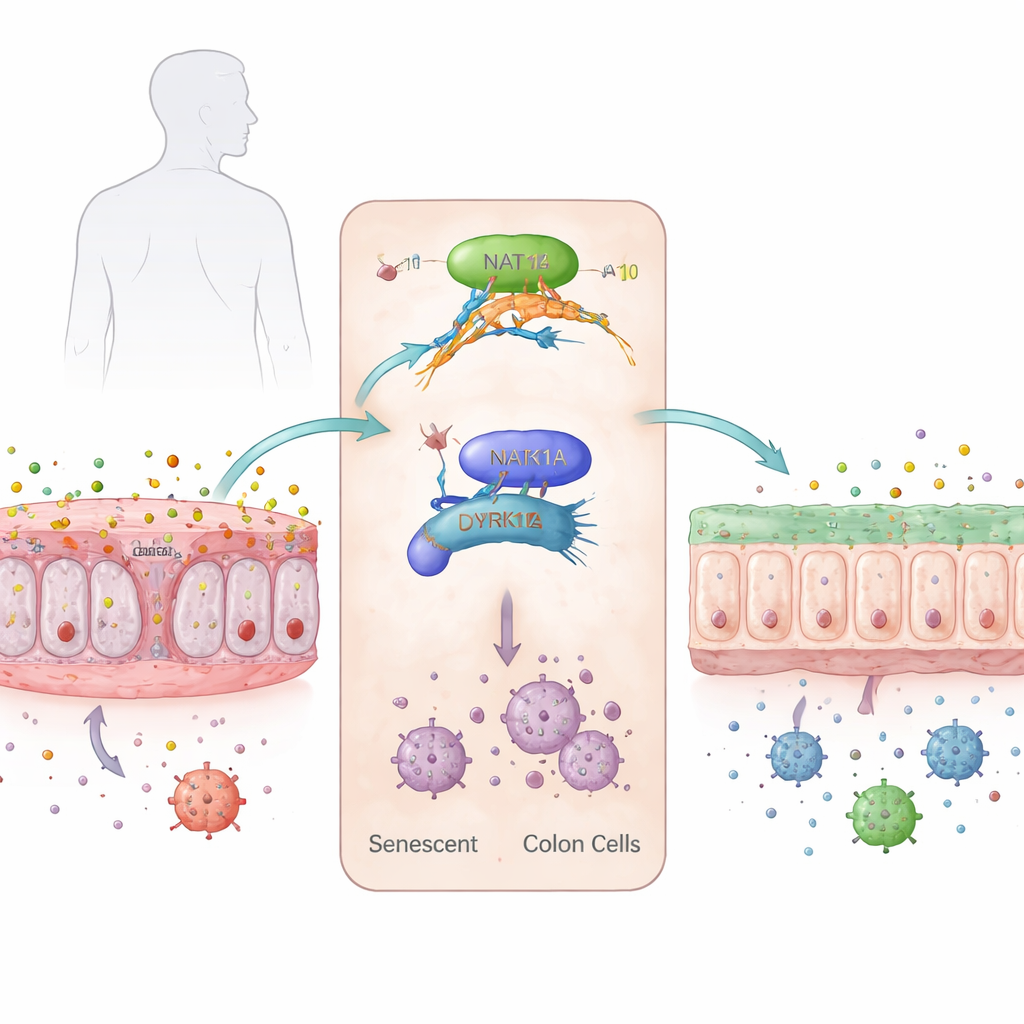
Verouderende cellen in de voorste linie van de darm
Het binnenoppervlak van de dikke darm is bedekt met een enkele laag epitheelcellen die zich voortdurend vernieuwen en zo een barrière vormen tussen ons lichaam en de miljoenen darmmicroben. Met het ouder worden verzwakt deze barrière: de slijmlaag wordt dunner, stamcellen verliezen vitaliteit en veel cellen raken in een staat die senescentie heet, waarin ze stoppen met delen maar niet afsterven. Deze senescentie cellen lekken ontstekingsbevorderende stoffen die de darm kwetsbaarder maken en de kans op ziekten als colitis ulcerosa vergroten, vooral bij oudere volwassenen van wie de behandelingsopties vaak beperkt zijn door andere gezondheidsproblemen.
Een chemische markering op RNA als verborgen aanjager
De onderzoekers richtten zich op een subtiele chemische versiering op RNA genaamd N4-acetylcytidine, of ac4C, die bepaalde boodschappen binnen cellen stabieler kan maken en gemakkelijker in eiwit vertaalt. Ze ontdekten dat deze markering, en het belangrijkste "schrijvende" enzym NAT10, verhoogd zijn in verouderde en kunstmatig verouderde menselijke coloncellen. Wanneer cellen in het laboratorium werden geduwd naar senescentie, stegen de ac4C-niveaus, nam NAT10 toe en werden klassieke verouderingsmarkers en ontstekingsgenen geactiveerd. In muizendarmen steeg het NAT10-gehalte geleidelijk van jeugd naar hoge leeftijd, wat samenging met toenemende ontstekingssignalen en aanwijzingen voor DNA-schade.
Een enkel pad dat gemarkeerd RNA met oude cellen verbindt
Om te achterhalen hoe deze RNA-markering veroudering aanjaagt, scanden de onderzoekers de volledige set RNA-moleculen in coloncellen en vroegen welke berichten ac4C kregen toen cellen senescent werden en het verloren wanneer NAT10 werd verminderd. Eén duidelijke kandidaat was DYRK1A, een proteïnekinase dat helpt bij het regelen van de celdeling en de reactie op DNA-schade. In senescente coloncellen was het RNA van DYRK1A zwaar versierd met ac4C over het coderende gedeelte, waardoor het bericht stabieler werd en efficiënter in eiwit werd omgezet. NAT10 bond fysiek aan DYRK1A-RNA, en het blokkeren van NAT10 zorgde ervoor dat het DYRK1A-bericht sneller afbrak en minder gebruikt werd, wat leidde tot lagere DYRK1A-eiwitniveaus. Het herstellen van DYRK1A in NAT10-verminderde cellen bracht de senescente, ontstekingsrijke toestand terug, wat het als een belangrijke downstream-aktor markeert.
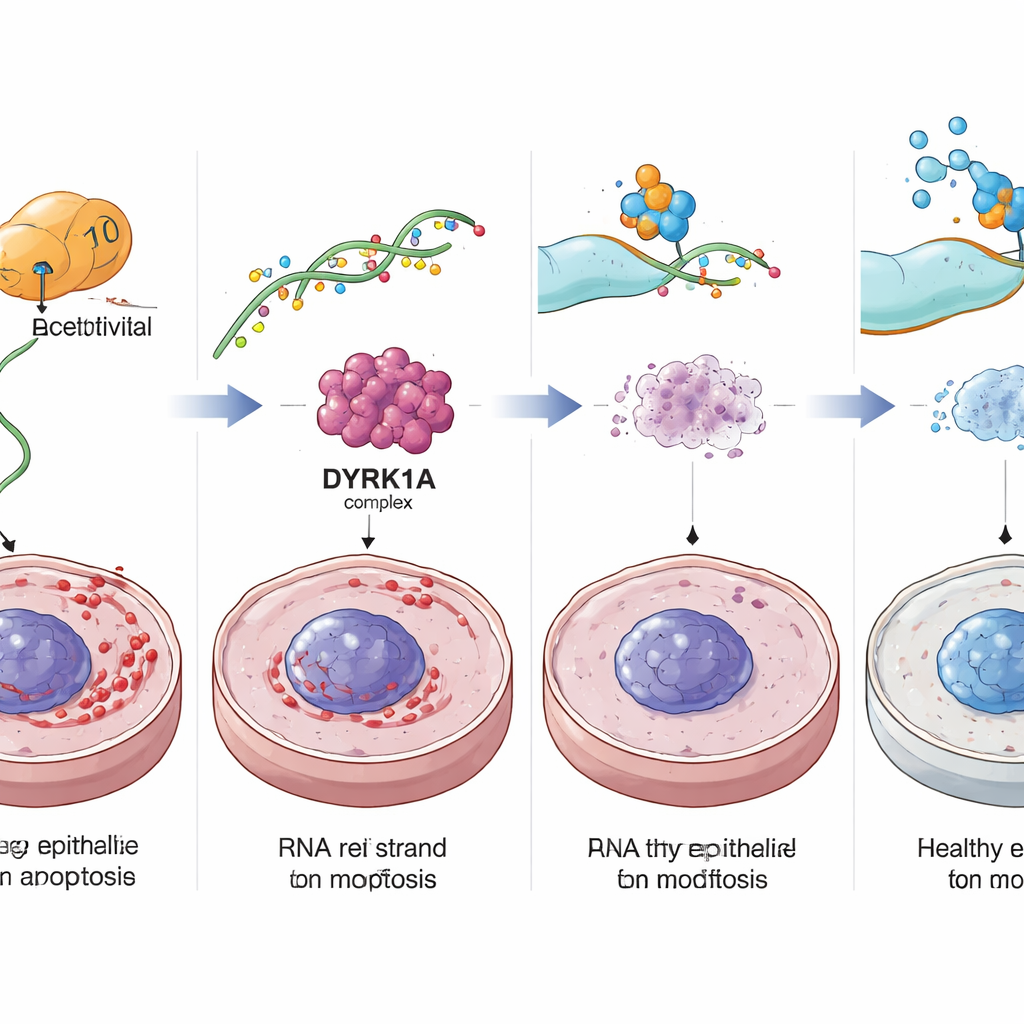
Het verjongen van de verouderende dikke darm bij muizen
De auteurs testten vervolgens of het terugschakelen van de NAT10–DYRK1A-route de dikke darm in levende dieren werkelijk kon verjongen. Muizen die slechts één werkend exemplaar van het Nat10-gen droegen, of oudere muizen behandeld met een NAT10-remmer genaamd Remodelin, vertoonden minder senescente cellen, meer delende stamachtige cellen, dikkere mucosale lagen en verbeterde barrière-eiwitten in de dikke darm. Kleine colon-organoïden uit deze muizen vormden meer uitgroeisels en waren beter bestand tegen stress, wat wijst op een sterkere regeneratieve capaciteit. Toen oudere muizen een chemische stof kregen die colitis opwekt, leidden het verminderen van Nat10 of het remmen van DYRK1A met het middel Harmine tot minder gewichtsverlies, mildere darmontstekingen, betere genezing van zweren en lagere markers van DNA-schade.
Signalen uit menselijke patiënten
Om te onderzoeken of dit mechanisme bij mensen van belang is, bekeken de onderzoekers colonbiopten van gezonde jonge volwassenen, gezonde ouderen en patiënten met colitis ulcerosa. Zowel NAT10 als DYRK1A waren overvloediger aanwezig in de dikke darmen van oudere individuen, en hun niveaus waren nog hoger bij oudere patiënten met colitis ulcerosa. Bovendien neigden de twee eiwitten samen te stijgen, en patiënten met ernstigere ziekteactiviteit hadden de hoogste niveaus. Deze waarnemingen suggereren dat de NAT10–DYRK1A-as niet alleen een eigenaardigheid van muismodellen is, maar ook actief is bij menselijke veroudering en ziekte.
Wat dit kan betekenen voor toekomstige behandelingen
Samengevat schetst de studie een beeld waarin een RNA-modificerend enzym, NAT10, helpt coloncellen in een schadelijke, levenslange senescente staat te duwen door DYRK1A-RNA te stabiliseren. In verouderende darmen en bij bij ouderen optredende colitis ulcerosa lijkt deze route overactief, wat de barrière verzwakt en ontsteking versterkt. Door NAT10 of DYRK1A terug te draaien, konden de onderzoekers darmweefsel verjongen en colitis verzachten bij oude muizen. Voor lezers zonder specialistische achtergrond is de kernboodschap dat een omkeerbare chemische markering op RNA mogelijk een nieuw aanknopingspunt biedt voor therapieën die het verouderende darmkanaal beschermen en de uitkomst voor oudere patiënten met inflammatoire darmaandoeningen verbeteren.
Bronvermelding: Chen, J., Xue, M., Mi, S. et al. Targeting NAT10 alleviates colonic senescence and elderly-onset colitis by disrupting N4-acetylation of DYRK1A. Nat Commun 17, 3311 (2026). https://doi.org/10.1038/s41467-026-70220-w
Trefwoorden: darmveroudering, colitis ulcerosa, RNA-modificatie, NAT10, cellulaire veroudering