Clear Sky Science · pl
Celowanie w NAT10 łagodzi starzenie okrężnicy i zapalenie jelita grubego na starość przez zaburzenie N4-acetylacji DYRK1A
Dlaczego starzejące się jelita mają znaczenie
W miarę jak ludzie żyją dłużej, coraz więcej z nas zmaga się z problemami trawiennymi, które dawniej rzadko pojawiały się w podeszłym wieku. Jednym z takich problemów jest wrzodziejące zapalenie jelita grubego rozpoczynające się u osób starszych, powodujące ból, krwawienia i zwiększone ryzyko raka jelita. Badanie stawia proste, ale istotne pytanie: czy można spowolnić albo nawet odwrócić związane z wiekiem uszkodzenia wyściółki okrężnicy, celując w pojedynczy molekularny „wyłącznik”, i w ten sposób złagodzić przebieg zapalenia jelita u osób w podeszłym wieku?
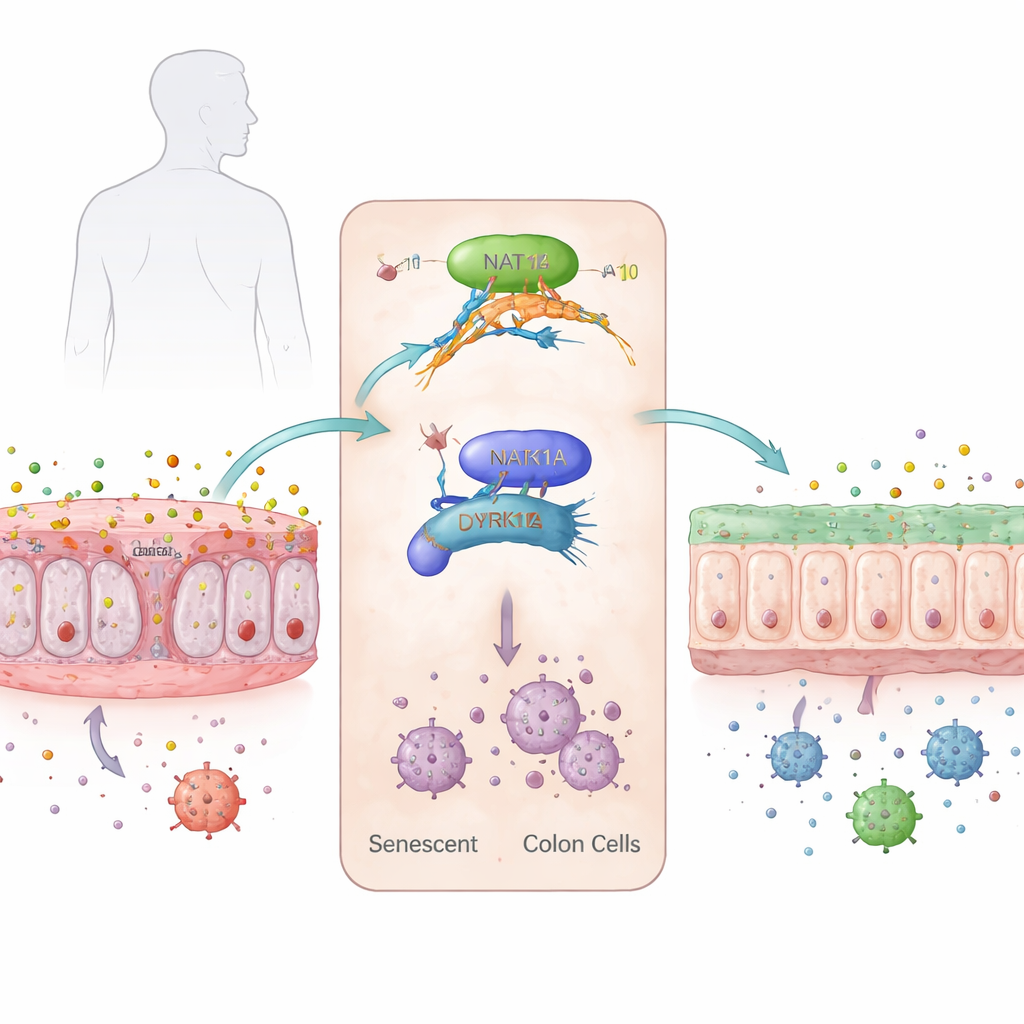
Starzejące się komórki na pierwszej linii
Wewnętrzną powierzchnię okrężnicy pokrywa pojedyncza warstwa komórek nabłonkowych, które nieustannie się odnawiają, tworząc barierę między naszym ciałem a obfitującym światem mikrobioty jelitowej. Wraz z wiekiem ta bariera osłabia się: warstwa śluzu staje się cieńsza, komórki macierzyste tracą energię, a wiele komórek wchodzi w stan zwany senescencją — przestają się dzielić, lecz nie ulegają apoptozie. Te senescentne komórki wydzielają substancje zapalne, które osłabiają jelito i zwiększają podatność na choroby, takie jak wrzodziejące zapalenie jelita grubego, szczególnie u starszych osób, których możliwości leczenia są ograniczone przez inne problemy zdrowotne.
Chemiczny znak na RNA jako ukryty sprawca
Naukowcy skupili się na subtelnej modyfikacji chemicznej RNA zwanej N4-acetylocytydyną, czyli ac4C, która może stabilizować niektóre komunikaty w komórkach i ułatwiać ich tłumaczenie na białko. Odkryli, że ten znak oraz główny enzym „piszący” go, NAT10, są zwiększone w starzejących się i sztucznie postarzałych ludzkich komórkach okrężnicy. Gdy komórki w laboratorium zostały sprowokowane do senescencji, poziomy ac4C wzrosły, NAT10 stał się bardziej obfity, a klasyczne markery starzenia i geny zapalne zostały włączone. U myszy w okrężnicy poziomy NAT10 rosły stopniowo od młodości do starości, co korelowało ze wzrostem sygnałów zapalnych i oznak uszkodzeń DNA.
Pojedynczy szlak łączący oznakowane RNA ze starymi komórkami
Aby ustalić, jak ten znak na RNA napędza proces starzenia, zespół przeanalizował cały zbiór cząsteczek RNA w komórkach okrężnicy i sprawdził, które z nich zyskiwały ac4C podczas wchodzenia w senescencję, a traciły go po zmniejszeniu NAT10. Jednym wyraźnym kandydatem był DYRK1A, kinaza białkowa pomagająca kontrolować cykl komórkowy i reakcje na uszkodzenia DNA. W senescentnych komórkach okrężnicy RNA DYRK1A było silnie oznaczone ac4C w obrębie regionu kodującego, co stabilizowało komunikat i zwiększało jego translację na białko. NAT10 wiązał się fizycznie z RNA DYRK1A, a zahamowanie NAT10 powodowało szybszy rozpad tego komunikatu i jego mniejsze wykorzystanie, obniżając poziomy białka DYRK1A. Przywrócenie DYRK1A w komórkach pozbawionych NAT10 przywracało stan senescentny i zapalny, wskazując na jego kluczową rolę jako efektora.
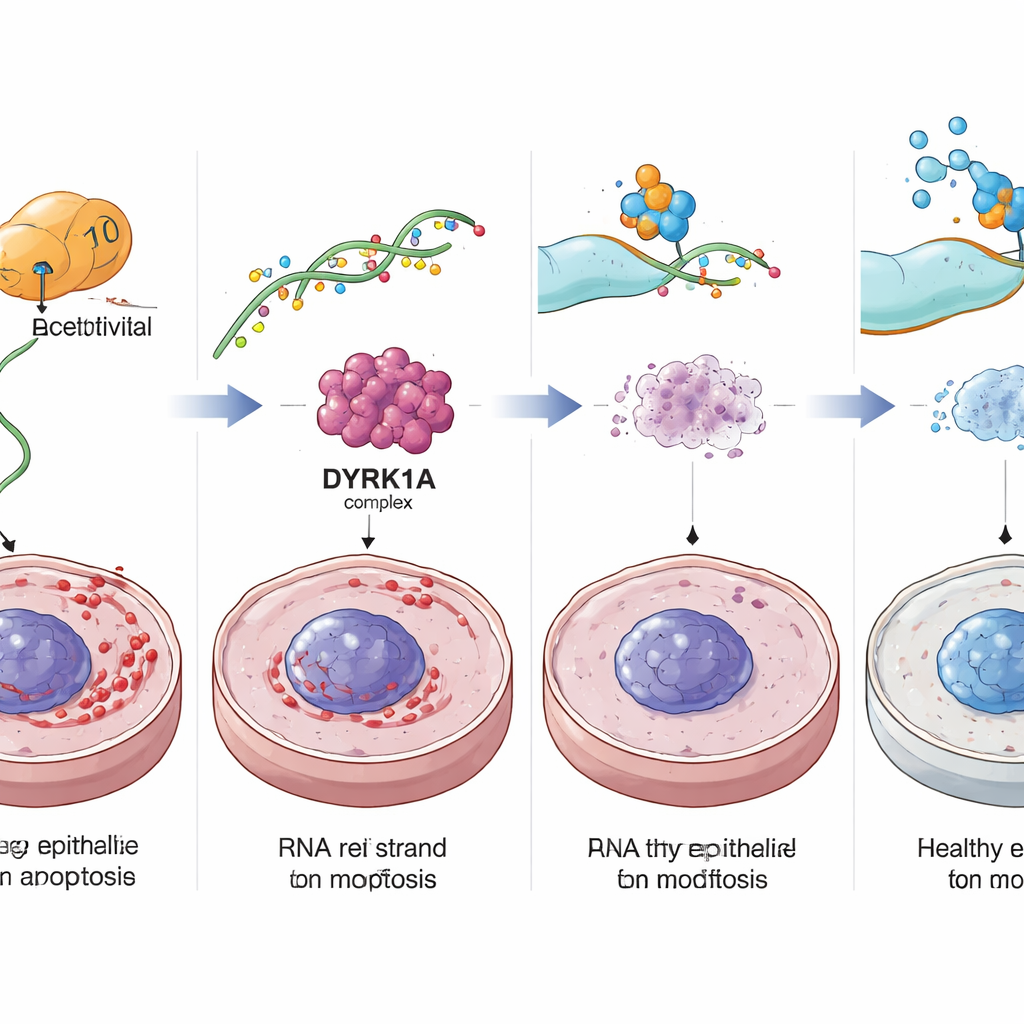
Młodzenie starzejącej się okrężnicy u myszy
Autorzy sprawdzili następnie, czy stłumienie szlaku NAT10–DYRK1A może faktycznie odmłodzić okrężnicę u żywych zwierząt. Myszy mające tylko jedną czynną kopię genu Nat10 albo stare myszy leczone lekiem blokującym NAT10 o nazwie Remodelin wykazywały mniej komórek senescentnych, więcej dzielących się komórek przypominających komórki macierzyste, grubsze warstwy śluzówki i lepsze białka bariery w okrężnicy. Maleńkie organoidy okrężnicy hodowane z tych myszy tworzyły więcej pączkujących struktur i lepiej znosiły stres, co sugeruje silniejszą zdolność regeneracyjną. Gdy starszym myszom podano substancję wywołującą zapalenie jelita, zmniejszenie aktywności Nat10 lub zahamowanie DYRK1A lekiem Harmine prowadziło do mniejszej utraty masy, łagodniejszego zapalenia okrężnicy, lepszego gojenia wrzodów i obniżenia markerów uszkodzeń DNA.
Sygnały od pacjentów
Aby sprawdzić, czy ten mechanizm ma znaczenie u ludzi, zespół przebadał próbki biopsji okrężnicy pochodzące od zdrowych młodych dorosłych, zdrowych starszych osób oraz pacjentów z wrzodziejącym zapaleniem jelita grubego. Zarówno NAT10, jak i DYRK1A były bardziej obfite w okrężnicach osób starszych, a ich poziomy były jeszcze wyższe u starszych pacjentów z wrzodziejącym zapaleniem jelita grubego. Co więcej, oba białka miały tendencję do jednoczesnego wzrostu, a pacjenci z cięższą aktywnością choroby mieli najwyższe poziomy. Te obserwacje sugerują, że oś NAT10–DYRK1A nie jest jedynie anomalią modeli mysich, lecz działa także w ludzkim starzeniu i chorobie.
Co to może znaczyć dla przyszłych terapii
W sumie badanie przedstawia obraz, w którym enzym modyfikujący RNA, NAT10, pomaga popychać komórki okrężnicy w szkodliwy, długotrwały stan senescencji przez stabilizowanie RNA DYRK1A. W starzejących się okrężnicach oraz w zapaleniu jelita grubego o początku w starszym wieku ten szlak wydaje się nadaktywny, osłabiając barierę i wzmacniając zapalenie. Wyhamowując NAT10 lub DYRK1A, badacze byli w stanie odmłodzić tkankę okrężnicy i złagodzić zapalenie u starych myszy. Dla czytelników niezwiązanych z nauką kluczowa wiadomość jest taka, że odwracalna chemiczna modyfikacja RNA może być nowym punktem uchwytu dla terapii chroniących starzejące się jelito i poprawiających wyniki leczenia starszych pacjentów z zapalnymi chorobami jelit.
Cytowanie: Chen, J., Xue, M., Mi, S. et al. Targeting NAT10 alleviates colonic senescence and elderly-onset colitis by disrupting N4-acetylation of DYRK1A. Nat Commun 17, 3311 (2026). https://doi.org/10.1038/s41467-026-70220-w
Słowa kluczowe: starzenie jelit, wrzodziejące zapalenie jelita grubego, modyfikacja RNA, NAT10, starzenie komórkowe