Clear Sky Science · de
Die Zielsteuerung von NAT10 lindert koloniale Seneszenz und im Alter beginnende Kolitis durch Störung der N4-Acetylierung von DYRK1A
Warum gealterte Därme wichtig sind
Da Menschen länger leben, haben immer mehr von uns Verdauungsprobleme, die früher im hohen Alter selten waren. Ein solches Problem ist die Colitis ulcerosa, die erstmals im Seniorenalter auftreten kann, mit Schmerzen, Blutungen und einem erhöhten Risiko für Darmkrebs. Diese Studie stellt eine einfache, aber wirkungsvolle Frage: Können wir altersbedingte Schäden der Darmoberfläche verlangsamen oder sogar umkehren, indem wir einen einzelnen molekularen "Schalter" ansteuern — und dadurch die im Alter beginnende Colitis weniger schwer verlaufen lassen?
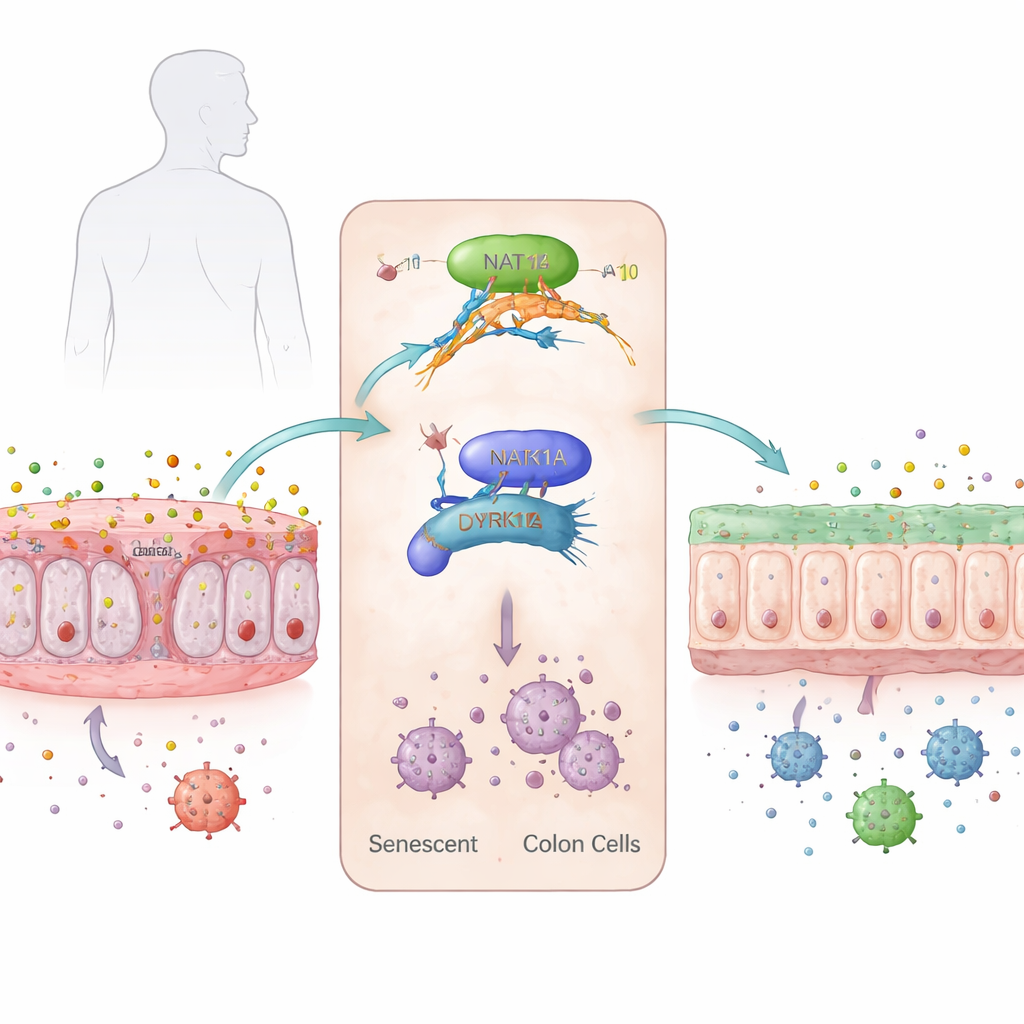
Alterszellen an der Frontlinie des Dickdarms
Die innere Oberfläche des Dickdarms ist von einer einzigen Schicht von Epithelzellen bedeckt, die sich ständig erneuern und eine Barriere zwischen unserem Körper und der dicht besiedelten Welt der Darmmikroben bilden. Mit zunehmendem Alter wird diese Barriere schwächer: Die Schleimschicht dünnt aus, Stammzellen verlieren an Leistungsfähigkeit und viele Zellen treten in einen Zustand namens Seneszenz ein, in dem sie aufhören, sich zu teilen, aber nicht sterben. Diese seneszenten Zellen setzen entzündungsfördernde Substanzen frei, die den Darm fragiler machen und das Risiko für Erkrankungen wie Colitis ulcerosa erhöhen — besonders bei älteren Erwachsenen, deren Behandlungsmöglichkeiten durch andere Gesundheitsprobleme eingeschränkt sind.
Eine chemische Markierung auf RNA als verborgener Treiber
Die Forscher konzentrierten sich auf eine subtile chemische Kennzeichnung auf RNA namens N4-Acetylcytidin oder ac4C, die bestimmte Botenstoffe in Zellen stabiler machen und deren Übersetzung in Protein fördern kann. Sie fanden heraus, dass diese Markierung und das sie schreibende Enzym NAT10 in gealterten und künstlich gealterten menschlichen Darmzellen zunehmen. Wenn Zellen im Labor in Seneszenz getrieben wurden, stiegen die ac4C-Werte, NAT10 wurde vermehrt und typische Altersmarker sowie entzündliche Gene wurden aktiviert. In den Mäusedärmen stieg NAT10 mit zunehmendem Alter kontinuierlich an, einhergehend mit einer Zunahme entzündlicher Signale und Hinweisen auf DNA-Schäden.
Ein einzelner Weg, der markierte RNA mit alten Zellen verbindet
Um herauszufinden, wie diese RNA-Markierung das Altern vorantreibt, durchsuchte das Team das gesamte Spektrum der RNA-Moleküle in Darmzellen und fragte, welche von ihnen ac4C gewinnen, wenn Zellen seneszent werden, und diese Markierung verlieren, wenn NAT10 reduziert wird. Ein klarer Spitzenreiter war DYRK1A, eine Proteinkinase, die am Zellzyklus und an Reaktionen auf DNA-Schäden beteiligt ist. In seneszenten Darmzellen war die DYRK1A-RNA entlang ihres kodierenden Bereichs stark mit ac4C versehen, wodurch die Nachricht stabiler und effizienter in Protein übersetzt wurde. NAT10 band physisch an DYRK1A-RNA, und das Blockieren von NAT10 führte dazu, dass die DYRK1A-Botschaft schneller abgebaut und seltener genutzt wurde, was die DYRK1A-Proteinmenge senkte. Die Wiederherstellung von DYRK1A in NAT10-verarmten Zellen brachte den seneszenten, entzündlichen Zustand zurück und markiert DYRK1A damit als wichtigen nachgelagerten Treiber.
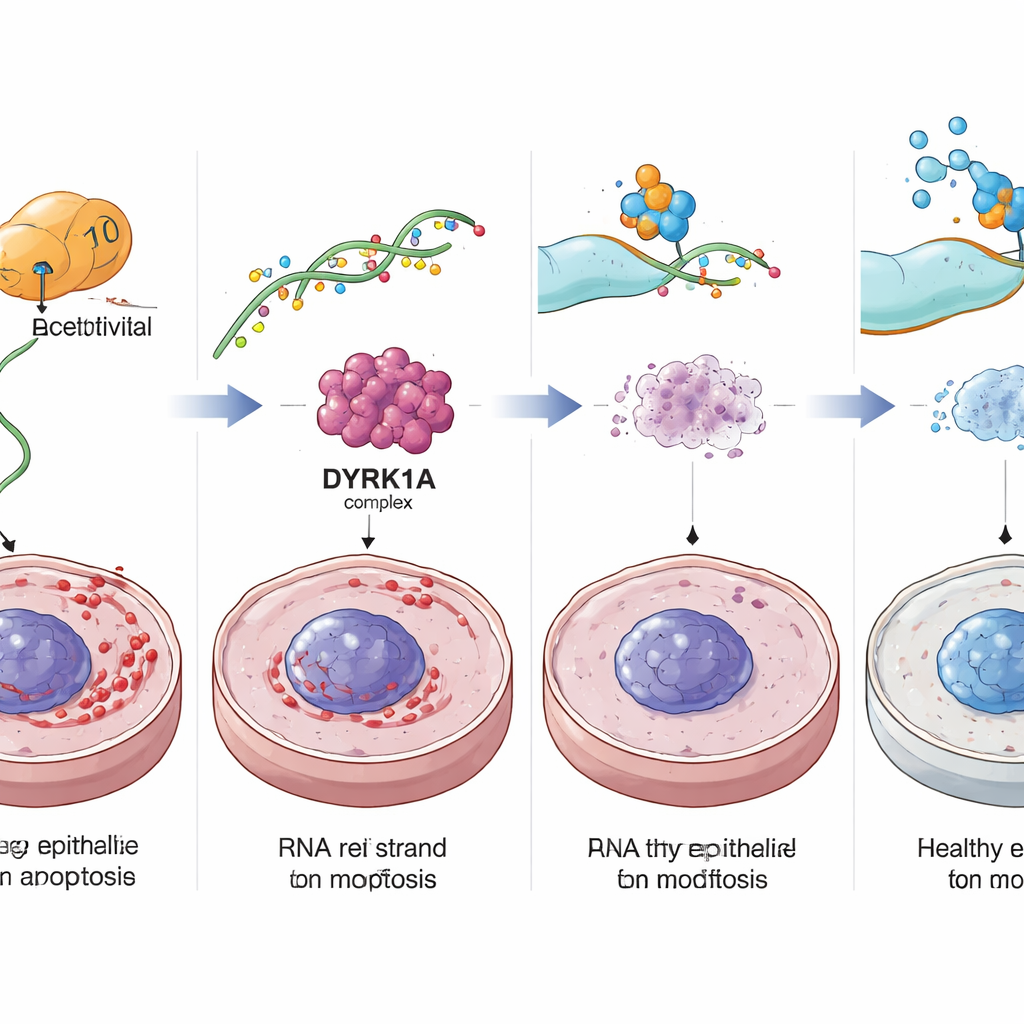
Verjüngung des gealterten Dickdarms bei Mäusen
Die Autoren prüften anschließend, ob das Absenken dieser NAT10–DYRK1A-Achse den Darm in lebenden Tieren tatsächlich verjüngen kann. Mäuse mit nur einer funktionierenden Kopie des Nat10-Gens oder gealterte Mäuse, die mit einem NAT10-blockierenden Wirkstoff namens Remodelin behandelt wurden, zeigten weniger seneszente Zellen, mehr teilende, stammzellähnliche Zellen, dickere Mukosaschichten und verbesserte Barrieremoleküle im Darm. Kleine Kolon-Organoide aus diesen Mäusen bildeten mehr Knospenstrukturen und widerstanden Stress besser, was auf eine stärkere Regenerationsfähigkeit hindeutet. Als gealterten Mäusen eine chemische Substanz verabreicht wurde, die Kolitis auslöst, führten die Reduktion von Nat10 oder die Hemmung von DYRK1A mit dem Wirkstoff Harmine zu geringerem Gewichtsverlust, milderen Entzündungen des Darms, besserer Heilung von Geschwüren und niedrigeren Markern für DNA-Schäden.
Signale aus Patientenproben
Um zu prüfen, ob dieser Mechanismus beim Menschen relevant ist, untersuchte das Team Kolonbiopsien von gesunden jungen Erwachsenen, gesunden älteren Personen und Patienten mit Colitis ulcerosa. Sowohl NAT10 als auch DYRK1A waren in den Kolonen älterer Personen stärker vertreten, und ihre Werte waren bei älteren Patienten mit Colitis ulcerosa noch höher. Zudem stiegen die beiden Proteine tendenziell gemeinsam an, und Patienten mit stärkerer Krankheitsaktivität zeigten die höchsten Werte. Diese Beobachtungen deuten darauf hin, dass die NAT10–DYRK1A-Achse kein Mausmodellartefakt ist, sondern auch beim menschlichen Altern und bei Erkrankungen aktiv sein dürfte.
Was das für künftige Behandlungen bedeuten könnte
In der Summe zeichnet die Studie das Bild, dass ein RNA-modifizierendes Enzym, NAT10, Darmzellen in einen schädlichen, langlebigen seneszenten Zustand treibt, indem es die DYRK1A-RNA stabilisiert. In gealterten Kolonen und bei im Alter beginnender Colitis ulcerosa scheint diese Achse überaktiv zu sein, die Barriere zu schwächen und die Entzündung zu verstärken. Durch das Herunterregeln von NAT10 oder DYRK1A konnten die Forschenden Darmgewebe verjüngen und die Colitis bei gealterten Mäusen abmildern. Für Laien lautet die Kernbotschaft: Eine reversible chemische Markierung auf RNA könnte ein neuer Ansatzpunkt für Therapien sein, die den alternden Darm schützen und die Behandlungsergebnisse älterer Patientinnen und Patienten mit entzündlichen Darmerkrankungen verbessern.
Zitation: Chen, J., Xue, M., Mi, S. et al. Targeting NAT10 alleviates colonic senescence and elderly-onset colitis by disrupting N4-acetylation of DYRK1A. Nat Commun 17, 3311 (2026). https://doi.org/10.1038/s41467-026-70220-w
Schlüsselwörter: Darmalterung, Colitis ulcerosa, RNA-Modifikation, NAT10, zelluläre Seneszenz