Clear Sky Science · sv
En perfunderad, parallelliserad blod-hjärnbarriär-tumörplattform för undersökning av ämnens permeation och effekt
Varför det är så svårt att behandla hjärntumörer
Moderna cancerläkemedel har förbättrat överlevnaden för många patienter, men hjärntumörer förblir svåra att behandla. En viktig orsak är hjärnans eget säkerhetssystem, blod-hjärnbarriären, som blockerar de flesta ämnen från att komma in i hjärnan. Denna studie beskriver en laboratorieodlad modell som förenar en realistisk hjärnbarriär med patientderiverad hjärntumörvävnad på en miniatyr plastplattform, så att forskare bättre kan se vilka läkemedel som faktiskt når tumörer och hur väl de fungerar när de väl anländer.
En liten barriär som blockerar stora förhoppningar
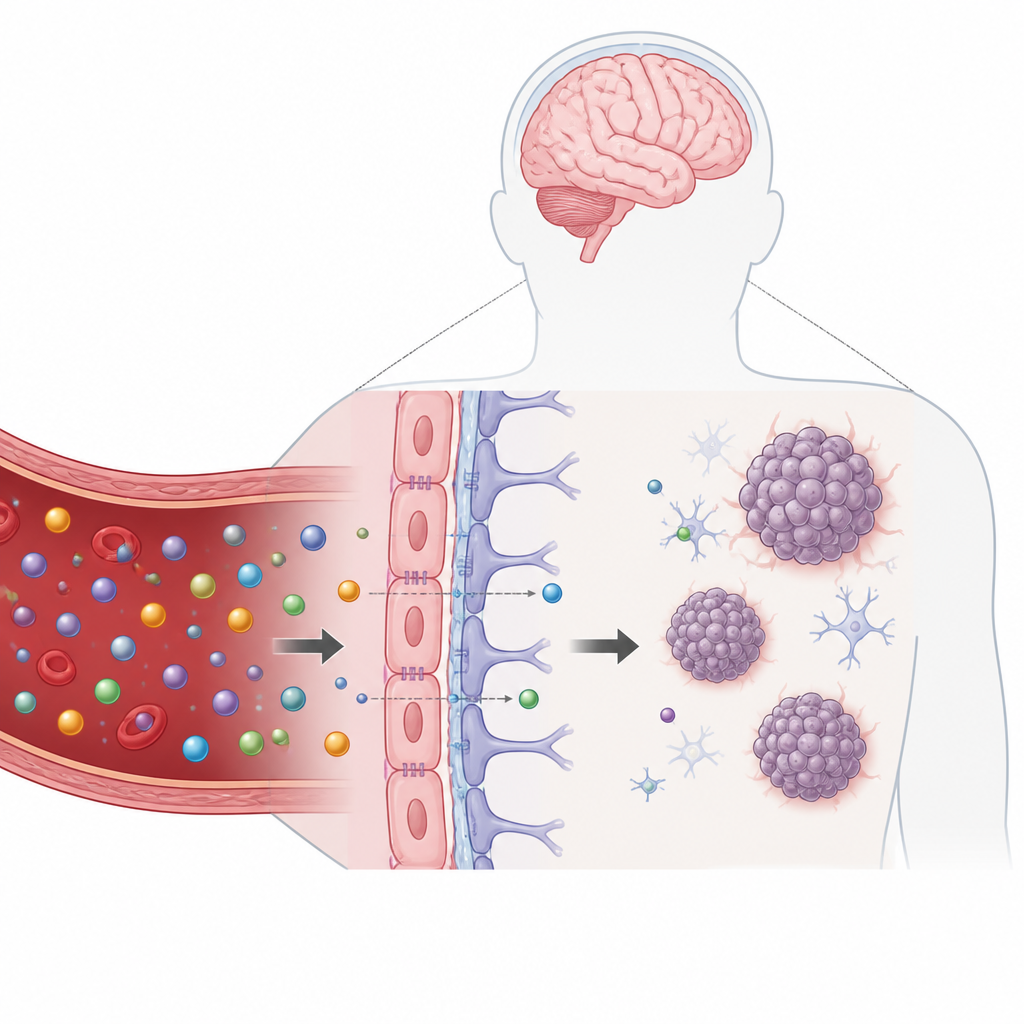
Blod-hjärnbarriären är ett tunt cellskikt som bekläder blodkärl i hjärnan och noggrant kontrollerar vad som släpps igenom från blodomloppet. Medan den skyddar våra hjärnor från toxiner hindrar den också många hjälpsamma läkemedel. Detta är särskilt problematiskt för barn med diffus mittlinje-gliom, en aggressiv hjärnstams-tumör med mycket dålig överlevnad. Befintliga platta cellkulturer och även många tredimensionella tumörmodeller saknar ofta en realistisk hjärnbarriär, vilket gör att läkemedel ser mer lovande ut i labbet än de visar sig vara hos patienter.
Bygga en hjärnbarriär och tumör på ett chip
För att åtgärda detta gap byggde forskarna en handflatesstor plastanordning som rymmer 32 miniatyrenheter ordnade som brunnarna i en standardlabplatta. Varje enhet innehåller en smal kanal klädd med mänskliga blodkärlsceller, stödjade av hjärnans stödjeceller — astrocyter och pericyter — inbäddade i en mjuk gel nedanför. Tillsammans bildar de en kompakt modell av blod-hjärnbarriären. Direkt under denna barriär skapade teamet en liten hängande droppe som kan hålla en enda sfärisk klump av tumörceller, odlade separat från celler donerade av barn med diffus mittlinje-gliom. Denna droppe placerar tumören mycket nära den konstgjorda blodkärlet, liknande dess läge i hjärnstammen.
Simulera blodflöde utan pumpar
I en levande hjärna utsätts kärlceller för konstant flöde och ett milt skjuv från det rörliga blodet, vilket hjälper barriären att hålla tätt. För att efterlikna detta utan skrymmande utrustning monterade teamet sin platta på en tiltande plattform inne i en varm inkubator. Genom att långsamt gunga plattan fram och tillbaka skapade de gravitationsdrivet flöde av näringslösning genom varje kanal, vilket utsatte kärlcellerna för realistiska nivåer av skjuvspänning. Datorsimuleringar och mätningar bekräftade att flödet och de mekaniska krafterna låg inom det intervall som förväntas i verkliga hjärnans kärl, och att barriären förblev tät för små fluorescerande testmolekyler.
Testa verkliga cancerläkemedel i en realistisk miljö
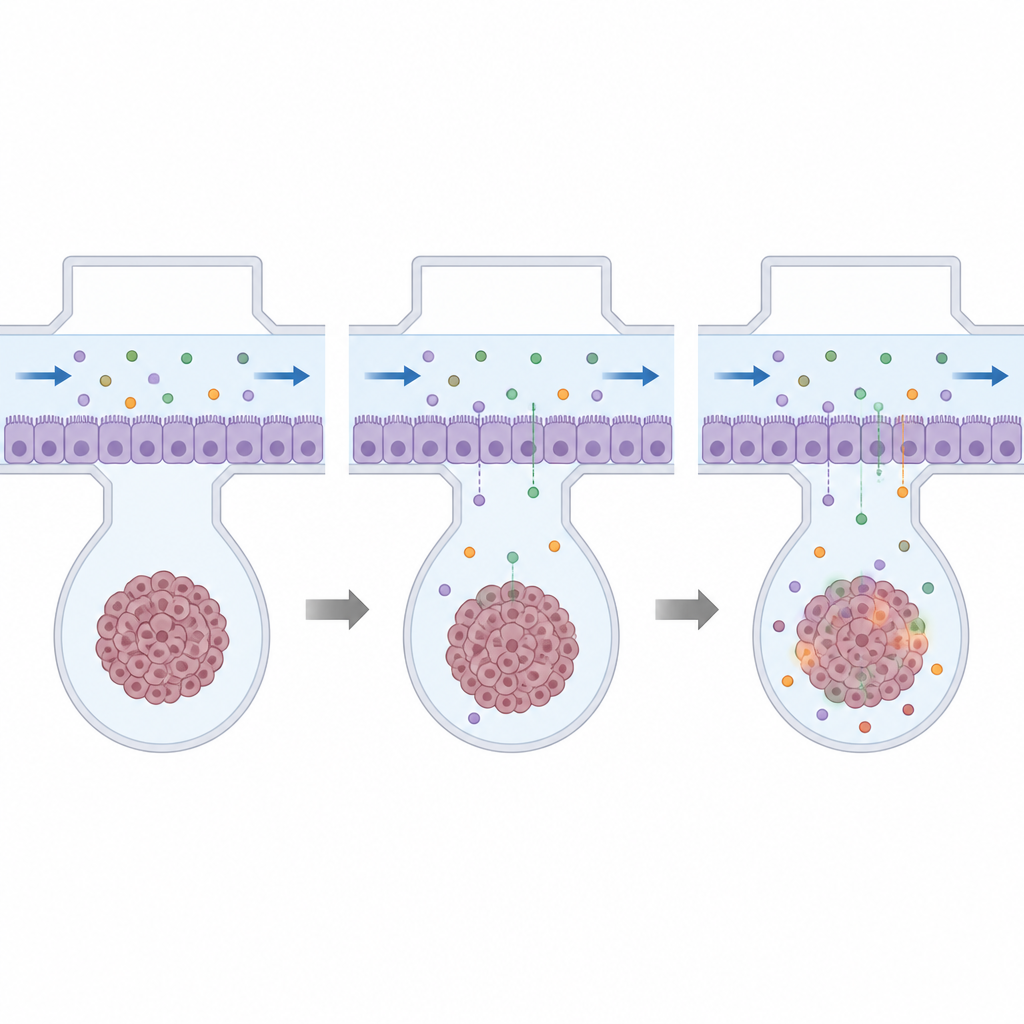
Med plattformen etablerad testade forskarna fyra existerande cytostatika som redan är godkända för andra cancerformer: cisplatin, doksorubicin, homoharringtonin och doketaxel. Först exponerade de hjärntumörsfäroider och blod-hjärnbarriärsfäroider i vanliga plattor för ett brett dosintervall för att bestämma hur mycket av varje läkemedel som dödade hälften av cellerna. Detta hjälpte dem välja doser som var skadliga för tumörceller men mindre skadliga för själva barriären. De flödade sedan dessa doser genom chipets övre kanal, vilket gjorde att läkemedlen bara nådde tumören om de kunde permeera genom det täta cellskiktet.
Vad den nya plattformen avslöjar
Resultaten visade att även när läkemedel tydligt var toxiska för tumörceller i standardskålar minskade närvaron av en intakt blod-hjärnbarriär på chipet starkt deras effekt. Tumörsfäroider bakom barriären förlorade betydligt färre celler än de som direkt badades i läkemedelslösning, vilket betonar hur kraftfullt barriären begränsar verklig läkemedelsexponering. Vissa läkemedel, såsom doksorubicin och homoharringtonin, gjorde också barriären läckigare vid doser långt under dem som dödade barriärcellerna, vilket tillät mer läkemedel att passera men också signalerade potentiell skada för frisk hjärnvävnad. Viktigt är att tumörer från olika patienter svarade olika, vilket understryker behovet av personaliserad testning.
Att föra personanpassad hjärntumörtestning närmare kliniken
För en icke-specialist är huvudbudskapet att det inte räcker att ett cancerläkemedel dödar tumörceller i en skål; det måste också korsa hjärnans skyddsvägg utan att orsaka för stor skada. Denna studie presenterar ett praktiskt, skalbart verktyg som förenar en realistisk blod-hjärnbarriär och patientderiverad tumörvävnad i ett miniatyriserat system. Eftersom varje testenhet använder endast några hundra tumörceller skulle sådana plattformar en dag kunna testa paneler av läkemedel och doser på ett barns egna celler före behandling, och hjälpa läkare att välja alternativ som både är effektivare och säkrare för hjärnan.
Citering: Wei, W., Stano, M., Kritzer, B. et al. A perfused, parallelized blood brain barrier-tumor platform for compound permeation and efficacy investigations. Microsyst Nanoeng 12, 175 (2026). https://doi.org/10.1038/s41378-026-01268-3
Nyckelord: blod-hjärnbarriär, diffus mittlinje-gliom, organ-on-chip, hjärntumörläkemedel, mikrofluidisk plattform