Clear Sky Science · nl
Een geperfundeerd, parallel uitgevoerd bloed-hersenbarrière-tumorplatform voor onderzoek naar doorlaatbaarheid van verbindingen en werkzaamheid
Waarom het zo moeilijk is hersentumoren te behandelen
Moderne kankerbehandelingen hebben het overleven van veel patiënten verbeterd, maar hersentumoren blijven hardnekkig moeilijk te behandelen. Een belangrijke reden is het eigen beveiligingssysteem van de hersenen, de bloed-hersenbarrière, die de meeste stoffen tegenhoudt voordat ze de hersenen bereiken. Deze studie beschrijft een in het laboratorium gekweekt model dat een realistische hersenbarrière en patiëntafgeleid hersentumorweefsel samenbrengt op een miniatuur plastic platform, zodat onderzoekers beter kunnen zien welke geneesmiddelen daadwerkelijk tumoren bereiken en hoe goed ze werken zodra ze daar aankomen.
Een klein schild dat grote hoop blokkeert
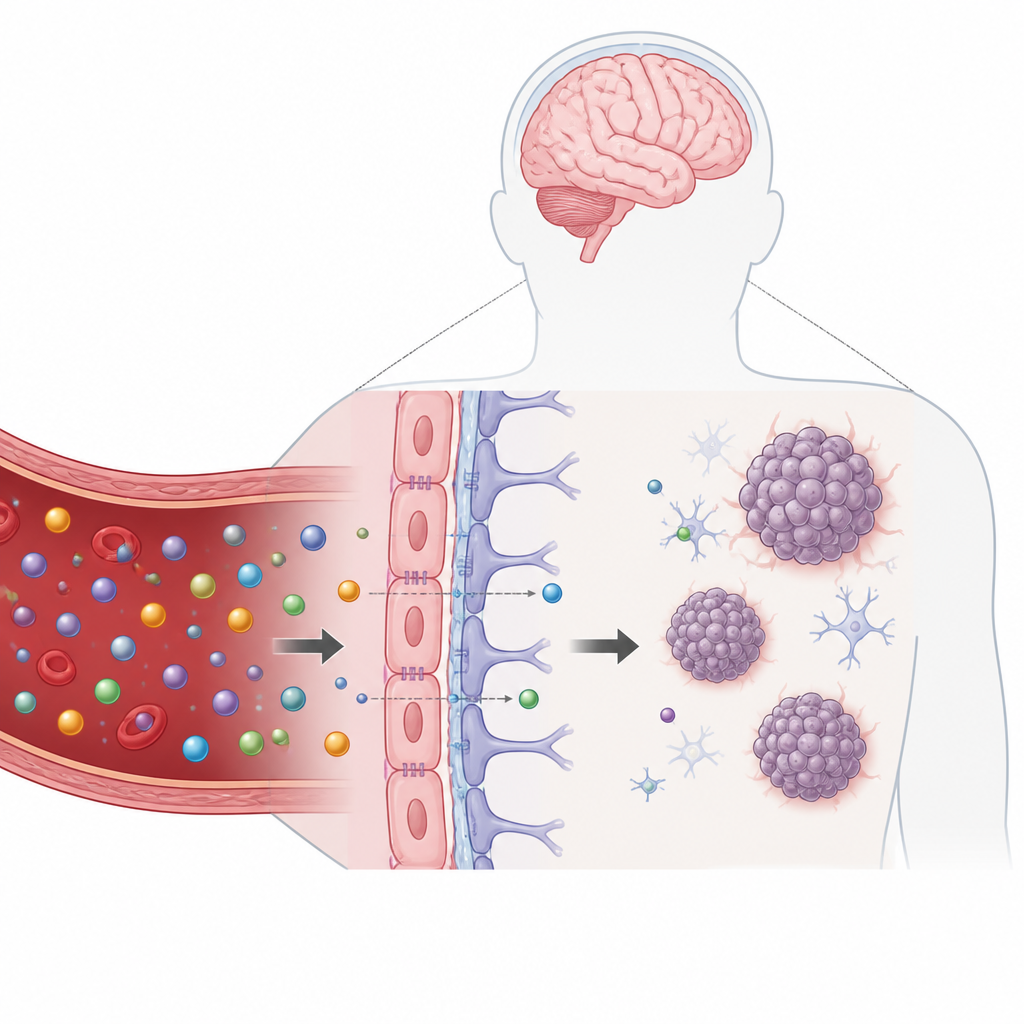
De bloed-hersenbarrière is een dunne laag cellen die de bloedvaten in de hersenen bekleedt en nauwkeurig bepaalt wat er vanuit de bloedbaan doordringt. Terwijl zij onze hersenen beschermt tegen toxines, houdt ze ook veel nuttige medicijnen buiten. Dit is bijzonder problematisch voor kinderen met diffuse midline-glioma, een agressieve tumor in de hersenstam met zeer slechte overlevingskansen. Bestaande platte celkweken en zelfs veel driedimensionale tumormodellen laten vaak een realistische hersenbarrière weg, waardoor geneesmiddelen in het lab veelbelovender lijken dan ze in patiënten blijken te zijn.
Een hersenbarrière en tumor op een chip bouwen
Om deze kloof te dichten, bouwden de onderzoekers een handpalmgroot plastic apparaat dat 32 miniatuur testunits bevat, gerangschikt als de putjes in een standaard laboratoriumplaat. Elke unit bevat een smalle kanaal bekleed met menselijke bloedvatcellen, ondersteund door hersensteuncellen genaamd astrocyten en pericyten ingebed in een zachte gel eronder. Samen vormen zij een compact model van de bloed-hersenbarrière. Direct onder deze barrière creëerde het team een klein hangend druppeltje dat één bolvormige klomp tumorcellen kan bevatten, geteeld uit cellen gedoneerd door kinderen met diffuse midline-glioma. Dit druppeltje plaatst de tumor zeer dicht bij het artificiële bloedvat, vergelijkbaar met de ligging in de hersenstam.
Bloedstroom simuleren zonder pompen
In een levend brein ervaren vatcellen constante stroming en zachte wrijving van het bewegende bloed, wat helpt de barrière strak te houden. Om dit na te bootsen zonder omvangrijke apparatuur, monteerden de onderzoekers hun plaat op een kantelstage in een warme incubator. Door de plaat langzaam heen en weer te wiegen creëerden zij zwaartekrachtgestuurde stroom van voedingsvloeistof door elk kanaal, waardoor de vatcellen blootgesteld werden aan realistische niveaus van schuifspanning. Computersimulaties en metingen bevestigden dat de stroming en mechanische krachten binnen het bereik bleven dat verwacht wordt in echte hersenvaten, en dat de barrière ondoorlatend bleef voor kleine fluorescerende testmoleculen.
Reële kankermiddelen testen in een realistische omgeving
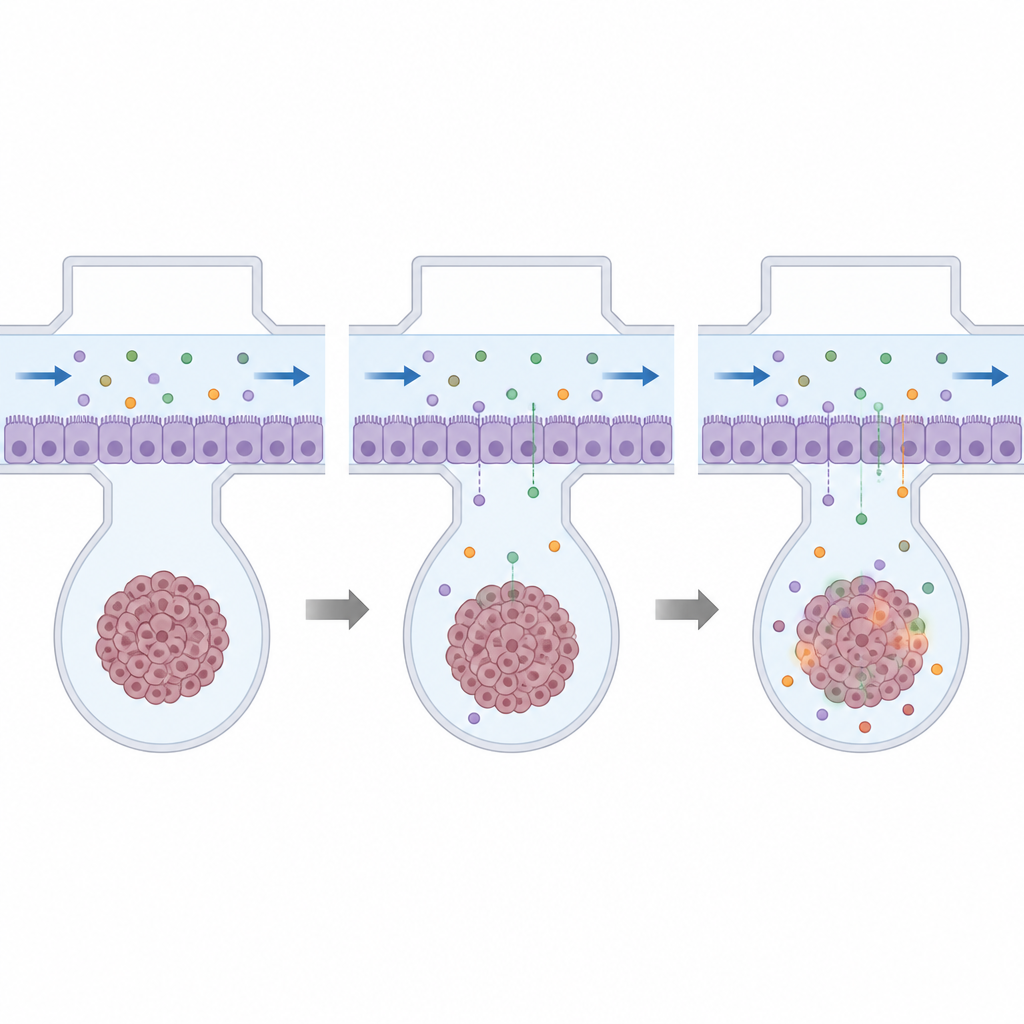
Nadat het platform was opgezet, testten de onderzoekers vier bestaande chemotherapeutica die al voor andere kankers zijn goedgekeurd: cisplatine, doxorubicine, homoharringtonine en docetaxel. Eerst zetten ze hersentumorsferoïden en bloed-hersenbarrière-sferoïden in gewone platen bloot aan een breed dosisbereik om te achterhalen welke concentratie de helft van de cellen deed afsterven. Dat hielp hen doses te kiezen die schadelijk waren voor tumorcellen maar minder schadelijk voor de barrièrecellen zelf. Vervolgens lieten ze deze doses door het bovenste kanaal van de chip stromen, waardoor geneesmiddelen de barrière alleen konden passeren en de tumor konden bereiken als ze door de dichte cellaag heen konden dringen.
Wat het nieuwe platform onthult
De resultaten lieten zien dat zelfs wanneer geneesmiddelen duidelijk toxisch waren voor tumorcellen in standaard schaaltjes, de aanwezigheid van een intacte bloed-hersenbarrière op de chip hun effect sterk verminderde. Tumorsferoïden achter de barrière verloren veel minder cellen dan die direct in geneesmiddelengrens werden ondergedompeld, wat benadrukt hoe krachtig de barrière de daadwerkelijke medicijnblootstelling beperkt. Sommige middelen, zoals doxorubicine en homoharringtonine, maakten de barrière bovendien lekker bij concentraties ver onder die welke de barrièrecellen deden afsterven, waardoor er meer medicijn kon passeren maar ook een mogelijk risico voor gezond hersenweefsel ontstond. Belangrijk is dat tumoren van verschillende patiënten verschillend reageerden, wat het belang van gepersonaliseerd testen onderstreept.
Gepersonaliseerd testen van hersentumoren dichterbij brengen
Voor een niet-specialist is de kernboodschap dat het niet voldoende is dat een kankermiddel tumorcellen in een schaaltje doodt; het moet ook de beschermende wand van de hersenen passeren zonder te veel schade te veroorzaken. Deze studie introduceert een praktisch, schaalbaar instrument dat een realistische bloed-hersenbarrière en patiëntafgeleid tumorweefsel samenbrengt in één miniaturiseerd systeem. Omdat elke testunit slechts enkele honderden tumorcellen gebruikt, zouden dergelijke platforms op den duur panelen van geneesmiddelen en doses op de cellen van een kind kunnen testen vóór behandeling, zodat artsen opties kunnen kiezen die zowel effectiever als veiliger voor de hersenen zijn.
Bronvermelding: Wei, W., Stano, M., Kritzer, B. et al. A perfused, parallelized blood brain barrier-tumor platform for compound permeation and efficacy investigations. Microsyst Nanoeng 12, 175 (2026). https://doi.org/10.1038/s41378-026-01268-3
Trefwoorden: bloed-hersenbarrière, diffuse midline-glioma, organ on chip, hersen-tumormedicijnen, microfluïdisch platform