Clear Sky Science · de
Eine durchspülte, parallelisierte Blut‑Hirn‑Schranke‑Tumor‑Plattform zur Untersuchung von Wirkstoffdurchtritt und Wirksamkeit
Warum die Behandlung von Hirntumoren so schwierig ist
Moderne Krebsmedikamente haben das Überleben vieler Patientinnen und Patienten verbessert, doch Hirntumoren bleiben hartnäckig schwer zu behandeln. Ein wesentlicher Grund ist das körpereigene Sicherheitssystem des Gehirns, die Blut‑Hirn‑Schranke, die die meisten Substanzen am Eindringen ins Gehirn hindert. Diese Studie beschreibt ein im Labor gezüchtetes Modell, das eine realistische Gehirnschranke und patientenabgeleitetes Tumorgewebe zusammen auf einer miniaturisierten Kunststoffplattform vereint, damit Forschende besser sehen können, welche Medikamente tatsächlich Tumoren erreichen und wie gut sie dort wirken.
Eine winzige Schranke, die große Hoffnungen blockiert
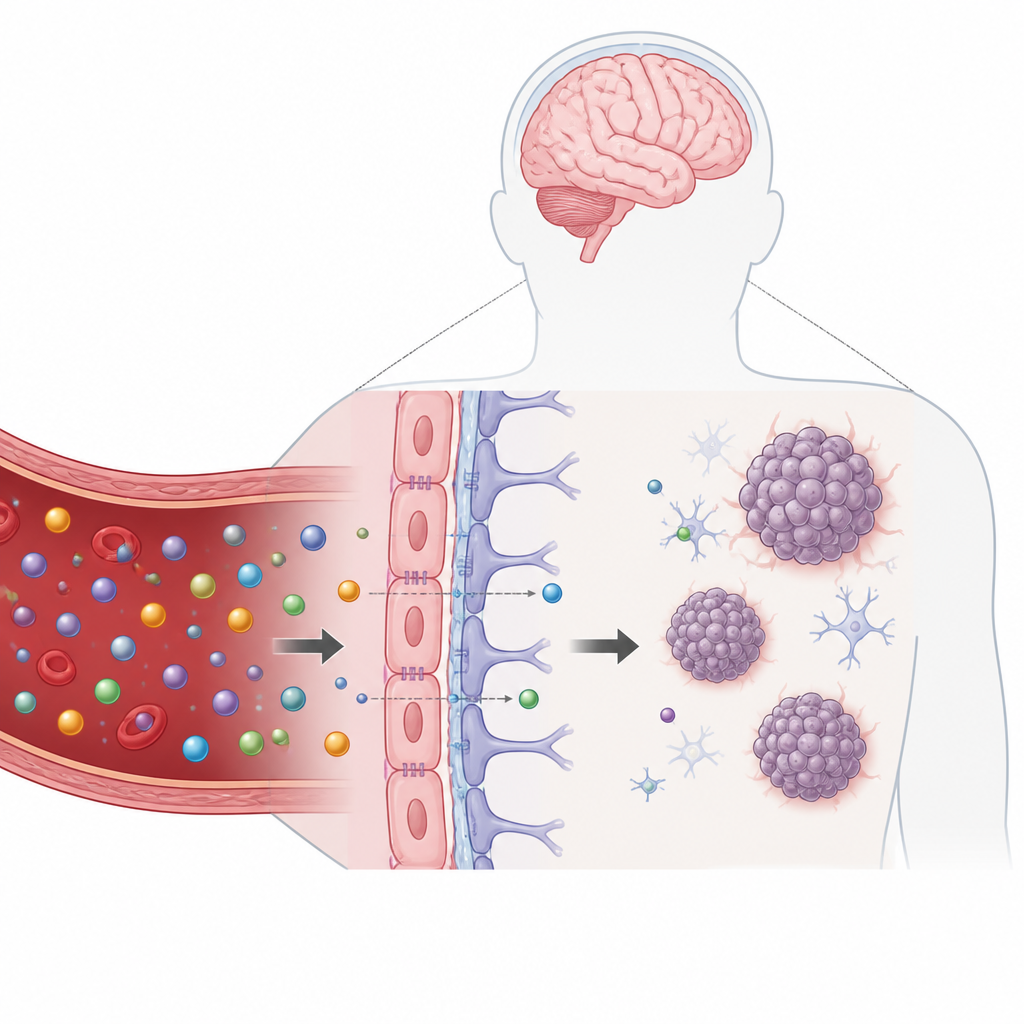
Die Blut‑Hirn‑Schranke ist eine dünne Zellschicht, die Blutgefäße im Gehirn auskleidet und streng kontrolliert, was aus dem Blut ins Gewebe gelangt. Zwar schützt sie das Gehirn vor Toxinen, sie hält aber auch viele hilfreiche Medikamente fern. Das ist besonders problematisch bei Kindern mit diffusem Mittellinien‑Gliom, einem aggressiven Tumor des Hirnstamms mit sehr schlechter Prognose. Bestehende flache Zellkulturen und selbst viele dreidimensionale Tumormodelle lassen häufig eine realistische Blut‑Hirn‑Schranke weg, wodurch Medikamente im Labor vielversprechender erscheinen, als sie bei Patientinnen und Patienten tatsächlich sind.
Aufbau einer Blut‑Hirn‑Schranke und eines Tumors auf einem Chip
Um diese Lücke zu schließen, bauten die Forschenden ein handtellergroßes Kunststoffgerät, das 32 miniaturisierte Testeinheiten in der Anordnung einer Standardplattenstruktur fasst. Jede Einheit enthält einen schmalen Kanal, der mit menschlichen Gefäßzellen ausgekleidet ist und von Hirnstützzellen, sogenannten Astrozyten und Perizyten, in einem weichen Gel darunter gestützt wird. Zusammen bilden sie ein kompaktes Modell der Blut‑Hirn‑Schranke. Direkt unterhalb dieser Schranke erzeugte das Team einen winzigen hängenden Tropfen, der eine einzelne kugelförmige Zellmasse aufnehmen kann, gewachsen aus Zellen, die von Kindern mit diffusem Mittellinien‑Gliom gespendet wurden. Dieser Tropfen bringt den Tumor sehr nahe an das künstliche Blutgefäß, ähnlich wie seine Lage im Hirnstamm.
Blutfluss ohne Pumpen simulieren
Im lebenden Gehirn sind Gefäßzellen ständigem Fluss und sanfter Reibung durch das Blut ausgesetzt, was zur Dichtigkeit der Schranke beiträgt. Um dies ohne sperrige Geräte nachzubilden, befestigte das Team seine Platte auf einer kippbaren Bühne in einem warmen Inkubator. Durch langsames Hin‑ und Herschaukeln der Platte erzeugten sie einen gravitationsgetriebenen Fluss der Nährlösung durch jeden Kanal, der die Gefäßzellen realistischen Scherkräften aussetzt. Computersimulationen und Messungen bestätigten, dass Fluss und mechanische Kräfte im Bereich dessen lagen, was in realen Hirngefäßen zu erwarten ist, und dass die Schranke gegenüber kleinen fluoreszenten Testmolekülen dicht blieb.
Echte Krebsmedikamente in realistischer Umgebung testen
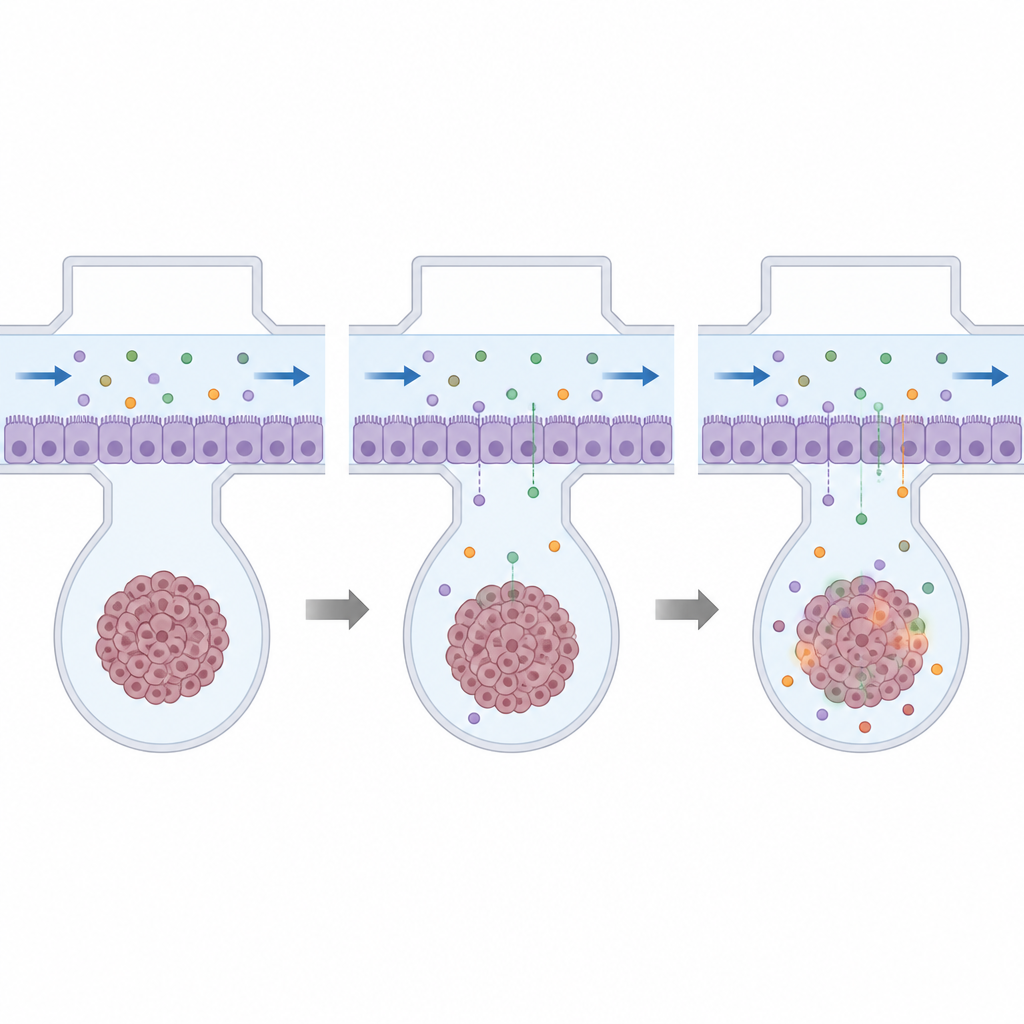
Mit der etablierten Plattform testeten die Forschenden vier bereits für andere Krebsarten zugelassene Chemotherapeutika: Cisplatin, Doxorubicin, Homoharringtonin und Docetaxel. Zunächst setzten sie Tumorsphäroide und Blut‑Hirn‑Schranken‑Sphäroide in Standardplatten einer breiten Dosisreihe aus, um die Dosis zu bestimmen, bei der jeweils die Hälfte der Zellen abstirbt. Das half, Dosen auszuwählen, die für die Tumorzellen schädlich, für die Schranke selbst aber weniger zerstörerisch sind. Anschließend ließen sie diese Dosen durch den oberen Kanal des Chips fließen, sodass Medikamente die Schranke überwinden mussten, um den Tumor zu erreichen — genau wie im Körper nur solche Wirkstoffe durchkommen, die die dichte Zellschicht permeieren können.
Was die neue Plattform enthüllt
Die Ergebnisse zeigten, dass selbst wenn Medikamente in Standardkulturen eindeutig toxisch für Tumorzellen waren, das Vorhandensein einer intakten Blut‑Hirn‑Schranke auf dem Chip ihre Wirkung deutlich abschwächte. Tumorsphäroide hinter der Schranke verloren weit weniger Zellen als solche, die direkt in Medikamentenlösung getaucht wurden, was die starke Begrenzung der tatsächlichen Arzneimittelexposition durch die Schranke unterstreicht. Manche Wirkstoffe, etwa Doxorubicin und Homoharringtonin, machten die Schranke bei Dosen undichten, die deutlich unter den zelltötenden Konzentrationen lagen — dadurch gelangte mehr Wirkstoff hindurch, was aber auch auf potenzielle Schäden im gesunden Hirngewebe hinweist. Wichtig ist auch, dass Tumoren verschiedener Patientinnen und Patienten unterschiedlich reagierten, was die Notwendigkeit personalisierter Tests betont.
Personalisierte Hirntumortests rücken näher
Für Nicht‑Fachleute lautet die Kernbotschaft: Es reicht nicht, dass ein Krebsmedikament Tumorzellen in einer Schale abtötet; es muss auch die Schutzwand des Gehirns überwinden, ohne dabei zuviel Schaden anzurichten. Diese Studie stellt ein praktikables, skalierbares Werkzeug vor, das eine realistische Blut‑Hirn‑Schranke und patientenabgeleitetes Tumorgewebe in einem miniaturisierten System vereint. Da jede Testeinheit nur wenige hundert Tumorzellen benötigt, könnten solche Plattformen eines Tages Panels von Medikamenten und Dosen an den Zellen eines Kindes testen, bevor die Behandlung beginnt — und so Ärzten helfen, Optionen zu wählen, die sowohl wirksamer als auch sicherer für das Gehirn sind.
Zitation: Wei, W., Stano, M., Kritzer, B. et al. A perfused, parallelized blood brain barrier-tumor platform for compound permeation and efficacy investigations. Microsyst Nanoeng 12, 175 (2026). https://doi.org/10.1038/s41378-026-01268-3
Schlüsselwörter: Blut‑Hirn‑Schranke, diffuses Mittellinien‑Gliom, Organ‑on‑Chip, Medikamente gegen Hirntumoren, mikrofluidische Plattform