Clear Sky Science · ru
Анализ тайм-лапс изображений выявляет зависимые от триггера различия в продолжительности жизни ASC-«спеков» в инфламмасоме NLRP3
Почему важны крошечные искры внутри иммунных клеток
Когда наш организм чувствует опасность — например кристаллы, вызывающие подагру, вторжение микробов или токсические вещества — иммунные клетки включают мощные сигнальные «тревожные» системы. Одна из таких систем, называемая инфламмасомой NLRP3, помогает запускать воспаление для борьбы с угрозой, но при чрезмерной активации может вызывать заболевания. В этом исследовании рассматриваются крошечные яркие точки, или «спеки», которые появляются внутри иммунных клеток при срабатывании этой сигнализации. Наблюдая за формированием и исчезновением этих спеков во времени, авторы показывают, что не все сигналы опасности вызывают одинаковый воспалительный ответ, что ставит под сомнение представление о системе как простой выключатель «вкл/выкл».
Ближе к внутренней «сигнализации» клетки
Инфламмасомы — это молекулярные комплексы, которые собираются внутри иммунных клеток при столкновении с вредными сигналами извне (например, бактериальными токсинами) или изнутри (такими как кристаллы мочевой кислоты). После сборки они активируют провоспалительные посредники и специфическую форму клеточной гибели — пироптоз. Одной из характерных черт этого процесса является появление одной или нескольких ярких точек, состоящих из белка ASC, которые собираются вместе с другими компонентами инфламмасомы. Традиционно ученые оценивали этот ответ с помощью конечных тестов на больших популяциях клеток — подсчитывая суммарное число спеков или воспалительных молекул в один момент времени — что затрудняло наблюдение за динамикой в отдельной клетке на протяжении часов.
Наблюдение за спеками вживую, по одной клетке
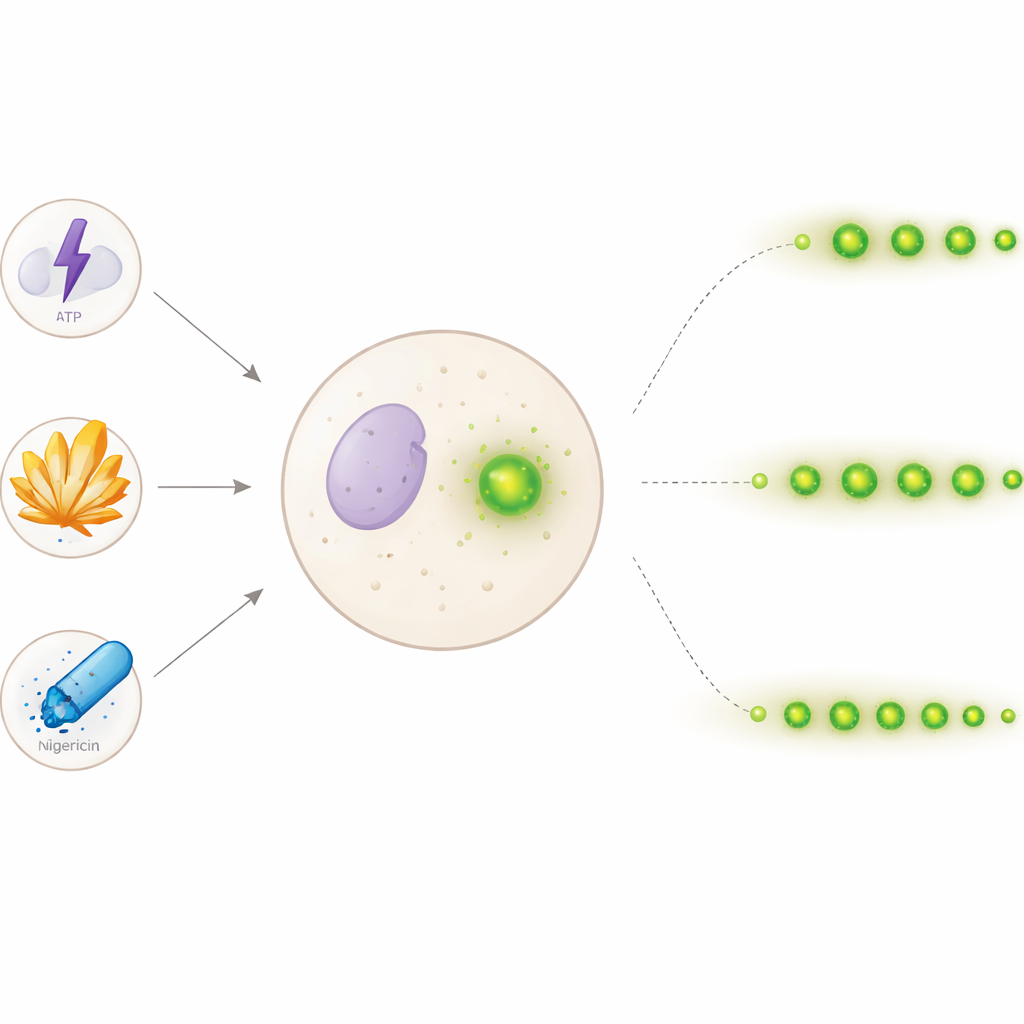
Чтобы получить более детальное представление, команда использовала человеческие клетки, подобные иммунным, генетически модифицированные так, что ASC светится зеленым под микроскопом. После «прайминга» клеток они индуцировали сборку инфламмасомы тремя распространенными стимуляторами: АТФ (сигнальная молекула), острые кристаллы мононатриевой ураты (связанные с подагрой) и ионофор нигерицин (часто используемый в лабораторных исследованиях). Затем они снимали изображения каждые 30 минут в течение 24 часов. Имея тысячи изображений, исследователи построили поэтапный компьютерный алгоритм, который автоматически находил круглые яркие спеки и отслеживал каждый из них — как он появляется, немного смещается, бледнеет или исчезает. Сравнивая каждый спек на последовательных кадрах и используя адаптивный поиск при ослаблении сигнала, программа могла оценивать, как долго отдельные спеки оставались видимыми — их «время жизни».
Простые алгоритмы выявляют сложное поведение
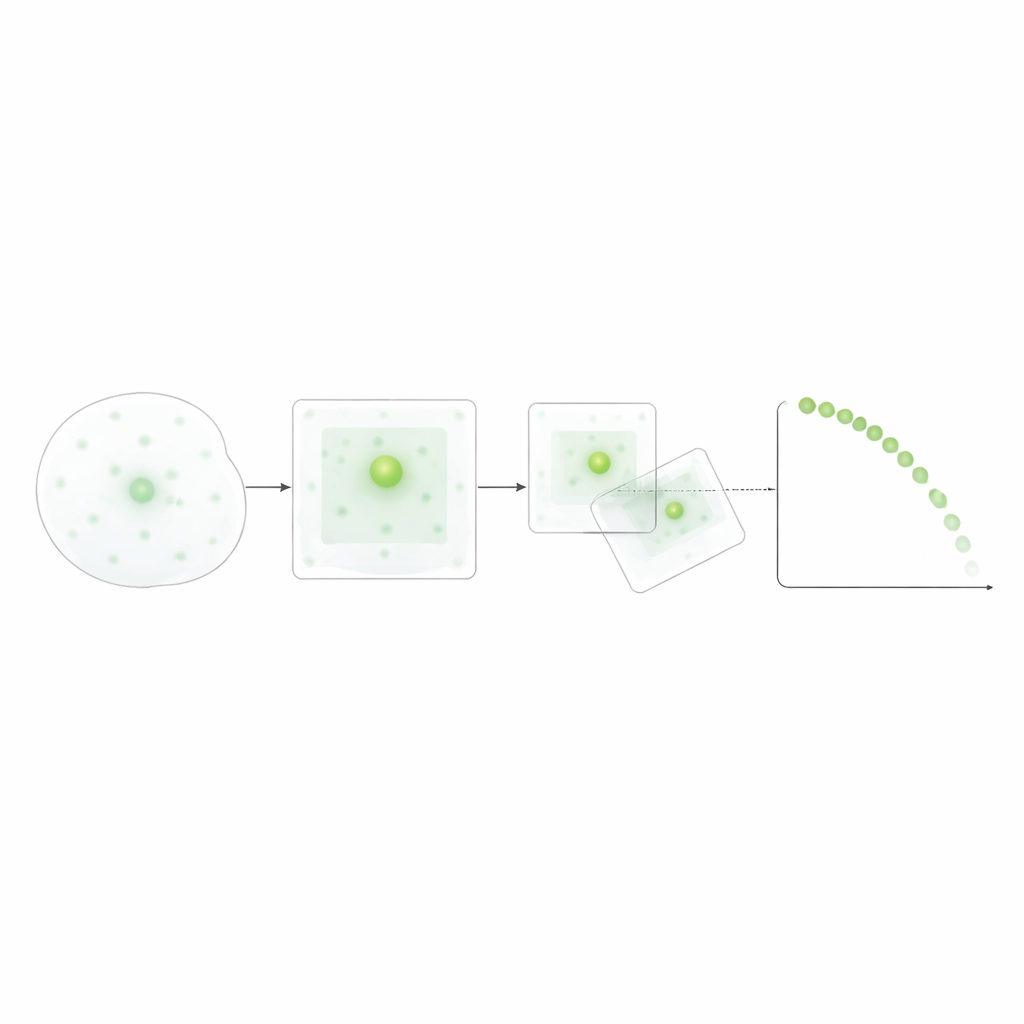
Вместо опоры на ресурсоемкое глубокое обучение исследователи разработали прозрачный, основанный на правилах метод: пороговая обработка изображения, очистка с помощью базовых фильтров и отслеживание ближайшего соседнего спека между кадрами в пределах реалистичного диапазона перемещений. Они донастраивали пороги яркости и пределы движения с помощью ручных измерений, чтобы автоматический подсчет соответствовал человеческой оценке. После валидации такой подход позволил объединить данные по многим полям зрения и экспериментам, получив распределения времён жизни спеков и времени их образования для каждого триггера. Невысокие требования к объему данных делают метод практичным для стандартных лабораторий, при этом он позволяет захватывать динамику спеков на уровне отдельных клеток.
Разные триггеры — разные времена жизни спеков
Оказалось, что продолжительность жизни этих спеков сильно зависит от способа активации инфламмасомы. АТФ вызывал множество короткоживущих спеков, большинство из которых быстро исчезало. В то же время уратные кристаллы и нигерицин приводили к более долгоживущим спекам, причем нигерицин также стимулировал образование большего общего числа спеков. Статистические тесты распределений времени жизни и графики в стиле анализа выживаемости подтвердили, что каждый триггер формирует характерный паттерн: быстро возникающие, короткоживущие спеки при воздействии АТФ; более медленно и непрерывно формирующиеся, долгоживущие спеки при уратных кристаллах; и быстро формирующиеся, долгоживущие спеки при нигерицине. Интересно, что время появления спека не всегда предсказывало, как долго он продержится, что говорит о том, что длительность жизни определяется скорее природой триггера, чем моментом появления.
Что эти крошечные спеки могут значить для здоровья
Исследование показывает, что спеки, обозначающие активность инфламмасомы, не все одинаковы: их число и длительность существования зависят от типа сигнала опасности. Это означает, что один и тот же молекулярный «тревожный механизм» может настраиваться по-разному в ответ на АТФ, кристаллы или ионофоры, потенциально приводя к различным воспалительным исходам в здоровье и при болезни. Не менее важно то, что работа демонстрирует: аккуратная тайм-лапс визуализация в сочетании с простой аналитической схемой может раскрыть это скрытое разнообразие без необходимости в огромных наборах данных или сложном искусственном интеллекте. В перспективе понимание связи между временем жизни спеков и полезным или вредным воспалением может помочь уточнить терапевтические подходы при таких состояниях, как подагра, хронические воспалительные и аутоиммунные заболевания.
Цитирование: Herring, M., Persson, A., Karlsson, R. et al. Time-lapse image analysis reveals trigger-dependent differences in ASC speck lifetime in the NLRP3 inflammasome. Sci Rep 16, 14173 (2026). https://doi.org/10.1038/s41598-026-50936-x
Ключевые слова: инфламмасома, ASC-спек, одноклеточная визуализация, воспаление, гибель клетки