Clear Sky Science · pl
Analiza obrazów w czasie ujawnia zależne od bodźca różnice w czasie trwania „specków” ASC w inflammasomie NLRP3
Dlaczego drobne iskry wewnątrz komórek odpornościowych mają znaczenie
Gdy organizm wykryje zagrożenie — np. kryształy powodujące dnę, inwazyjne mikroby lub toksyczne związki — komórki odpornościowe uruchamiają potężne systemy alarmowe. Jeden z tych systemów, zwany inflammasomem NLRP3, pomaga zapoczątkować stan zapalny w walce z zagrożeniami, ale jego nadmierna aktywność może też prowadzić do chorób. W tym badaniu analizowano drobne, jasne punkty, czyli „specki”, które pojawiają się w komórkach odpornościowych po uruchomieniu tego alarmu. Obserwując, jak specki powstają i znikają w czasie, badacze pokazują, że różne sygnały nie wywołują takiego samego rodzaju odpowiedzi zapalnej, co podważa pogląd o tym systemie jako prostym włączniku on–off.
Bliższe spojrzenie na wewnętrzny alarm komórki
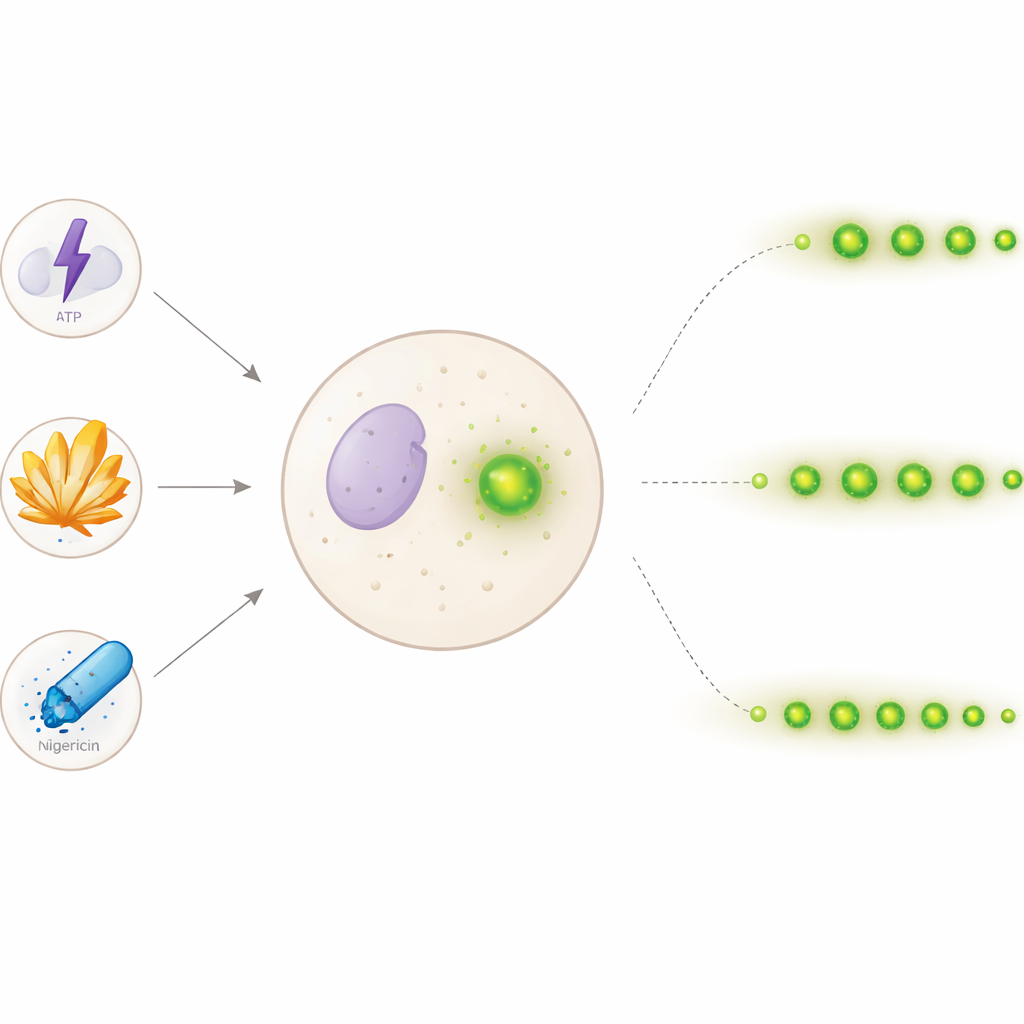
Inflammasomy to molekularne maszyny, które składają się w komórkach odpornościowych po wykryciu szkodliwych sygnałów z zewnątrz (np. toksyn bakteryjnych) lub wewnątrz organizmu (takich jak kryształy kwasu moczowego). Po zmontowaniu aktywują mediatory zapalenia oraz gwałtowną formę śmierci komórki zwaną pyroptozą. Charakterystycznym objawem tego procesu jest pojawienie się jednego lub kilku jasnych specków z białka ASC, które skupiają się razem z innymi elementami inflammasomu. Tradycyjnie reakcję tę mierzy się testami punktowymi na dużych populacjach komórek — zliczając całkowitą liczbę specków lub cząsteczek zapalnych w jednym czasie — co utrudnia obserwację tego, co dzieje się w pojedynczej komórce przez godziny.
Obserwacja specków na żywo, komórka po komórce
Aby uzyskać bardziej szczegółowy obraz, zespół użył ludzkich komórek podobnych do odpornościowych, zmodyfikowanych tak, by ASC świecił na zielono pod mikroskopem. Po „primingu” komórek wywołali składanie się inflammasomu trzema powszechnymi bodźcami: ATP (cząsteczka sygnałowa), ostrymi kryształami moczanu sodu (powiązanymi z dną) oraz nośnikiem jonów nigericyną (często stosowaną w badaniach laboratoryjnych). Następnie rejestrowali obrazy co 30 minut przez 24 godziny. Dysponując tysiącami obrazów, zbudowali krokowy algorytm komputerowy, który automatycznie wykrywał okrągłe, jasne specki i śledził każdy z nich, gdy się pojawiał, przesuwał nieznacznie, bledł lub znikał. Porównując każdy speck w jednym obrazie z kolejnym i stosując adaptacyjne wyszukiwanie, gdy sygnały słabły, program mógł oszacować, jak długo poszczególne specki pozostawały widoczne — ich „czas życia”.
Proste algorytmy ujawniają złożone zachowanie
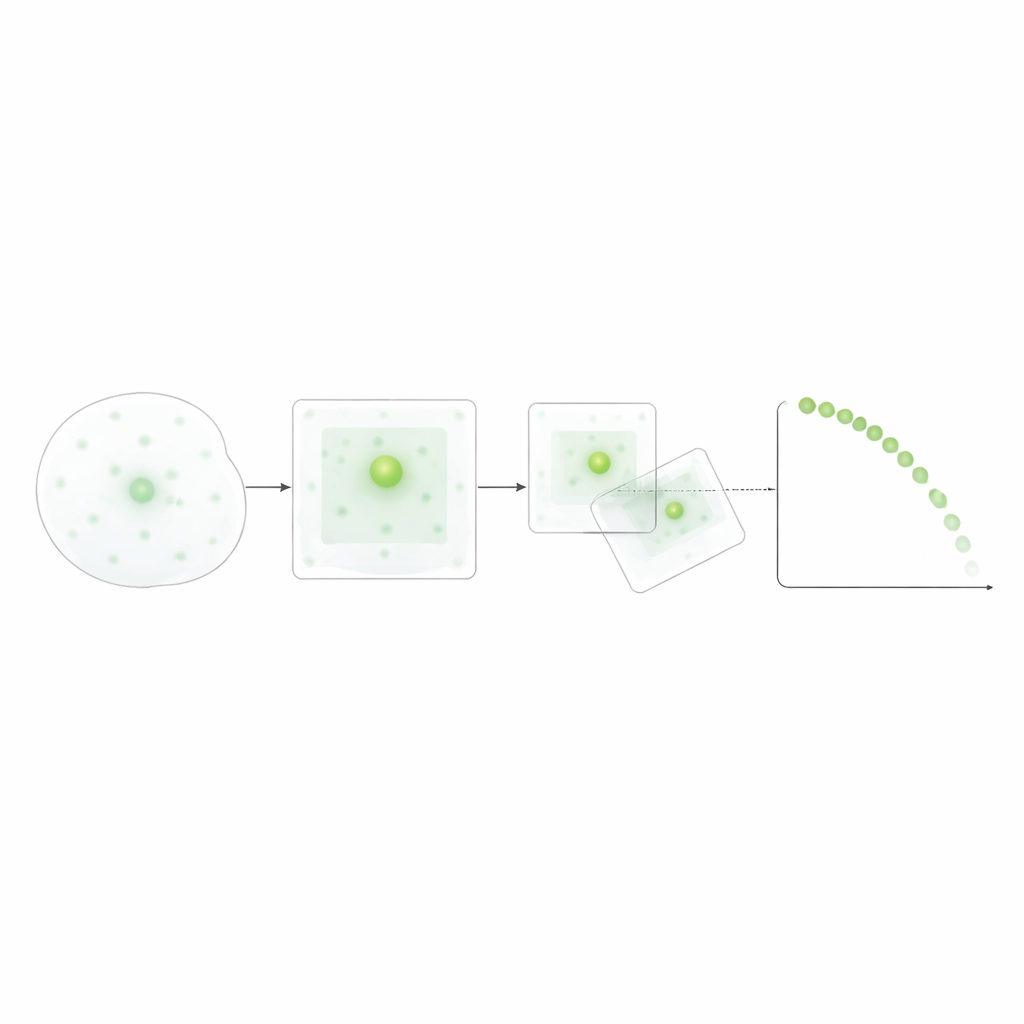
Zamiast polegać na wymagającym danych głębokim uczeniu, badacze zaprojektowali przejrzystą, regułową metodę: progowanie obrazu, oczyszczanie go podstawowymi filtrami i śledzenie najbliższego sąsiadującego specka między klatkami w realistycznym zakresie ruchu. Dostosowali progi jasności i limity ruchu za pomocą pomiarów ręcznych, aby upewnić się, że automatyczne zliczenia odpowiadają ocenie ludzkiej. Po walidacji podejście to pozwoliło na łączenie danych z wielu pól widzenia i eksperymentów, dając rozkłady czasów życia specków i czasów ich powstawania dla każdego bodźca. Stosunkowo niewielkie wymagania dotyczące danych sprawiają, że metoda jest praktyczna w typowych laboratoriach, jednocześnie rejestrując dynamiczny taniec specków na poziomie pojedynczych komórek.
Różne bodźce, różne czasy życia specków
Czasy życia tych specków okazały się w dużej mierze zależne od rodzaju wyzwalacza inflammasomu. ATP powodowało powstawanie wielu krótkotrwałych specków, które w większości szybko znikały. W przeciwieństwie do tego kryształy moczanu i nigericyna prowadziły do powstawania specków o dłuższym czasie trwania, przy czym nigericyna powodowała też większą łączną liczbę specków. Testy statystyczne rozkładów czasów życia i krzywych typu „survival” potwierdziły, że każdy bodziec generował odrębny wzorzec: szybko powstające, krócej żyjące specki dla ATP; powoli i ciągłe powstawanie dłużej utrzymujących się specków dla kryształów moczanu; oraz szybko powstające, długo żyjące specki dla nigericyny. Co ciekawe, czas powstawania specków nie przewidywał wyraźnie, jak długo będą trwać, co sugeruje, że czas życia kształtuje bardziej natura bodźca niż moment pojawienia się specka.
Co te drobne specki mogą oznaczać dla zdrowia
Badanie pokazuje, że specki oznaczające aktywność inflammasomu nie są sobie równe; ich liczba i czas trwania zmieniają się w zależności od rodzaju sygnału zagrożenia. To sugeruje, że ten sam molekularny alarm może być dostrojony do odmiennej odpowiedzi na ATP, kryształy czy jono- przenośniki, co może prowadzić do różnych konsekwencji zapalnych w zdrowiu i chorobie. Równie ważne jest to, że praca demonstruje, iż staranna mikroskopia czasowa wraz z prostym pipeline’em analitycznym może ujawnić tę ukrytą różnorodność bez potrzeby ogromnych zbiorów danych czy skomplikowanej sztucznej inteligencji. W dłuższej perspektywie zrozumienie, jak czasy życia specków łączą się z korzystnym lub szkodliwym zapaleniem, może pomóc udoskonalić terapie dla schorzeń od dny po przewlekłe choroby zapalne i autoimmunologiczne.
Cytowanie: Herring, M., Persson, A., Karlsson, R. et al. Time-lapse image analysis reveals trigger-dependent differences in ASC speck lifetime in the NLRP3 inflammasome. Sci Rep 16, 14173 (2026). https://doi.org/10.1038/s41598-026-50936-x
Słowa kluczowe: inflammasom, speck ASC, mikroskopia pojedynczych komórek, zapalenie, śmierć komórki