Clear Sky Science · de
Time‑lapse‑Bildanalyse enthüllt auslöserspezifische Unterschiede in der Lebensdauer von ASC‑Specks im NLRP3‑Inflammasom
Warum winzige Funken innerhalb von Immunzellen wichtig sind
Wenn unser Körper Gefahr wahrnimmt — etwa Kristalle, die Gicht auslösen, eindringende Mikroben oder giftige Verbindungen — schalten Immunzellen kräftige Alarmsysteme ein. Eines dieser Systeme, das NLRP3‑Inflammasom, initiiert Entzündungen zur Abwehr der Bedrohung, kann aber bei Überaktivität auch Krankheiten antreiben. Diese Studie betrachtet winzige helle Punkte, sogenannte „Specks“, die in Immunzellen auftreten, wenn dieser Alarm ausgelöst wird. Indem die Forschenden beobachten, wie diese Specks im Laufe der Zeit entstehen und verschwinden, zeigen sie, dass nicht alle Gefahrensignale dieselbe Art von Entzündungsantwort hervorrufen — und stellen damit die Vorstellung infrage, dass dieses System wie ein einfacher Ein‑/Aus‑Schalter funktioniert.
Ein genauerer Blick auf den inneren Alarm der Zelle
Inflammasome sind molekulare Maschinen, die sich in Immunzellen zusammenlagern, wenn sie schädliche Signale von außen (z. B. bakterielle Toxine) oder innen (wie Harnsäurekristalle) wahrnehmen. Nach der Assemblierung aktivieren sie Entzündungsbotenstoffe und eine feurige Form des Zelltods namens Pyroptose. Kennzeichen dieses Prozesses ist das Auftreten eines oder mehrerer heller Specks aus dem Protein ASC, die mit anderen Inflammasom‑Bauteilen zusammenklumpen. Traditionell messen Forschende diese Antwort mit Endpunkttests an großen Zellpopulationen — sie zählen Specks oder entzündliche Moleküle zu einem einzigen Zeitpunkt — wodurch es schwerfällt, das Geschehen in einzelnen Zellen über Stunden hinweg nachzuvollziehen.
Specks live beobachten, Zelle für Zelle
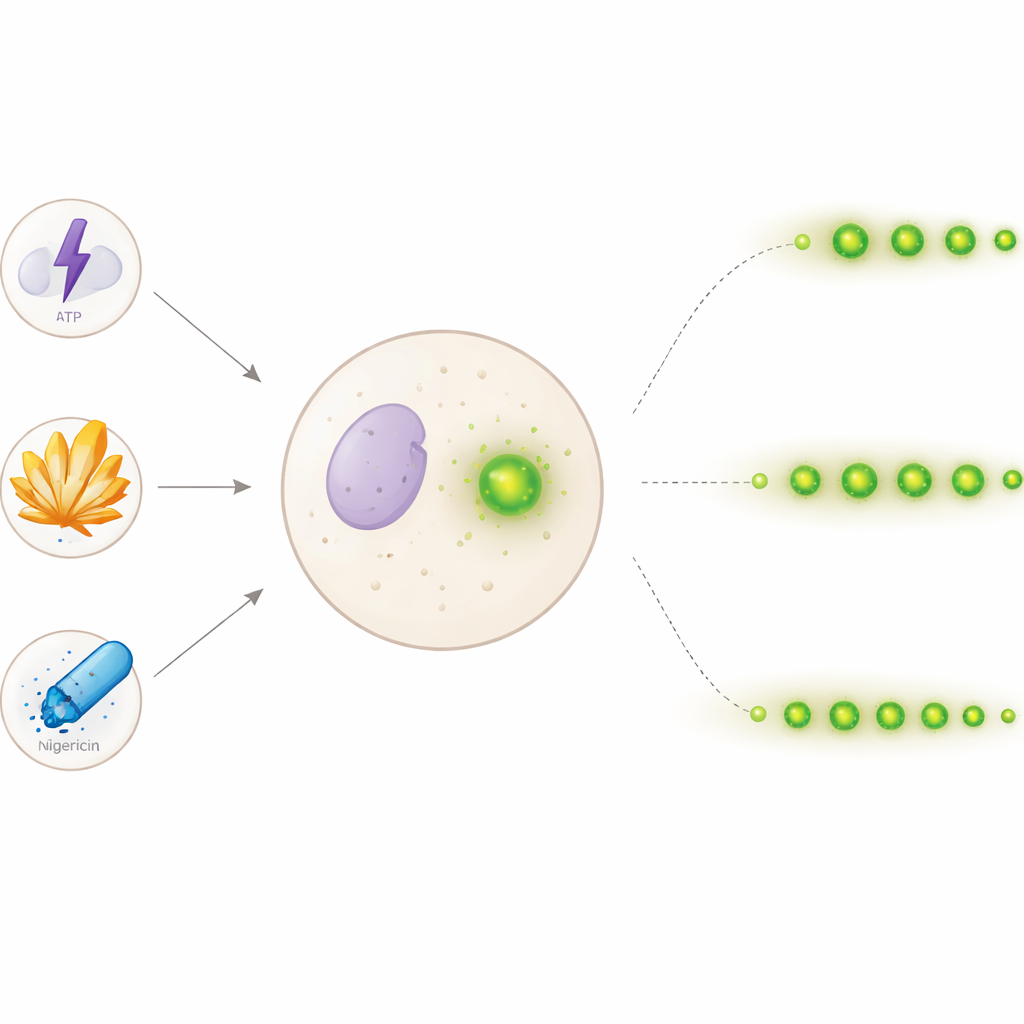
Um ein detaillierteres Bild zu erhalten, verwendete das Team menschliche, immunähnliche Zellen, die so verändert wurden, dass ASC unter dem Mikroskop grün leuchtet. Nach einer „Priming“-Behandlung lösten sie die Assemblierung des Inflammasoms mit drei gängigen Stimuli aus: ATP (ein Signalmolekül), scharfe Mononatriumurat‑Kristalle (mit Gicht assoziiert) und der Ionentransporter Nigericin (häufig in Laborstudien verwendet). Anschließend nahmen sie alle 30 Minuten über 24 Stunden Bilder auf. Mit Tausenden von Aufnahmen entwickelten sie einen schrittweisen Computeralgorithmus, der automatisch runde, helle Specks erkennt und jedes einzelne verfolgt, während es erscheint, sich leicht bewegt, verblasst oder verschwindet. Indem jeder Speck im Bild mit dem nächsten verglichen und bei Abnahme des Signals eine adaptive Suche eingesetzt wurde, konnte das Programm abschätzen, wie lange einzelne Specks sichtbar bleiben — ihre „Lebensdauer“.
Einfache Algorithmen offenbaren komplexes Verhalten
Statt auf datenintensives Deep Learning zu setzen, entwarfen die Forschenden eine transparente, regelbasierte Methode: Bildschwellen setzen, mit einfachen Filtern bereinigen und zwischen den Frames den nächstgelegenen Speck innerhalb eines realistischen Bewegungsbereichs verfolgen. Sie feinabgestimmten die Helligkeitsschwellen und Bewegungsgrenzen mithilfe manueller Messungen, um sicherzustellen, dass die automatisierten Zählungen mit menschlicher Einschätzung übereinstimmen. Nach der Validierung ermöglichte dieser Ansatz das Zusammenführen von Daten über viele mikroskopische Felder und Experimente hinweg und lieferte Verteilungen der Speck‑Lebensdauern und Entstehungszeiten für jeden Auslöser. Dieser vergleichsweise moderate Datenbedarf macht die Methode für Standardlaborumgebungen praktikabel, während sie dennoch die dynamische Entwicklung der Specks auf Einzelzellebene einfängt.
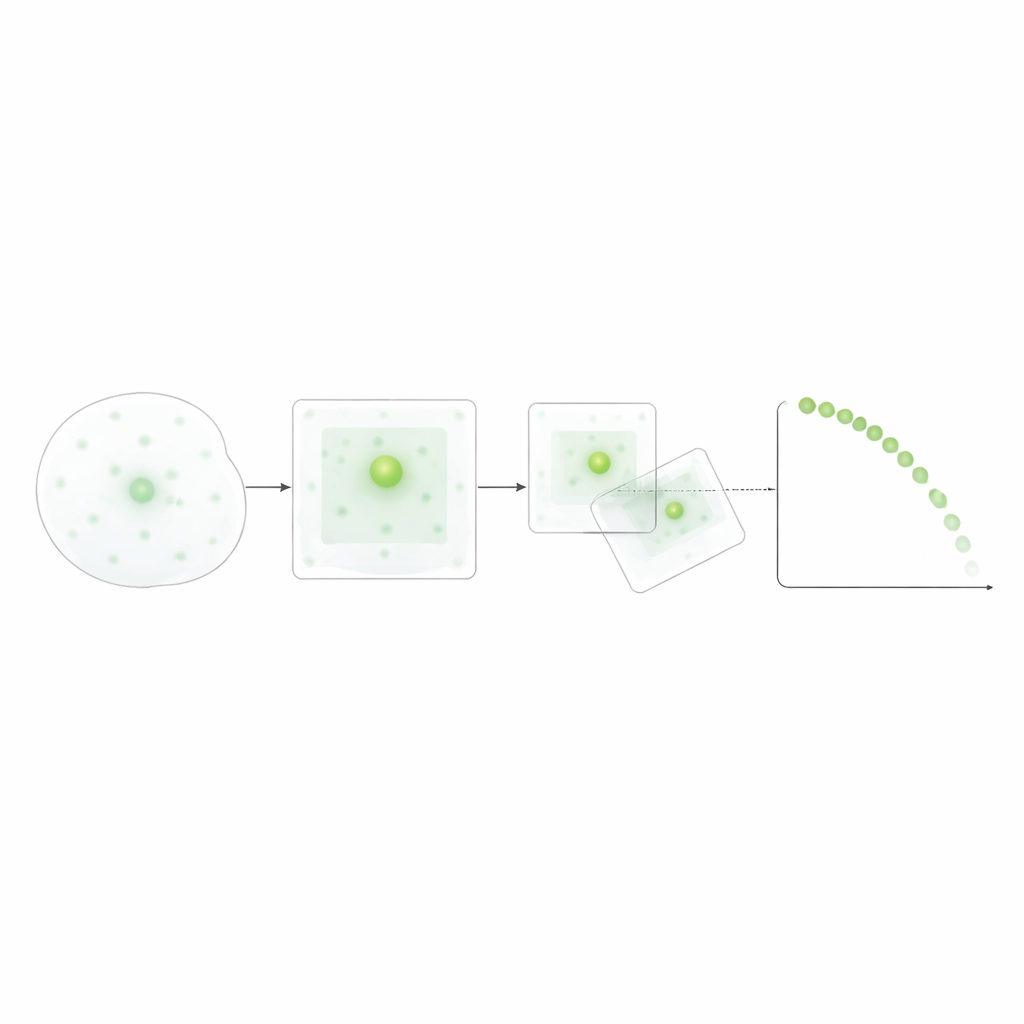
Unterschiedliche Auslöser, unterschiedliche Speck‑Lebensdauern
Die Lebensdauer dieser Specks hing stark davon ab, wie das Inflammasom ausgelöst wurde. ATP erzeugte viele kurzlebige Specks, von denen die meisten rasch verschwanden. Im Gegensatz dazu führten Uratkristalle und Nigericin zu länger anhaltenden Specks; zudem förderte Nigericin die Bildung einer insgesamt größeren Anzahl von Specks. Statistische Tests an Lebensdauerverteilungen und Überlebenskurven bestätigten, dass jeder Auslöser ein charakteristisches Muster erzeugte: bei ATP schnell entstehende, kurzlebige Specks; bei Uratkristallen langsamer und kontinuierlich entstehende, länger anhaltende Specks; und bei Nigericin schnell entstehende, langlebige Specks. Interessanterweise sagte der Zeitpunkt der Speckentstehung nicht klar vorher, wie lange sie bestehen würden, was darauf hindeutet, dass die Lebensdauer eher durch die Art des Auslösers als durch den Entstehungszeitpunkt geprägt wird.
Was diese winzigen Specks für die Gesundheit bedeuten könnten
Die Studie zeigt, dass die Specks, die Inflammasom‑Aktivität markieren, nicht alle gleich sind: Anzahl und Persistenz variieren je nach Art des Gefahrensignals. Das legt nahe, dass derselbe molekulare Alarm unterschiedlich auf ATP, Kristalle oder Ionophore abgestimmt werden kann und so zu unterschiedlichen entzündlichen Ergebnissen in Gesundheit und Krankheit führt. Ebenso wichtig ist, dass die Arbeit demonstriert, dass sorgfältige Zeitraffer‑Bildgebung kombiniert mit einer einfachen Analyse‑Pipeline diese verborgene Vielfalt ohne riesige Datensätze oder komplexe künstliche Intelligenz aufdecken kann. Langfristig könnte das Verständnis, wie Speck‑Lebensdauern mit nützlicher versus schädlicher Entzündung zusammenhängen, helfen, Therapien für Erkrankungen von Gicht bis zu chronischen entzündlichen und Autoimmunerkrankungen zu verfeinern.
Zitation: Herring, M., Persson, A., Karlsson, R. et al. Time-lapse image analysis reveals trigger-dependent differences in ASC speck lifetime in the NLRP3 inflammasome. Sci Rep 16, 14173 (2026). https://doi.org/10.1038/s41598-026-50936-x
Schlüsselwörter: Inflammasom, ASC‑Speck, Einzelzell‑Bildgebung, Entzündung, Zelltod