Clear Sky Science · nl
Tijdverloopbeeldanalyse onthult trigger-afhankelijke verschillen in ASC-specklevensduur in het NLRP3-inflammasoom
Waarom kleine vonken binnen immuuncellen ertoe doen
Wanneer ons lichaam gevaar detecteert—zoals kristallen die jicht veroorzaken, binnendringende microben of giftige stoffen—zetten immuuncellen krachtige alarmsystemen aan. Eén van deze systemen, het NLRP3-inflammasoom, helpt ontsteking op te roepen om bedreigingen te bestrijden maar kan bij overactiviteit ook ziekte bevorderen. Deze studie onderzoekt kleine felle stippen, of "specks", die in immuuncellen verschijnen wanneer dit alarm wordt geactiveerd. Door te observeren hoe deze specks zich vormen en verdwijnen in de tijd, laten de onderzoekers zien dat niet alle gevaarsignalen hetzelfde soort ontstekingsrespons oproepen, wat de veronderstelling uitdaagt dat dit systeem als een eenvoudige aan/uit-schakelaar werkt.
Een nadere blik op het interne alarm van de cel
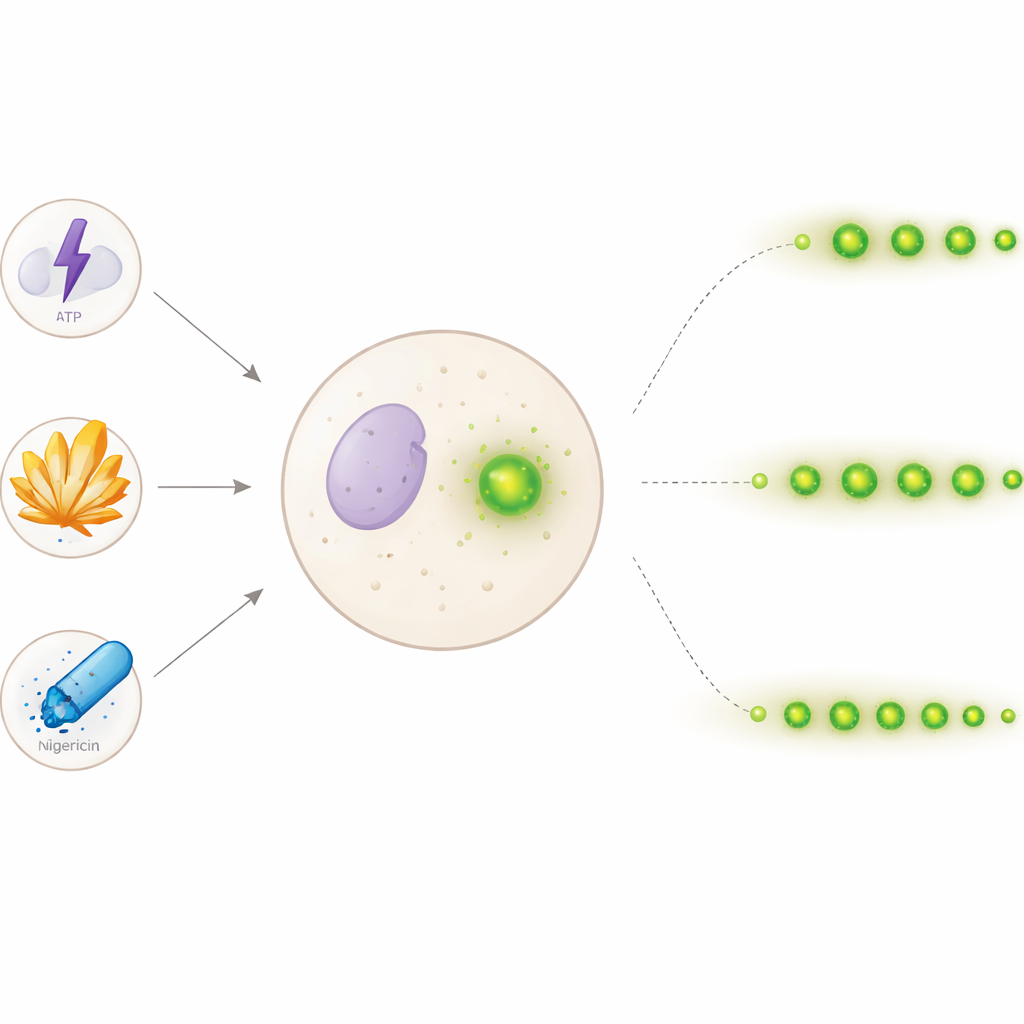
Inflammasomen zijn moleculaire machines die zich in immuuncellen assembleren wanneer ze schadelijke signalen van buiten het lichaam (zoals bacteriële toxines) of van binnen (zoals urinezuurkristallen) tegenkomen. Eenmaal samengesteld activeren ze ontstekingsboodschappers en een brandachtige vorm van celdood genaamd pyroptose. Een kenmerk van dit proces is het verschijnen van een of meer felle specks opgebouwd uit een eiwit genaamd ASC, die samenklonteren met andere inflammasoomcomponenten. Traditioneel meten wetenschappers deze respons met eindpunttests op grote celpopulaties—het tellen van totale specks of ontstekingsmoleculen op één tijdstip—waardoor moeilijk te zien is wat er in een individuele cel over uren gebeurt.
Specks live volgen, cel voor cel
Om een gedetailleerder beeld te krijgen gebruikten de onderzoekers mensachtige immuuncellen die zodanig waren gemodificeerd dat ASC groen oplicht onder de microscoop. Na het "primen" van de cellen activeerden ze de assemblage van het inflammasoom met drie veelvoorkomende stimuli: ATP (een signaalmolecuul), scherpe monosodiumuraatkristallen (geassocieerd met jicht) en de ionendrager nigericine (vaak gebruikt in laboratoriumstudies). Vervolgens namen ze elke 30 minuten beelden op gedurende 24 uur. Met duizenden beelden bouwden ze een stap-voor-stap computeralgoritme dat automatisch ronde, felle specks kon herkennen en elk ervan kon volgen terwijl het verscheen, licht bewoog, vervaagde of verdween. Door elke speck in een beeld met die in het volgende te vergelijken, en een adaptieve zoekstrategie te gebruiken wanneer signalen zwakker werden, kon het programma inschatten hoe lang individuele specks zichtbaar bleven—hun "levensduur".
Eenvoudige algoritmen onthullen complex gedrag
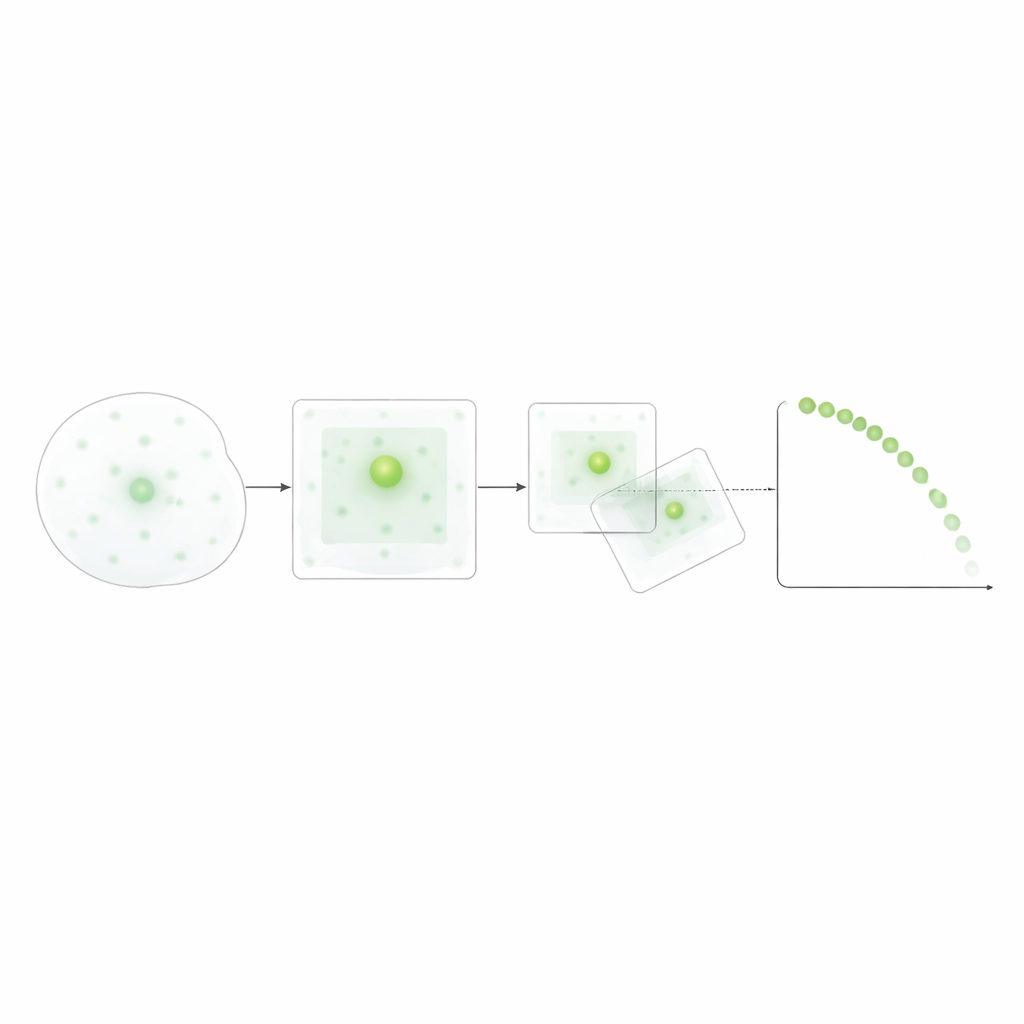
In plaats van te vertrouwen op data-intensieve deep learning, ontwierpen de onderzoekers een transparante, regelgebaseerde methode: drempelen van het beeld, schoonmaken met basale filters en het volgen van de dichtstbijzijnde naburige speck tussen frames binnen een realistisch bewegingsbereik. Ze verfijnden de helderheidsdrempels en bewegingslimieten met handmatige metingen om ervoor te zorgen dat de geautomatiseerde tellingen overeenkwamen met menselijke beoordeling. Eenmaal gevalideerd maakte deze aanpak het mogelijk gegevens over veel microscopische velden en experimenten samen te voegen, wat distributies van specklevensduren en vormingstijden voor elke trigger opleverde. Deze relatief bescheiden data-eis maakt de methode praktisch voor standaard laboratoriumopstellingen, terwijl ze toch de dynamische dans van specks op single-cell resolutie vastlegt.
Verschillende triggers, verschillende specklevensduren
De levensduren van deze specks bleken sterk afhankelijk van de manier waarop het inflammasoom werd geactiveerd. ATP produceerde veel kortlevende specks, waarvan de meeste snel verdwenen. Daarentegen leidden uraatkristallen en nigericine tot langer aanhoudende specks, en nigericine stimuleerde bovendien de vorming van een groter totaal aantal specks. Statistische toetsen op levensduurdistributies en survival-achtige curves bevestigden dat elke trigger een onderscheidend patroon opleverde: snel gevormde, kortlevende specks voor ATP; langzamer en continu gevormde, langer aanhoudende specks voor uraatkristallen; en snel gevormde, langlevende specks voor nigericine. Interessant was dat het tijdstip waarop specks vormden niet duidelijk voorspelde hoe lang ze zouden blijven bestaan, wat suggereert dat de levensduur meer wordt bepaald door de aard van de trigger dan door het moment van verschijnen.
Wat deze kleine specks voor de gezondheid kunnen betekenen
De studie toont aan dat de specks die inflammasoomactiviteit markeren niet allemaal gelijk zijn; hun aantal en hoe lang ze aanhouden variëren met het type gevaarsignaal. Dit impliceert dat hetzelfde moleculaire alarm anders kan worden afgestemd op ATP, kristallen of ionoforen, wat mogelijk leidt tot uiteenlopende ontstekingsuitkomsten bij gezondheid en ziekte. Even belangrijk laat het werk zien dat zorgvuldige time-lapse beeldvorming gecombineerd met een eenvoudige analyseketen deze verborgen diversiteit kan onthullen zonder enorme datasets of complexe kunstmatige intelligentie. Op de lange termijn kan begrip van hoe specklevensduren samenhangen met gunstige versus schadelijke ontsteking helpen bij het verfijnen van therapieën voor aandoeningen variërend van jicht tot chronische ontstekings- en auto-immuunziekten.
Bronvermelding: Herring, M., Persson, A., Karlsson, R. et al. Time-lapse image analysis reveals trigger-dependent differences in ASC speck lifetime in the NLRP3 inflammasome. Sci Rep 16, 14173 (2026). https://doi.org/10.1038/s41598-026-50936-x
Trefwoorden: inflammasoom, ASC-speck, single-cell beeldvorming, ontsteking, celdood