Clear Sky Science · ru
Экспериментальные и теоретические данные об ингибирующих свойствах молекул политиофена и полипиррола для защиты мягкой стали от коррозии в серной кислоте
Почему важно защищать повседневную сталь
От мостов и автомобилей до заводских труб — значительная часть современной инфраструктуры зависит от мягкой стали. Однако этот распространённый металл постепенно растворяется при контакте с агрессивными кислотами, используемыми для очистки и в производстве. Исследование, лежащее в основе этой статьи, изучает, как два специальных пластоподобных материала — политиеофен и полипиррол — могут словно молекулярный дождевик покрыть сталь и помешать ей разрушаться в серной кислоте, широко применяемом промышленном химическом веществе.
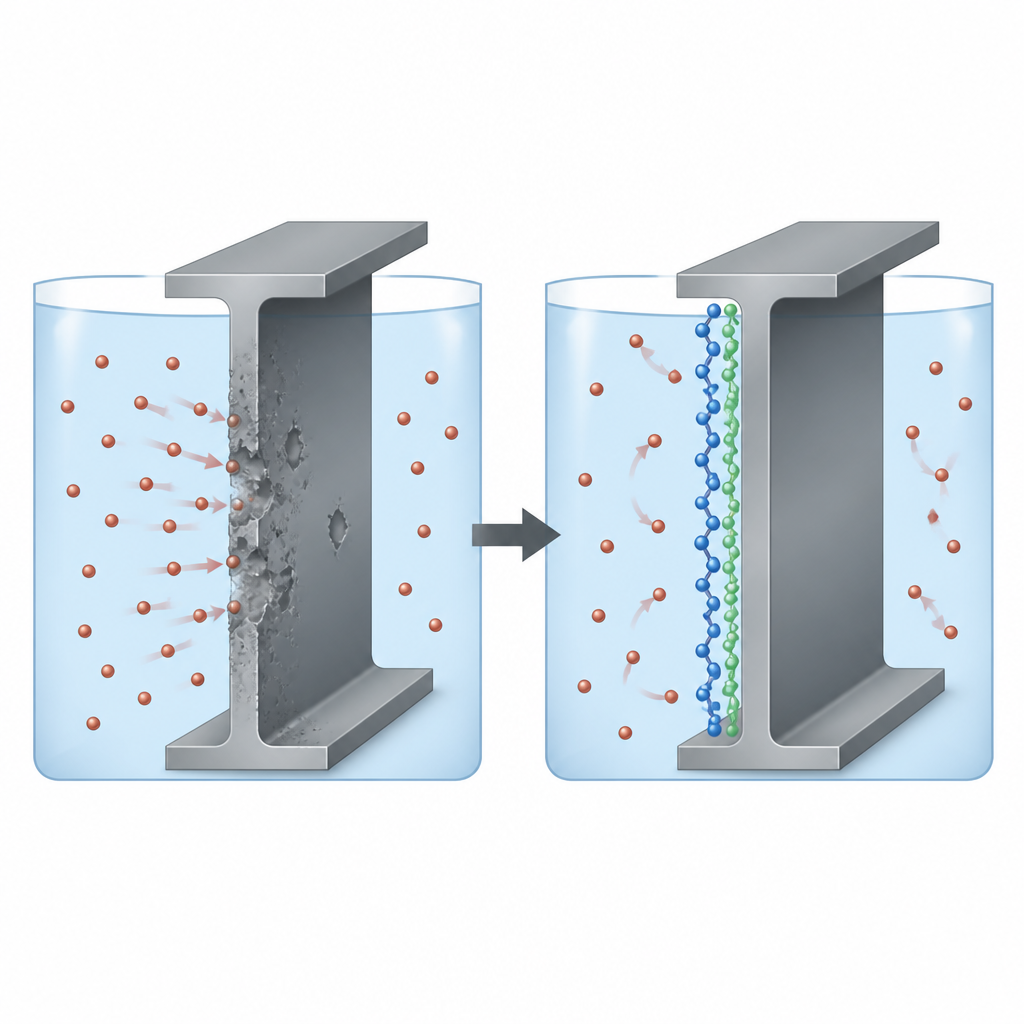
Атака на сталь в кислотных растворах
В многих отраслях серная кислота необходима для очистки, травления и обработки стальных деталей, но она также агрессивно разрушает поверхность металла. Инженеры часто добавляют в кислоту «ингибиторы коррозии», чтобы замедлить этот процесс. Авторы сосредоточились на двух электрически проводящих полимерах — политиеофене и полипирроле — выбранных потому, что их цепочечные структуры несут облака подвижных электронов и реактивных атомов, которые могут прочно цепляться за сталь. Ключевой вопрос заключался в том, способны ли эти полимеры сформировать тонкий щит на мягкой стали в серной кислоте и какой из двух обеспечивает лучшую защиту.
Проверка эффективности молекулярного щита
Команда сначала испытала реальные образцы стали в серной кислоте с добавлением полимеров и без них. Они измеряли скорость растворения металла, отслеживая потерю веса с течением времени, и использовали чувствительные электрические методы, показывающие, как легко течёт ток при коррозии. Во всех случаях добавление любого из полимеров резко снизило скорость коррозии и замедлило как процессы растворения металла, так и реакции с образованием газов на поверхности. При более высоких дозах полимера коррозия падала более чем на 90 процентов, то есть лишь небольшая часть стали терялась по сравнению с незащищёнными образцами. Эксперименты также показали, что полимеры помогают стали противостоять «точечной коррозии» (pitting) — опасной форме локализованного поражения, которая прорезает глубокие отверстия в металле.
Как тонкая плёнка блокирует кислоту
Электрические измерения дали представление о происходящем на поверхности стали. По мере увеличения концентрации полимера сопротивление прохождению заряда росло, а кажущаяся электрическая ёмкость поверхности уменьшалась. Проще говоря, между сталью и кислотой нарастал более плотный, более изолирующий слой, заставляющий электроны и коррозионные ионы гораздо труднее проникать через него. Анализ изменения характеристик с температурой указал на то, что полимеры удерживаются главным образом физическим притяжением и электростатическими силами, а не прочными химическими связями, и что они выстраиваются в один относительно однородный слой на металле. Это согласуется с классическими моделями адсорбции, в которых поверхность постепенно заполняется молекулами ингибитора до тех пор, пока большинство реакционноспособных участков не будет покрыто.
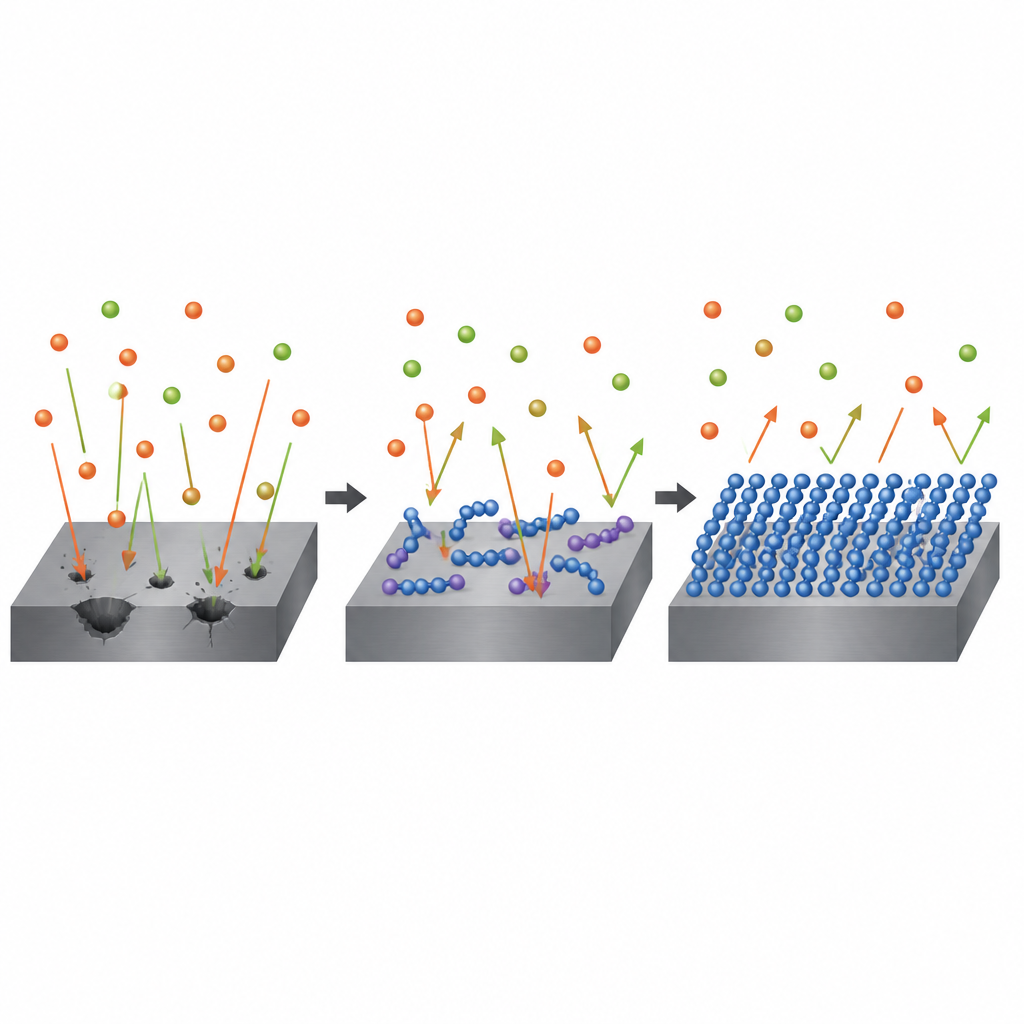
Заглядывая в молекулы с помощью компьютера
Чтобы понять, почему один полимер работает лучше другого, исследователи обратились к вычислительной химии. Они использовали квантовые расчёты, чтобы отобразить, где располагаются электроны в каждой молекуле и как легко они могут перемещаться на стальную поверхность или от неё. По предсказаниям, полипиррол отдаёт больше электронной плотности железу и содержит более сильно заряженные участки, которые лучше захватывают металл. Моделирование, при котором полимеры «посадили» на виртуальную модель железной поверхности, показало, что полипиррол связывается чуть сильнее и лежит более плоско, максимально увеличивая контакт. Эти факторы помогают ему формировать более плотную, более связную защитную плёнку, чем политиеофен, хотя по некоторым простым электронным показателям политиеофен выглядит несколько более реакционноспособным.
Почему полипиррол лидирует
В совокупности лабораторные испытания и компьютерные модели рисуют согласованную картину. И политиеофен, и полипиррол могут действовать как самособирающееся покрытие, которое цепляется к мягкой стали в серной кислоте, существенно замедляя растворение металла и помогая предотвратить образование глубоких ям. Тем не менее полипиррол сильнее взаимодействует с железом и более эффективно упаковывается на поверхности, поэтому он обеспечивает лучшую защиту при каждой проверенной концентрации. Для отраслей, вынужденных работать с сильными кислотами, но желающих увеличить срок службы оборудования и снизить количество отказов, такие полимерные ингибиторы предлагают многообещающий путь к более надёжной и долговечной стальной инфраструктуре.
Цитирование: Abdallah, M., Al-Gorair, A.S., Al Jahdaly, B.A. et al. Experimental and theoretical insights into the inhibitory capabilities of polythiophene and polypyrrole molecules for protecting mild steel from corrosion in sulfuric acid. Sci Rep 16, 15045 (2026). https://doi.org/10.1038/s41598-026-50293-9
Ключевые слова: коррозия стали, ингибиторы коррозии, проводящие полимеры, серная кислота, полипиррол