Clear Sky Science · de
Experimentelle und theoretische Einblicke in die hemmenden Fähigkeiten von Polythiophen- und Polypyrrol-Molekülen zum Schutz von Baustahl vor Korrosion in Schwefelsäure
Warum der Schutz von alltäglichem Stahl wichtig ist
Von Brücken und Autos bis zu Fabrikleitungen hängt vieles im modernen Leben von gewöhnlichem Baustahl ab. Dieses weit verbreitete Metall löst sich jedoch langsamt auf, wenn es mit aggressiven Säuren in Kontakt kommt, die beim Reinigen und in der Fertigung eingesetzt werden. Die hier beschriebene Studie untersucht, wie zwei besondere, kunststoffähnliche Materialien, Polythiophen und Polypyrrol, Stahl in einen molekularen Regenmantel hüllen können, der ihn in Schwefelsäure — einer in der Industrie weit verbreiteten Chemikalie — vor dem Zerfall bewahrt.
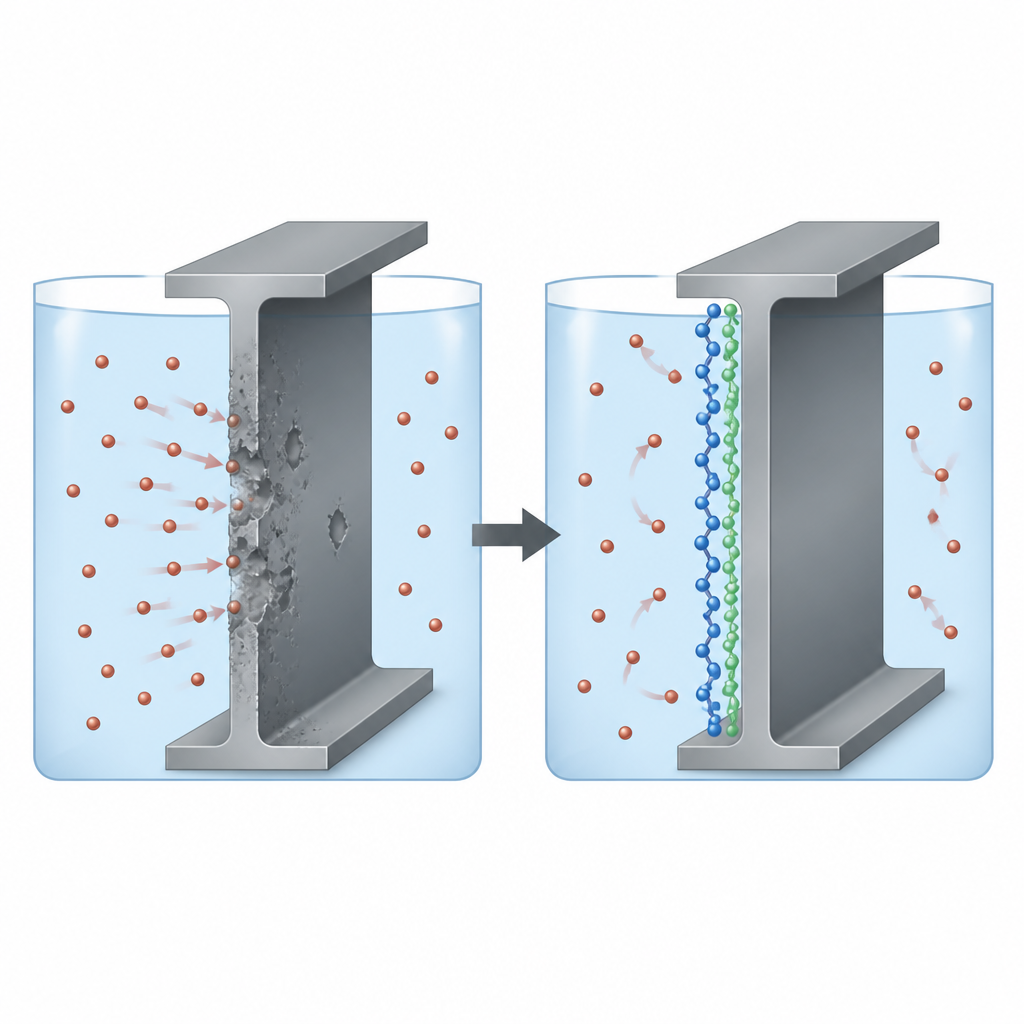
Stahl unter Beschuss in sauren Lösungen
In vielen Branchen ist Schwefelsäure unverzichtbar zum Reinigen, Beizen und Formen von Stahlteilen, greift dabei aber auch die Metalloberfläche aggressiv an. Ingenieure geben dem Säurebad häufig „Korrosionsinhibitoren“ zu, um diesen Schaden zu verlangsamen. Die Autoren konzentrierten sich auf zwei elektrisch leitfähige Polymere, Polythiophen und Polypyrrol, die aufgrund ihrer kettenartigen Struktur Wolken beweglicher Elektronen und reaktiver Atome tragen, welche am Stahl haften können. Die zentrale Frage war, ob diese Polymere auf Baustahl in Schwefelsäure eine dünne Schutzschicht bilden können und welches der beiden die bessere Schutzwirkung bietet.
Prüfung, wie gut der molekulare Schild wirkt
Das Team testete zunächst reale Stahlproben in Schwefelsäure mit und ohne die Polymere. Sie bestimmten die Auflösung des Metalls, indem sie den Massenverlust über die Zeit verfolgten und empfindliche elektrische Messungen einsetzten, die zeigen, wie leicht Strom während der Korrosion fließt. In allen Fällen führte das Zusatz der Polymere zu einer deutlichen Reduktion der Korrosionsrate und verlangsamte sowohl das Metallauflösungs- als auch das Gasbildungsreaktionen an der Oberfläche. Bei höheren Polymerkonzentrationen sank die Korrosion um mehr als 90 Prozent, sodass nur ein kleiner Bruchteil des Stahls gegenüber ungeschützten Proben verloren ging. Die Experimente zeigten außerdem, dass die Polymere dem Stahl halfen, „Grubenbildung“ zu widerstehen — eine gefährliche, stark lokalisierte Angriffsform, die tiefe Löcher ins Metall frisst.
Wie ein dünner Film die Säure blockiert
Elektrische Messungen zeichneten ein Bild dessen, was an der Stahloberfläche geschieht. Mit zunehmender Polymermenge stieg der Widerstand gegen Ladungstransport und die scheinbare elektrische Kapazität an der Oberfläche nahm ab. Einfacher ausgedrückt: Zwischen Stahl und Säure bildete sich eine dichtere, isolierendere Schicht, die es Elektronen und korrosiven Ionen deutlich erschwerte, hindurchzudringen. Die Analyse der temperaturabhängigen Leistungsänderungen deutete darauf hin, dass die Polymere überwiegend durch physikalische Anziehung und elektrostatische Kräfte gehalten werden, statt durch starke chemische Bindungen, und dass sie sich in einer einzelnen, relativ gleichmäßigen Schicht auf dem Metall anordnen. Das stimmt mit klassischen Adsorptionsmodellen überein, in denen die Oberfläche nach und nach mit Inhibitor-Molekülen gefüllt wird, bis die meisten reaktiven Stellen bedeckt sind.
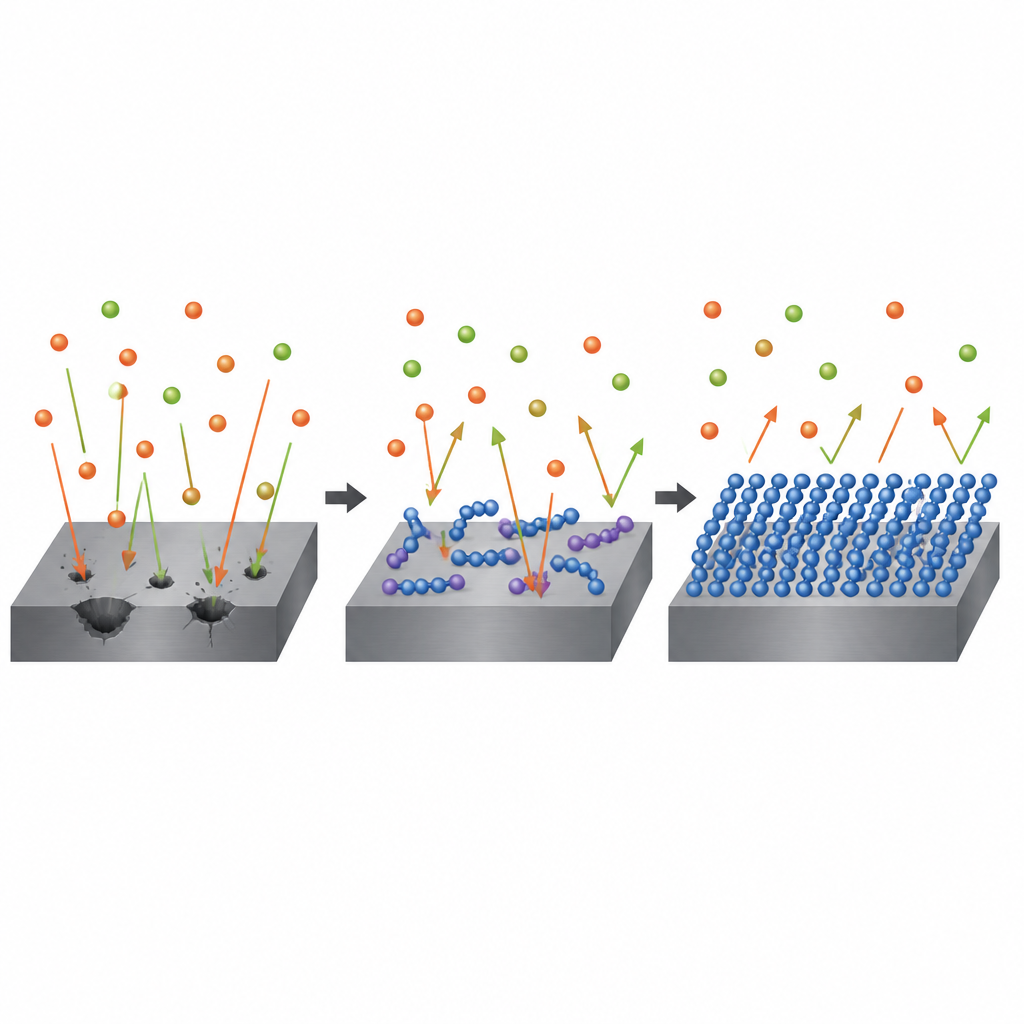
Ein Blick in die Moleküle am Computer
Um zu verstehen, warum ein Polymer besser wirkt als das andere, wandten sich die Forscher der Rechnerchemie zu. Sie nutzten Quantenberechnungen, um zu kartieren, wo sich Elektronen in jedem Molekül befinden und wie leicht sie zum oder vom Stahl übertragen werden können. Es wurde vorhergesagt, dass Polypyrrol mehr Elektronendichte an Eisen abgibt und stärker geladene Bereiche präsentiert, die das Metall besser greifen können. Simulationen, in denen die Polymere virtuell auf einer Modell-Eisenoberfläche „landen“, zeigten, dass Polypyrrol etwas stärker bindet und flach aufliegt, wodurch der Kontakt maximiert wird. Diese Faktoren helfen ihm, einen dichteren, kohäsiveren Schutzfilm zu bilden als Polythiophen, obwohl Polythiophen in einigen einfachen elektronischen Kennwerten geringfügig reaktiver erscheint.
Warum Polypyrrol die Nase vorn hat
Zusammenfassend ergeben Laborversuche und Computermodelle ein stimmiges Bild. Sowohl Polythiophen als auch Polypyrrol können wie ein selbstorganisierender Überzug wirken, der an Baustahl in Schwefelsäure haftet, die Auflösung des Metalls deutlich verlangsamt und das Entstehen tiefer Gruben verhindert. Polypyrrol jedoch wechselwirkt stärker mit Eisen und ordnet sich effizienter auf der Oberfläche an, sodass es bei jeder getesteten Konzentration besseren Schutz liefert. Für Industrien, die starke Säuren einsetzen, aber möchten, dass ihre Anlagen länger halten und weniger ausfallen, bieten solche polymerbasierten Inhibitoren einen vielversprechenden Weg zu sichererer, langlebigerer Stahlinfrastruktur.
Zitation: Abdallah, M., Al-Gorair, A.S., Al Jahdaly, B.A. et al. Experimental and theoretical insights into the inhibitory capabilities of polythiophene and polypyrrole molecules for protecting mild steel from corrosion in sulfuric acid. Sci Rep 16, 15045 (2026). https://doi.org/10.1038/s41598-026-50293-9
Schlüsselwörter: Stahlkorrosion, Korrosionsinhibitoren, leitfähige Polymere, Schwefelsäure, Polypyrrol