Clear Sky Science · pl
Doświadczeniowe i teoretyczne wglądy w zdolności hamujące cząsteczek politiopfeny i polipirrolu w ochronie stali niskowęglowej przed korozją w kwasie siarkowym
Dlaczego ochrona zwykłej stali ma znaczenie
Od mostów i samochodów po rurociągi w zakładach — współczesne życie w dużej mierze zależy od stali niskowęglowej. Ten powszechny metal jednak powoli rozpuszcza się w kontakcie z agresywnymi kwasami stosowanymi do czyszczenia i w procesach przemysłowych. Badanie opisane w tym artykule bada, jak dwa specjalne, przypominające tworzywo materiały — politiophena i polipirrol — mogą otulić stal molekularnym „płaszczykiem”, chroniąc ją przed niszczeniem w kwasie siarkowym, szeroko stosowanym związku przemysłowym.
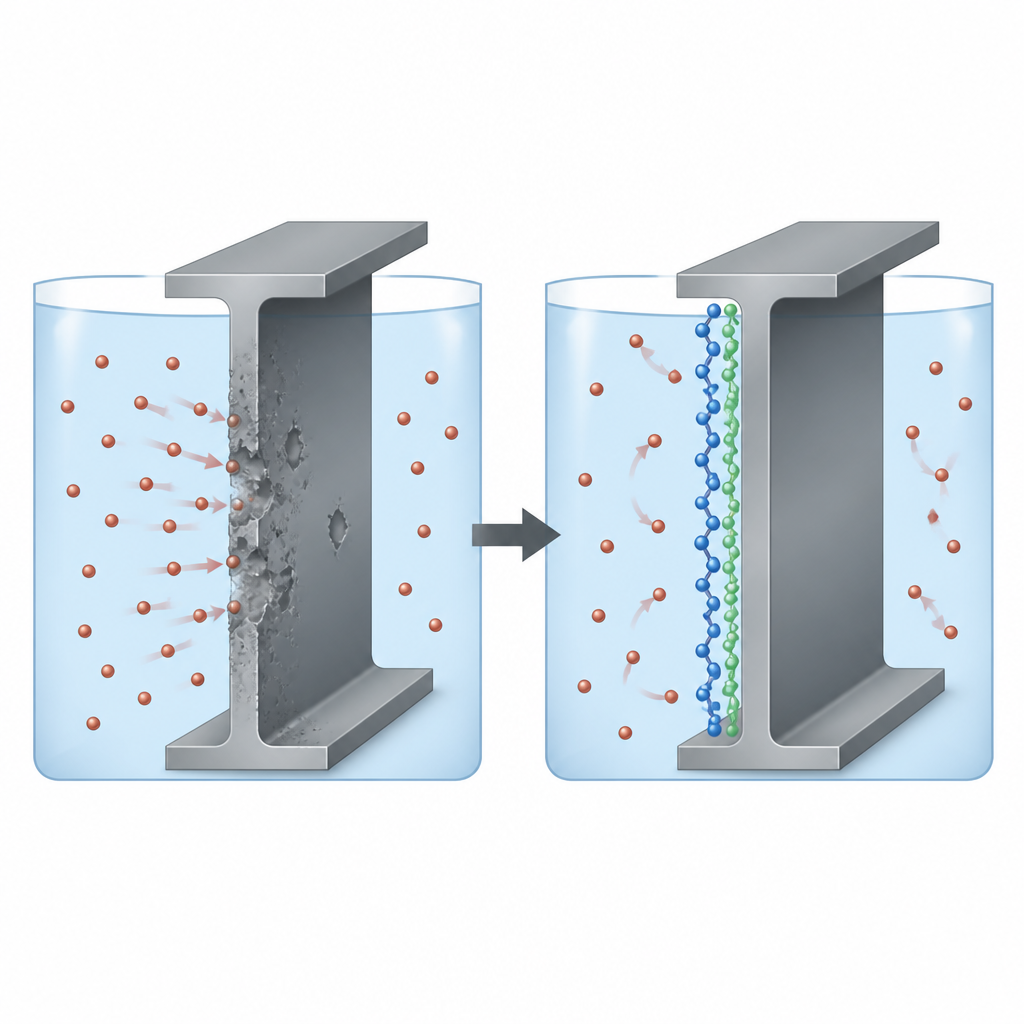
Stal pod atakiem w roztworach kwaśnych
W wielu gałęziach przemysłu kwas siarkowy jest niezbędny do czyszczenia, trawienia i kształtowania elementów stalowych, ale jednocześnie agresywnie wżera się w powierzchnię metalu. Inżynierowie często dodają do kwasu „inhibitory korozji”, aby spowolnić to niszczenie. Autorzy skupili się na dwóch przewodzących elektrycznie polimerach — politiophenie i polipirrolu — wybranych ze względu na ich łańcuchową strukturę niosącą chmury ruchomych elektronów i reaktywnych atomów, które mogą przywierać do stali. Kluczowe pytanie brzmiało, czy te polimery mogą utworzyć cienką tarczę na stali niskowęglowej w kwasie siarkowym i który z nich zapewnia lepszą ochronę.
Badanie skuteczności molekularnej powłoki
Zespół najpierw testował rzeczywiste próbki stali w kwasie siarkowym z dodatkiem polimerów i bez nich. Mierzono tempo rozpuszczania metalu, śledząc ubytek masy w czasie oraz stosując czułe metody elektryczne ujawniające, jak łatwo przepływa prąd podczas korozji. We wszystkich przypadkach dodanie któregoś z polimerów znacząco zmniejszało szybkość korozji oraz spowalniało zarówno reakcje rozpuszczania metalu, jak i tworzenia gazów na powierzchni. Przy wyższych dawkach polimeru korozja spadła o ponad 90 procent, co oznacza, że w porównaniu z niechronionymi próbkami utrata stali była znikoma. Eksperymenty wykazały także, że polimery pomagały stali opierać się „dziurkowaniu” (pittingowi) — niebezpiecznej, silnie zlokalizowanej formie ataku, która drąży głębokie otwory w metalu.
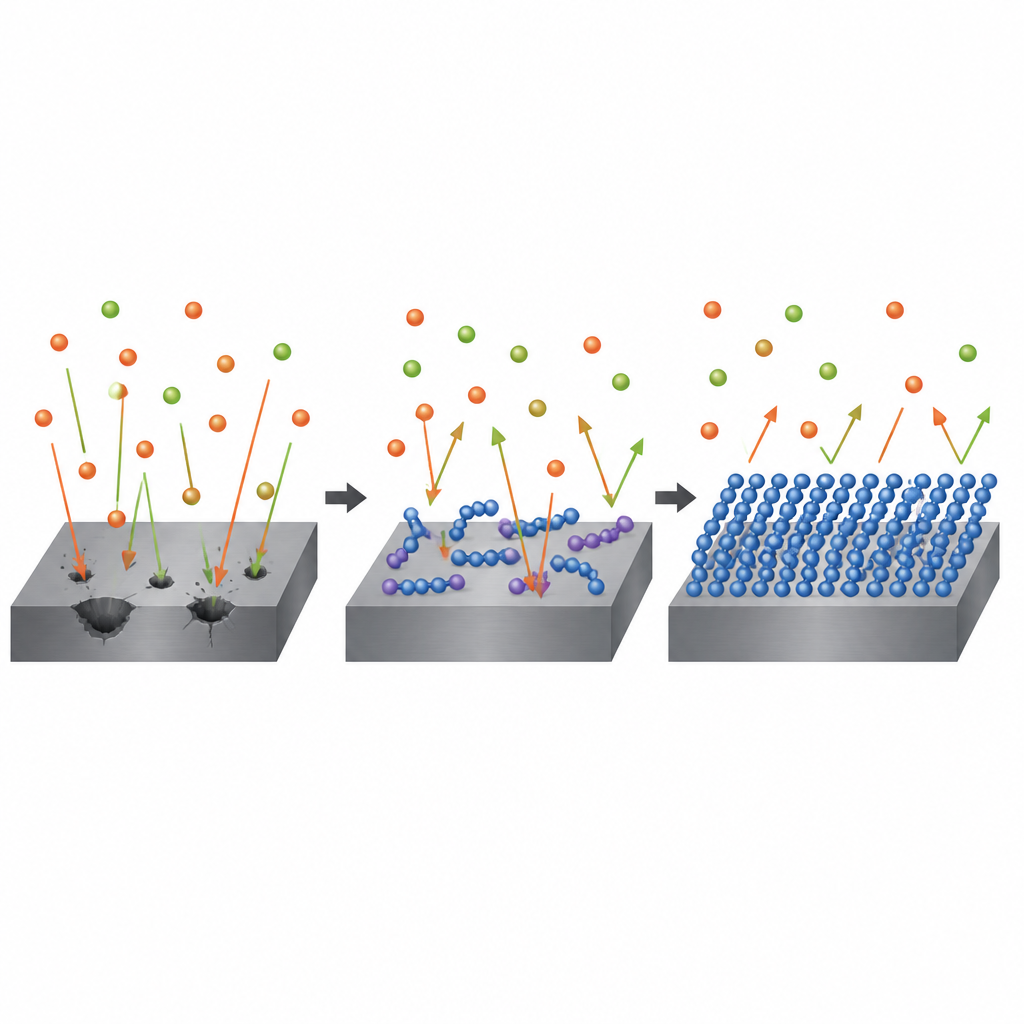
Jak cienka warstwa blokuje kwas
Pomiary elektryczne naszkicowały, co dzieje się na powierzchni stali. Wraz ze wzrostem zawartości polimeru wzrastał opór dla przepływu ładunków, a pozorna pojemność elektryczna powierzchni malała. Mówiąc prościej: między stalą a kwasem budowała się gęstsza, bardziej izolująca warstwa, zmuszając elektrony i korozyjne jony do znacznie większego wysiłku, by przez nią przejść. Analiza zmian wydajności w funkcji temperatury sugerowała, że polimery utrzymywane są głównie przez przyciąganie fizyczne i siły elektrostatyczne, a nie przez silne wiązania chemiczne, i że układają się w pojedynczą, dość jednolitą warstwę na metalu. Zgadza się to z klasycznymi modelami adsorpcji, w których powierzchnia stopniowo wypełnia się cząsteczkami inhibitora, aż większość reaktywnych miejsc zostanie pokryta.
Zajrzeć w cząsteczki za pomocą komputera
Aby zrozumieć, dlaczego jeden polimer działa lepiej od drugiego, badacze sięgnęli po chemię komputerową. Wykorzystali obliczenia kwantowe do zobrazowania, gdzie w każdej cząsteczce znajdują się elektrony i jak łatwo mogą przemieszczać się na powierzchnię stali lub z niej. Przewidziano, że polipirrol oddaje więcej gęstości elektronowej żelazu i prezentuje silniej naładowane obszary, które lepiej chwytają metal. Symulacje, które wirtualnie „lądują” polimery na modelowej powierzchni żelaznej, wykazały, że polipirrol wiąże się nieco silniej i układa się płasko, maksymalizując styczność. Te czynniki pomagają mu zbudować bardziej zwartą, spójną warstwę ochronną niż politiophena, mimo że politiophena wydaje się nieco bardziej reaktywna w niektórych prostych miarach elektronicznych.
Dlaczego polipirrol wypada lepiej
W sumie wyniki z laboratoriów i modeli komputerowych tworzą spójną opowieść. Zarówno politiophena, jak i polipirrol mogą zachowywać się jak samoorganizująca się powłoka przylegająca do stali niskowęglowej w kwasie siarkowym, znacznie spowalniając tempo rozpuszczania metalu i pomagając zapobiegać powstawaniu głębokich ubytków. Jednak polipirrol oddziałuje mocniej z żelazem i układa się gęściej na powierzchni, dzięki czemu zapewnia lepszą ochronę przy każdej testowanej koncentracji. Dla branż, które muszą używać silnych kwasów, a jednocześnie chcą, by urządzenia działały dłużej i rzadziej zawodziły, inhibitory oparte na takich polimerach oferują obiecującą drogę do bezpieczniejszej i trwalszej infrastruktury stalowej.
Cytowanie: Abdallah, M., Al-Gorair, A.S., Al Jahdaly, B.A. et al. Experimental and theoretical insights into the inhibitory capabilities of polythiophene and polypyrrole molecules for protecting mild steel from corrosion in sulfuric acid. Sci Rep 16, 15045 (2026). https://doi.org/10.1038/s41598-026-50293-9
Słowa kluczowe: korozja stali, inhibitory korozji, polimery przewodzące, kwas siarkowy, polipirrol