Clear Sky Science · fr
Perspectives expérimentales et théoriques sur les capacités inhibitrices des molécules de polythiophène et de polypyrrole pour protéger l'acier doux de la corrosion dans l'acide sulfurique
Pourquoi il est important de protéger l'acier courant
Des ponts et des voitures aux tuyauteries d'usine, une grande partie de la vie moderne repose sur l'acier doux. Pourtant, ce métal courant se dissout lentement au contact d'acides agressifs employés pour le nettoyage et la fabrication. L'étude à l'origine de cet article examine comment deux matériaux semblables à des plastiques, le polythiophène et le polypyrrole, peuvent envelopper l'acier d'un « imperméable » moléculaire qui l'empêche de se dégrader dans l'acide sulfurique, un produit chimique industriel largement utilisé.
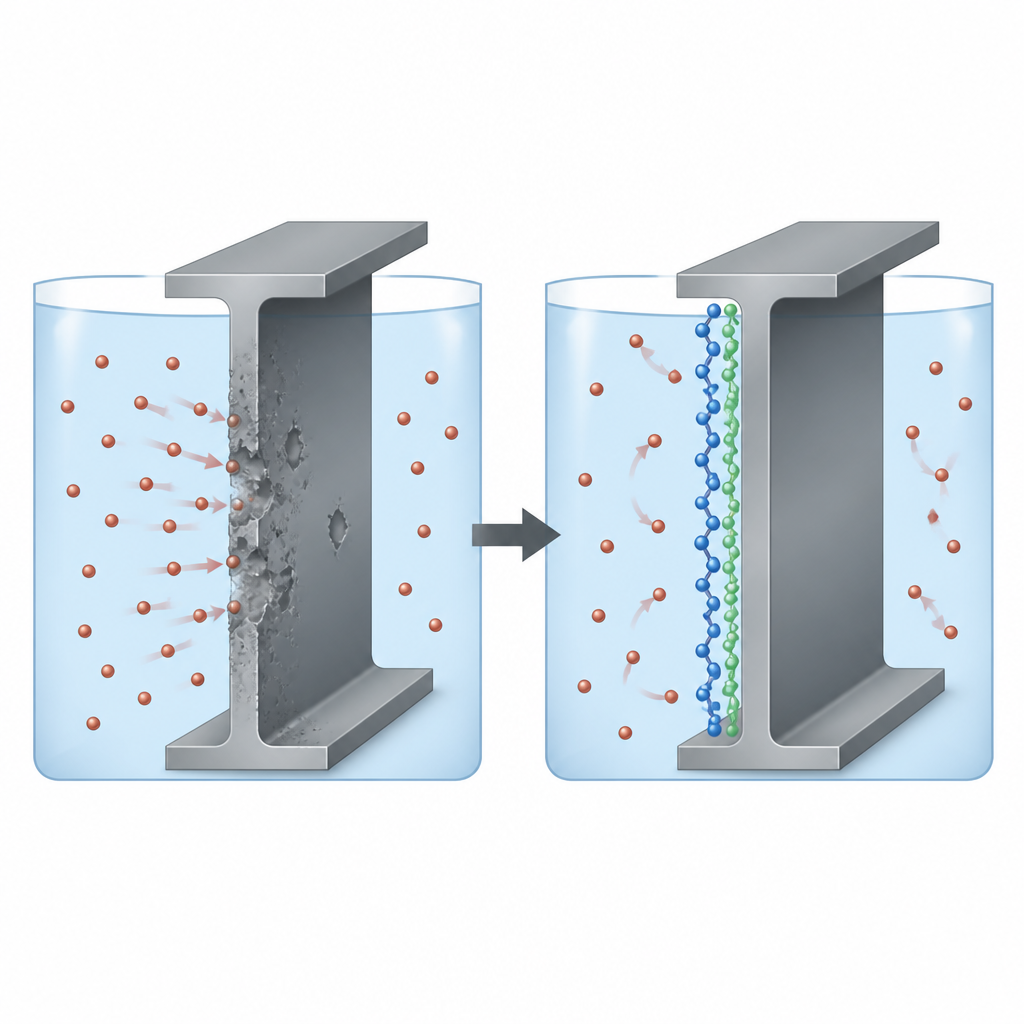
L'acier attaqué dans des solutions acides
Dans de nombreuses industries, l'acide sulfurique est essentiel pour nettoyer, décaper et mettre en forme des pièces en acier, mais il attaque également la surface du métal de manière agressive. Les ingénieurs ajoutent souvent des « inhibiteurs de corrosion » à l'acide pour ralentir ces dommages. Les auteurs se sont concentrés sur deux polymères conducteurs électriques, le polythiophène et le polypyrrole, choisis parce que leurs structures en chaînes portent des nuages d'électrons mobiles et des atomes réactifs capables de s'accrocher à l'acier. La question centrale était de savoir si ces polymères pouvaient former un mince bouclier sur l'acier doux dans l'acide sulfurique, et lequel des deux offre la meilleure protection.
Évaluer l'efficacité du bouclier moléculaire
L'équipe a d'abord testé de vrais échantillons d'acier dans l'acide sulfurique avec et sans les polymères. Ils ont mesuré la vitesse de dissolution du métal en suivant la perte de masse au fil du temps et en utilisant des méthodes électriques sensibles révélant la facilité de passage du courant pendant la corrosion. Dans tous les cas, l'ajout de l'un ou l'autre polymère a fortement réduit le taux de corrosion et ralenti à la fois les réactions de dissolution du métal et celles de formation de gaz à la surface. À des doses plus élevées de polymère, la corrosion a chuté de plus de 90 %, ce qui signifie qu'une faible fraction de l'acier a été perdue par rapport aux échantillons non protégés. Les expériences ont également montré que les polymères aident l'acier à résister au « piqûres » (pitting), une forme dangereuse d'attaque très localisée qui creuse des trous profonds dans le métal.
Comment un film mince bloque l'acide
Les mesures électriques ont dessiné un tableau de ce qui se passe à la surface de l'acier. Avec davantage de polymère présent, la résistance au passage de charge a augmenté et la capacité électrique apparente à la surface a diminué. En termes plus simples, une couche plus dense et plus isolante s'est formée entre l'acier et l'acide, obligeant les électrons et les ions corrosifs à fournir beaucoup plus d'effort pour traverser. L'analyse de l'évolution des performances avec la température suggère que les polymères sont retenus principalement par attraction physique et forces électrostatiques, plutôt que par de fortes liaisons chimiques, et qu'ils s'organisent en une seule couche assez uniforme sur le métal. Ceci concorde avec les modèles classiques d'adsorption dans lesquels la surface se remplit progressivement de molécules inhibitrices jusqu'à ce que la plupart des sites réactifs soient couverts.
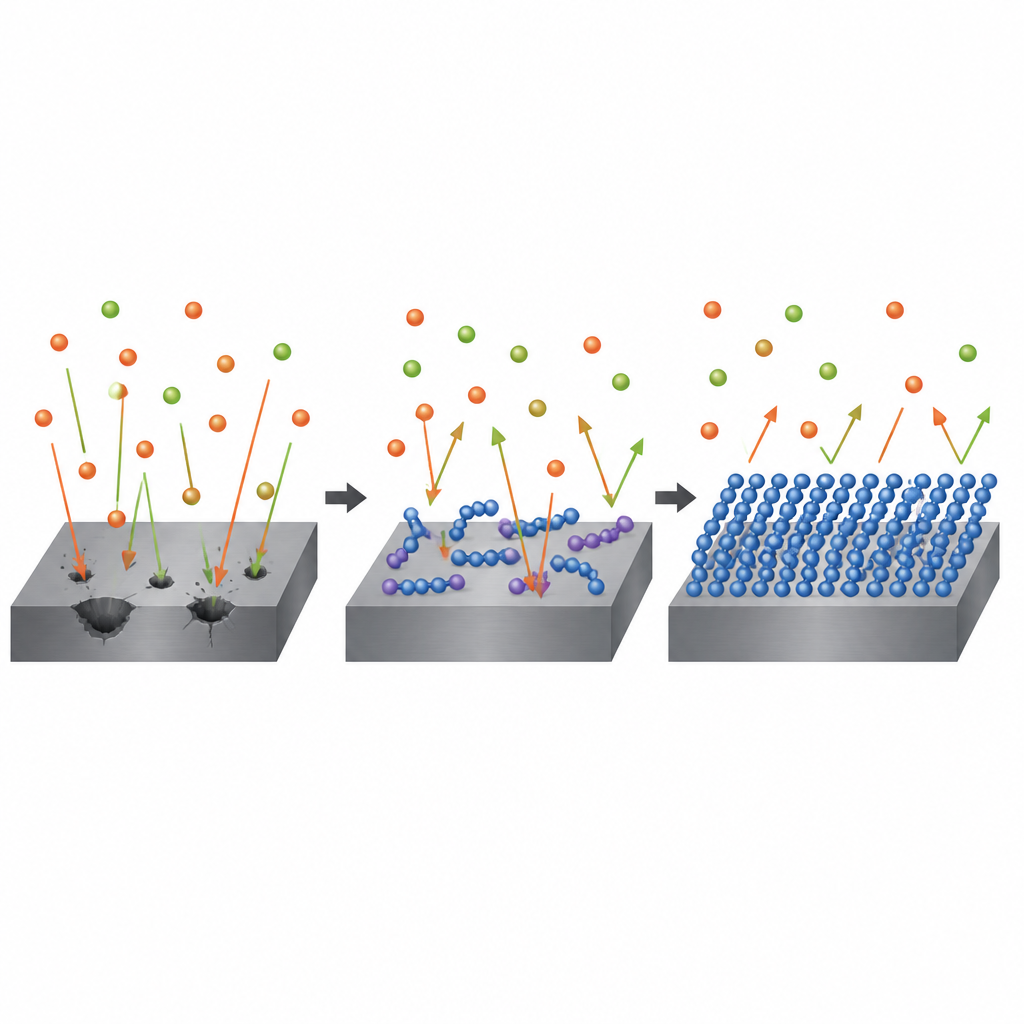
Observer les molécules par ordinateur
Pour comprendre pourquoi un polymère fonctionne mieux que l'autre, les chercheurs se sont tournés vers la chimie computationnelle. Ils ont utilisé des calculs quantiques pour cartographier où se situent les électrons sur chaque molécule et à quel point ils peuvent facilement se déplacer vers ou depuis la surface en fer. Le polypyrrole a été prédit comme donnant davantage de densité électronique au fer et présentant des régions plus fortement chargées pouvant agripper le métal. Des simulations qui « déposent » virtuellement les polymères sur une surface modèle de fer ont montré que le polypyrrole se lie un peu plus fortement et s'étend à plat, maximisant le contact. Ces facteurs l'aident à former un film protecteur plus serré et plus cohésif que le polythiophène, même si le polythiophène semble légèrement plus réactif selon certaines mesures électroniques simples.
Pourquoi le polypyrrole l'emporte
Pris ensemble, les tests en laboratoire et les modèles informatiques racontent une histoire cohérente. Le polythiophène et le polypyrrole peuvent tous deux agir comme un revêtement auto-organisé qui adhère à l'acier doux dans l'acide sulfurique, ralentissant considérablement la vitesse de dissolution du métal et aidant à prévenir la formation de piqûres profondes. Cependant, le polypyrrole interagit plus fortement avec le fer et se compactifie mieux à la surface, offrant ainsi une protection supérieure à toutes les concentrations testées. Pour les industries qui doivent employer des acides forts mais souhaitent que leurs équipements durent plus longtemps et tombent moins souvent en panne, ces inhibiteurs à base de polymères représentent une voie prometteuse vers des infrastructures en acier plus sûres et plus durables.
Citation: Abdallah, M., Al-Gorair, A.S., Al Jahdaly, B.A. et al. Experimental and theoretical insights into the inhibitory capabilities of polythiophene and polypyrrole molecules for protecting mild steel from corrosion in sulfuric acid. Sci Rep 16, 15045 (2026). https://doi.org/10.1038/s41598-026-50293-9
Mots-clés: corrosion de l'acier, inhibiteurs de corrosion, polymères conducteurs, acide sulfurique, polypyrrole