Clear Sky Science · ru
Эдельфозин вызывает остановку клеточного цикла и апоптоз в гладкомышечных клетках сосудов для подавления неоинтимальной гиперплазии
Почему засорённые артерии важны
Когда артерию расширяют баллоном или устанавливают стент, цель — восстановить кровоток к сердцу или мозгу. Но сосуд часто реагирует ростом нового внутреннего слоя из мышц и рубцовой ткани, который постепенно снова сужает просвет. В этом исследовании изучали, может ли препарат эдельфозин, изначально созданный для уничтожения раковых клеток, использоваться локально на сосудах, чтобы сдержать это разрастание и дольше поддерживать артерии открытыми.
Ближе к проблеме разрастания стенки сосуда
После процедур вроде ангиопластики или установки стента гладкомышечные клетки в стенке сосуда могут переключаться в режим активного деления. Они размножаются и мигрируют внутрь, формируя толстый слой, называемый неоинтимой, который сужает канал, по которому должен течь кровоток. Современные стенты выделяют препараты, замедляющие рост клеток, но они не всегда полностью предотвращают проблему и могут воздействовать на другие типы клеток. Авторы предположили, что препарат, способный избирательно направлять чрезмерно активные гладкомышечные клетки в запрограммированную гибель, может предложить более сильный и точечный способ предотвращения повторного сужения.
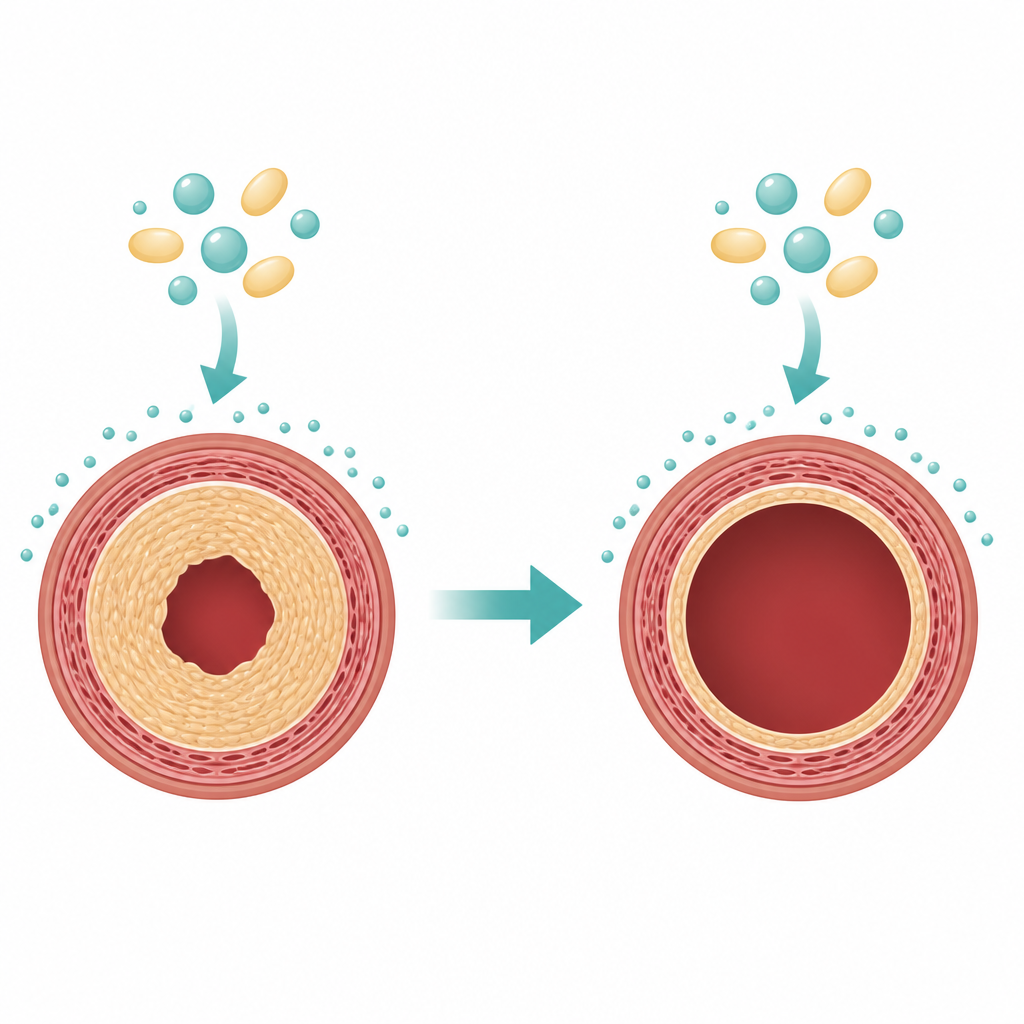
Заимствование противоракового препарата для сосудов
Эдельфозин — синтетическая жироподобная молекула, которая внедряется в клеточные мембраны и, как известно, запускает программы самоуничтожения в быстро делящихся раковых клетках, щадя многие покоящиеся клетки. Команда протестировала эдельфозин на гладкомышечных клетках, взятых из артерий крыс и мышей и выращенных в чашках. При умеренных дозах препарат заметно снижал число жизнеспособных клеток и количество синтезируемой ими новой ДНК, что указывает на остановку деления. Эти эффекты были сильнее при отсутствии факторов роста в сыворотке, что говорит о том, что эдельфозин особенно эффективен, когда клетки зависят от активных сигналов роста.
Как эдельфозин останавливает и удаляет проблемные клетки
Чтобы выяснить, что происходит внутри клеток, исследователи отслеживали их прохождение через клеточный цикл — стадии, через которые клетка проходит в подготовке к делению. При действии эдельфозина многие клетки скапливались на стадии непосредственно перед делением и во время него и часто не разделялись должным образом, оставаясь с двумя ядрами. Это указывало на блокаду на контрольной точке деления. Одновременно увеличивались молекулярные маркеры стресс‑реакции в внутренней структуре — эндоплазматическом ретикулуме, и активировались ключевые «исполнительные» белки, запускающие запрограммированную клеточную гибель. Блокирование этих ферментов смерти спасало множество клеток, подтверждая, что эдельфозин не просто замедляет рост, а активно запускает упорядоченную форму клеточного самоубийства.
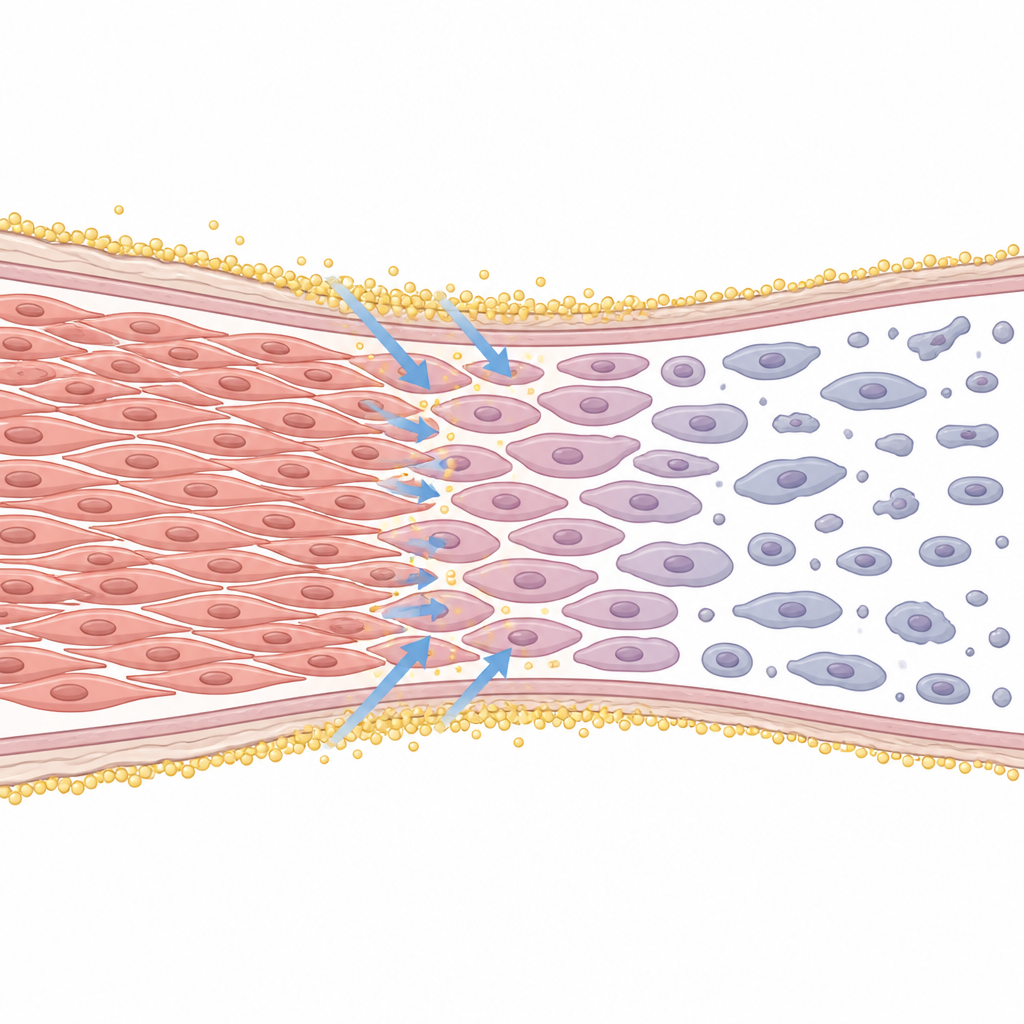
Роль кальция внутри клеток
В исследовании также изучали поток ионов кальция, которые служат мощными внутриклеточными сигналами. С помощью флуоресцентных красителей команда показала, что эдельфозин вызывает быстрый рост уровня кальция внутри гладкомышечных клеток. Препараты, блокирующие вход кальция извне или мешающие его высвобождению из внутренних депо, уменьшали этот подъём и частично ослабляли раннюю волну гибели клеток. Это указывает на то, что нарушение обращения кальция, связанное с внутренним стрессом, является одним из ранних шагов, посредством которых эдельфозин толкает эти клетки к выключению и удалению.
Проверка подхода в живых сосудах
Чтобы узнать, имеют ли лабораторные находки значение в живом организме, исследователи использовали модель мыши, в которой перетяжка сонной артерии надёжно вызывает утолщение внутреннего слоя. Они оборачивали повреждённую артерию гидрогелем, содержащим эдельфозин или безопасный наполнитель. Через две недели в артериях, обработанных эдельфозином, наблюдались значительно более тонкая неоинтима и более широкий открытый просвет, в то время как средний мышечный слой оставался целым. Окраска на фрагментированную ДНК выявила больше клеток, проходящих запрограммированную гибель в стенке сосуда у обработанных животных, что согласуется с результатами in vitro и не сопровождалось признаками очевидного повреждения сосуда или образования тромбов в этом краткосрочном исследовании.
Что это может означать для пациентов
Работа показывает, что эдельфозин может одновременно останавливать деление чрезмерно активных гладкомышечных клеток и подтолкнуть их к контролируемой самоуничтожению, смягчая утолщение, угрожающее заново закупорить обработанные артерии. Действуя через мембранные и внутренние стресс‑маршруты, а не через классические мишени клеточного деления, он отличается от препаратов, применяемых в современных лекарственных стентах, и может щадить больше окружающей здоровой ткани. Хотя предстоит ещё много проверок, особенно на человеческих сосудах и в долгосрочной перспективе, результаты позволяют предположить, что липидный препарат, заимствованный из онкологии, однажды сможет помочь дольше поддерживать проходимость вновь открытых артерий за счёт удаления тех самых клеток, которые вызывают повторное сужение.
Цитирование: Sun, J., Gui, Y., Liu, Y. et al. Edelfosine induces cell cycle arrest and apoptosis in vascular smooth muscle cells to suppress neointimal hyperplasia. Sci Rep 16, 14944 (2026). https://doi.org/10.1038/s41598-026-44632-z
Ключевые слова: эдельфозин, сосудистая гладкая мышца, неоинтимальная гиперплазия, рестеноз, апоптоз