Clear Sky Science · nl
Edelfosine veroorzaakt celcyclusarrest en apoptose in vasculaire gladde spiercellen om neointimale hyperplasie te remmen
Waarom dichtgroeiende arteriën ertoe doen
Wanneer een arterie wordt geopend met een ballon of stent, is het doel om de bloedstroom naar het hart of de hersenen te herstellen. Maar het vat reageert vaak door een nieuwe binnenlaag van spier- en littekenweefsel te vormen die de doorgang langzaam weer doet dichtslibben. Deze studie onderzoekt of een middel genaamd edelfosine, oorspronkelijk ontwikkeld om kankercellen te doden, lokaal op bloedvaten kan worden gebruikt om deze overgroei te remmen en arteriën langer open te houden.
Een nadere blik op overgroei van de vaatwand
Na ingrepen zoals dotteren of plaatsing van een stent kunnen gladde spiercellen in de vaatwand omschakelen naar een groeimodus. Ze delen zich en migreren naar binnen, waar ze een dikke laag vormen die neointima wordt genoemd en het kanaal waar het bloed doorheen moet stromen vernauwt. Huidige stents geven medicijnen af die celdeling vertragen, maar die voorkomen dit probleem niet altijd volledig en kunnen andere celtypen beïnvloeden. De auteurs redeneerden dat een middel dat selectief overactieve gladde spiercellen in een gecontroleerd doodsprogramma kan duwen, een krachtigere en gerichtere manier zou kunnen bieden om hervernauwing te voorkomen.
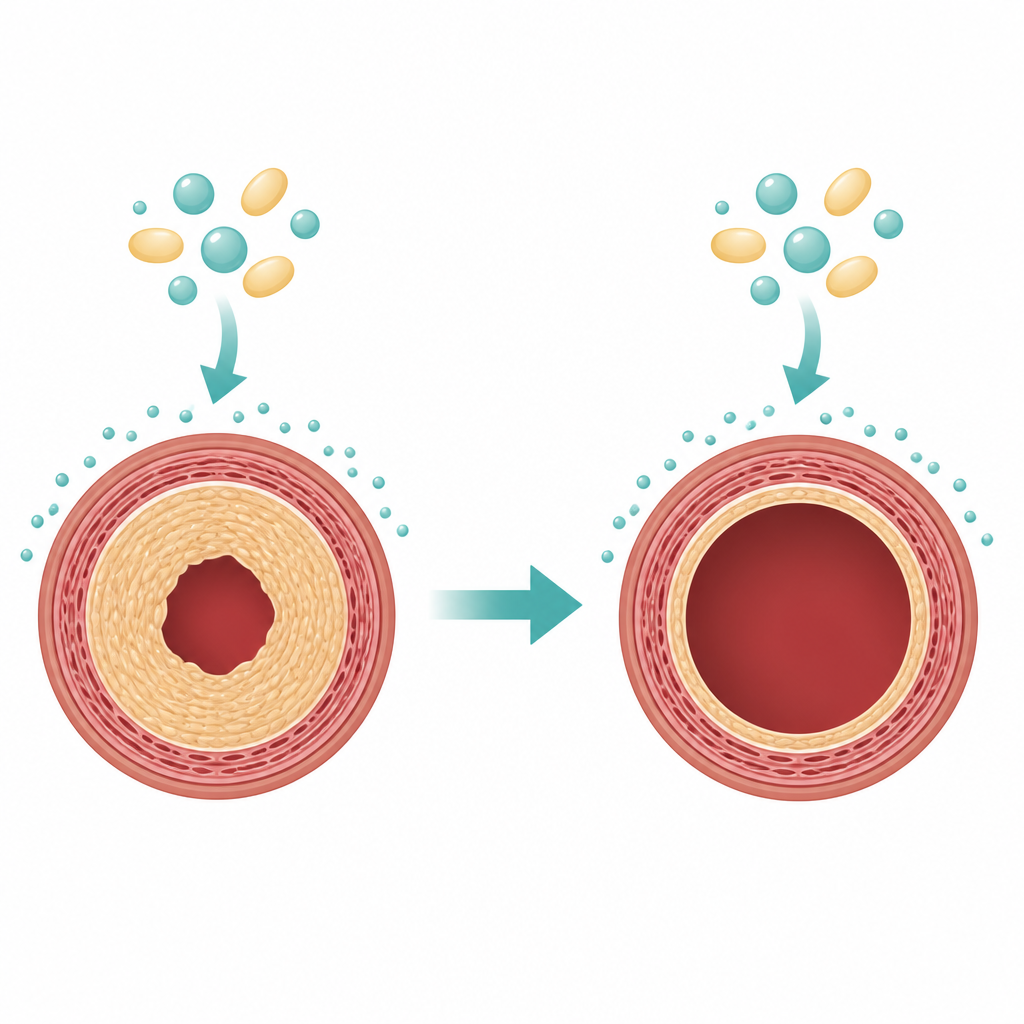
Een kankermedicijn lenen voor bloedvaten
Edelfosine is een synthetische, vetachtige molecule die in celmembranen schuift en bekendstaat om zelfdestructieprogramma's te activeren in snel delende kankercellen, terwijl veel rustende cellen gespaard blijven. Het team testte edelfosine op gladde spiercellen afkomstig van rat- en muisarteriën die in kweekschalen werden gekweekt. Bij matige doses verminderde het middel sterk het aantal levensvatbare cellen en de hoeveelheid nieuw DNA die werd gevormd, een teken dat de cellen waren gestopt met delen. Deze effecten waren sterker in afwezigheid van groeifactoren uit serum, wat suggereert dat edelfosine vooral hard toeslaat wanneer cellen afhankelijk zijn van actieve groeisignalen.
Hoe edelfosine probleemcellen stopt en verwijdert
Om te achterhalen wat er in de cellen gebeurt, volgden de onderzoekers hun voortgang door de celcyclus, de fasen die een cel doorloopt terwijl ze zich voorbereidt op deling. Onder invloed van edelfosine stapelden veel cellen zich op in de fase net voor en tijdens deling en slaagden er vaak niet in correct te splitsen, waardoor ze met twee kernen eindigden. Dit wees op een blokkade bij de delingscontrole. Tegelijkertijd namen moleculaire merkers van een stressreactie in een interne structuur, het endoplasmatisch reticulum, toe en werden belangrijke "uitvoerder"-eiwitten die geprogrammeerde celdood aansturen geactiveerd. Het remmen van deze doodseiwitten redde veel cellen, wat bevestigt dat edelfosine niet alleen de groei vertraagt maar actief een ordelijke vorm van celdood induceert.
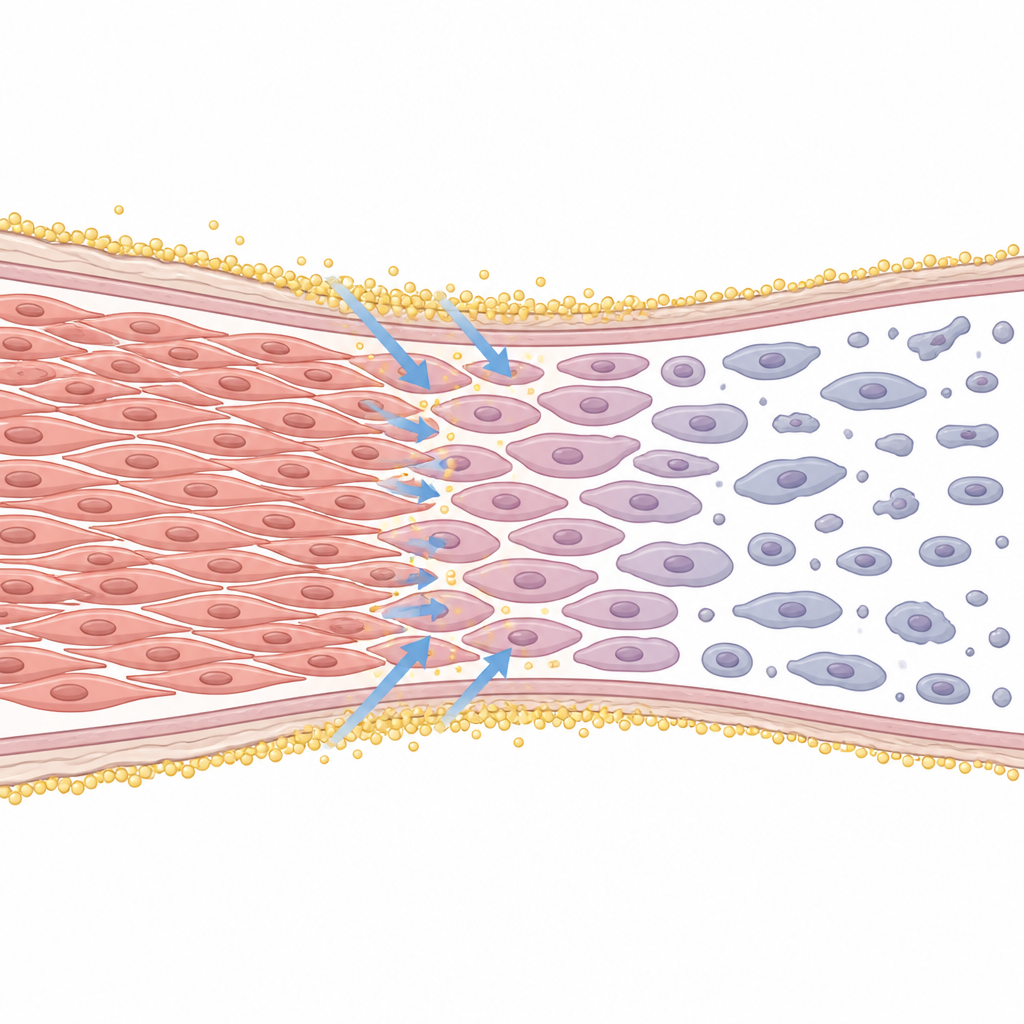
De rol van calcium in de cellen
De studie onderzocht ook de beweging van calciumionen, die als krachtige interne signaalmoleculen fungeren. Met behulp van fluorescerende kleurstoffen toonde het team aan dat edelfosine een snelle stijging van calciumspiegels binnen gladde spiercellen veroorzaakte. Middelen die de instroom van calcium van buiten de cel blokkeerden of de vrijlating van calcium uit interne voorraden verstoorden, verminderden deze stijging en verlichtten gedeeltelijk de vroege golf van celdood. Dit suggereert dat verstoorde calciumhuishouding, gekoppeld aan interne stress, een van de vroege stappen is waarmee edelfosine deze cellen naar uitschakeling en verwijdering duwt.
Het aanpakken van de methode in levende arteriën
Om te zien of deze bevindingen uit het lab ook in levende weefsels gelden, gebruikten de onderzoekers een muismodel waarbij het dichtbinden van een halsslagader betrouwbaar leidt tot verdikking van de binnenlaag. Ze wikkelden de beschadigde arterie in met een hydrogel die edelfosine of een onschadelijk draagmiddel bevatte. Na twee weken vertoonden de met edelfosine behandelde arteriën veel dunner geworden binnenlagen en een verder open kanaal, terwijl de middelste spierlaag intact bleef. Kleuring voor gefragmenteerd DNA toonde meer cellen die geprogrammeerde celdood ondergingen in de vaatwand van behandelde dieren, in overeenstemming met de kweekexperimenten en zonder tekenen van duidelijke vaatbeschadiging of trombusvorming in deze kortetermijnstudie.
Wat dit voor patiënten zou kunnen betekenen
Het werk suggereert dat edelfosine zowel kan stoppen dat overactieve gladde spiercellen delen als ze kan aansporen tot een gecontroleerd zelfdestructieproces, waardoor de verdikking die arteriën opnieuw kan doen dichtslibben wordt verminderd. Doordat het via membranen en interne stressroutes werkt in plaats van via klassieke celdelingsdoelen, verschilt het van de middelen die nu in medicinale stents worden gebruikt en kan het meer van het omliggende gezonde weefsel sparen. Hoewel er nog veel getest moet worden, vooral in menselijke vaten en over langere perioden, wekken de bevindingen de mogelijkheid dat een door kanker geïnspireerd lipide-medicijn op een dag zou kunnen helpen geopende arteriën langer open te houden door juist die cellen terug te snoeien die tot vernauwing leiden.
Bronvermelding: Sun, J., Gui, Y., Liu, Y. et al. Edelfosine induces cell cycle arrest and apoptosis in vascular smooth muscle cells to suppress neointimal hyperplasia. Sci Rep 16, 14944 (2026). https://doi.org/10.1038/s41598-026-44632-z
Trefwoorden: edelfosine, vasculaire gladde spiercel, neointimale hyperplasie, restenose, apoptose