Clear Sky Science · ar
الإيديلفوسين يسبب توقّف دورة الخلية والموت المبرمج في الخلايا العضلية الوعائية الملساء لتقليل فرط النسيج الداخلي
لماذا تهم الشرايين المسدودة
عند توسيع شريان بواسطة بالون أو دعامة، الهدف هو استعادة تدفق الدم إلى القلب أو الدماغ. لكن الوعاء غالبًا ما يستجيب بنمو طبقة داخلية جديدة من العضلات والندبة التي تعيد تضييق الممر تدريجيًا. تستقصي هذه الدراسة ما إذا كان دواء يُدعى الإيديلفوسين، المصمم أصلاً لقتل الخلايا السرطانية، يمكن استخدامه موضعيًا على الأوعية الدموية للحد من هذا النمو والحفاظ على الشرايين مفتوحة لفترة أطول.
نظرة أقرب على فرط نمو جدار الوعاء
بعد إجراءات مثل توسيع الشريان أو زرع الدعامة، يمكن أن تتحول الخلايا العضلية الملساء في جدار الوعاء إلى وضعية نمو. تتكاثر وتتحرك إلى الداخل، فتكوّن طبقة سميكة تُسمى النسيج الداخلي الجديد (neointima) التي تضيق القناة التي يجب أن يمر عبرها الدم. تطلق الدعامات الحالية أدوية تبطئ نمو الخلايا، لكنها لا تمنع هذه المشكلة بالكامل دائمًا وقد تؤثر على أنواع خلوية أخرى. افترض المؤلفون أن دواءً قادرًا على دفع الخلايا العضلية الملساء المفرطة النشاط نحو مسار موت مبرمج انتقائي قد يوفر وسيلة أقوى وأكثر تركيزًا لمنع إعادة التضييق.
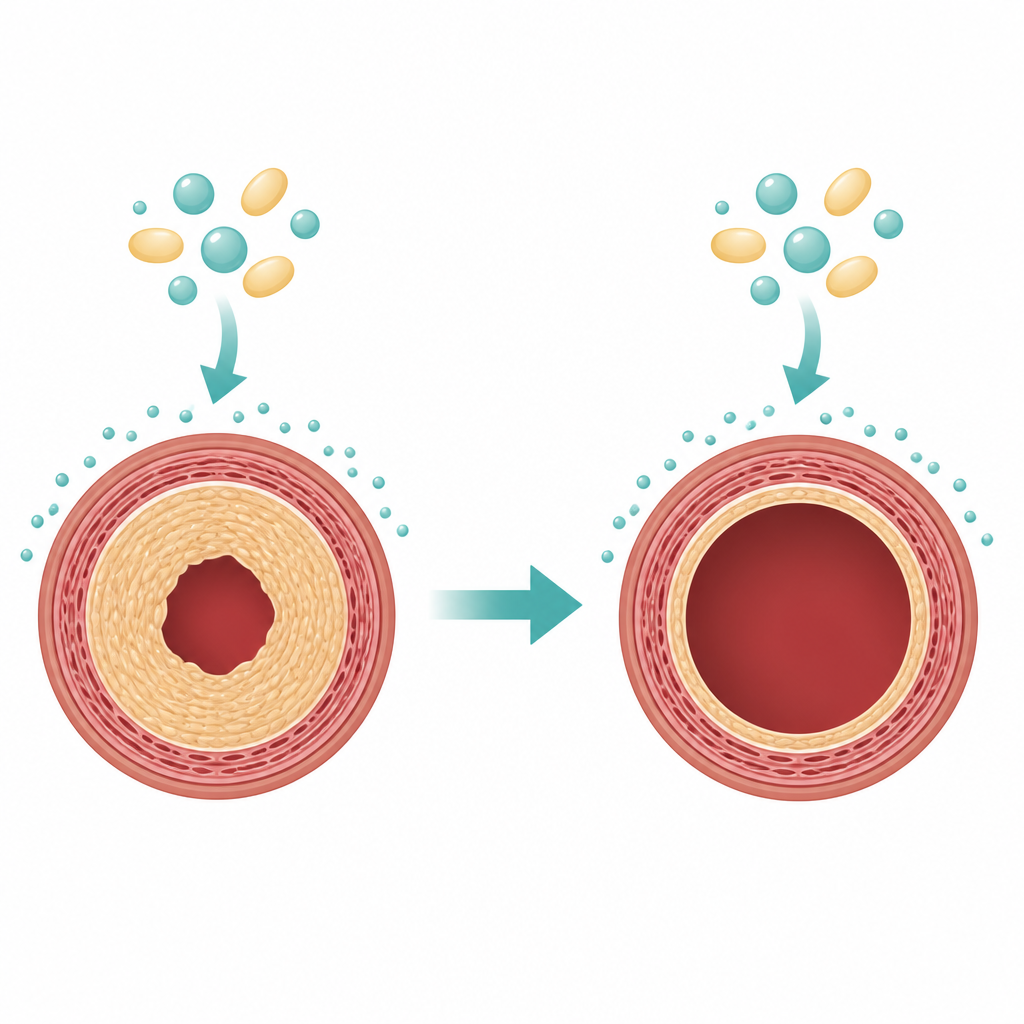
استعارة دواء سرطاني للأوعية الدموية
الإيديلفوسين هو جزيء صناعي شبيه بالدهون يندمج في أغشية الخلايا ومعروف بتحفيز برامج الانتحار الذاتي في الخلايا السرطانية سريعة الانقسام مع حفاظه على الكثير من الخلايا الساكنة. اختبر الفريق الإيديلفوسين على خلايا عضلية ملساء مأخوذة من شرايين الفئران والجرذان ومزروعة في أطباق. بجرعات معتدلة، خفض الدواء بشكل حاد عدد الخلايا الحيّة ومقدار الحمض النووي الجديد الذي تُنتجه، وهو مؤشر على توقفها عن الانقسام. كانت هذه التأثيرات أقوى في غياب عوامل النمو في المصل، ما يشير إلى أن الإيديلفوسين يؤثر بشدة خاصة عندما تعتمد الخلايا على إشارات نمو نشطة.
كيف يوقِف الإيديلفوسين ويزيل الخلايا المشكلة
لكي يفهموا ما الذي يحدث داخل الخلايا، تتبّع الباحثون تقدمها خلال دورة الخلية، وهي المراحل التي تمرّ بها الخلية أثناء استعدادها للانقسام. مع الإيديلفوسين، تراكمت كثير من الخلايا في المرحلة التي تسبق وأثناء الانقسام وغالبًا فشلت في الانقسام بشكل صحيح، ما أدى إلى وجود نواتين في الخلية. أشارت هذه الظاهرة إلى وجود حاجز عند نقطة فحص الانقسام. في الوقت نفسه، ازداد ظهور مؤشرات جزيئية لاستجابة الإجهاد في بنية داخلية تُسمى الشبكة الإندوبلازمية، وتشغّلت بروتينات "المنفذين" الأساسية التي تقود الموت المبرمج. إن حجب هذه الإنزيمات المسببة للموت أنقذ العديد من الخلايا، مما يؤكد أن الإيديلفوسين لم يكتفِ بإبطاء النمو بل فعّل بالفعل شكلًا منظمًا من انتحار الخلية.
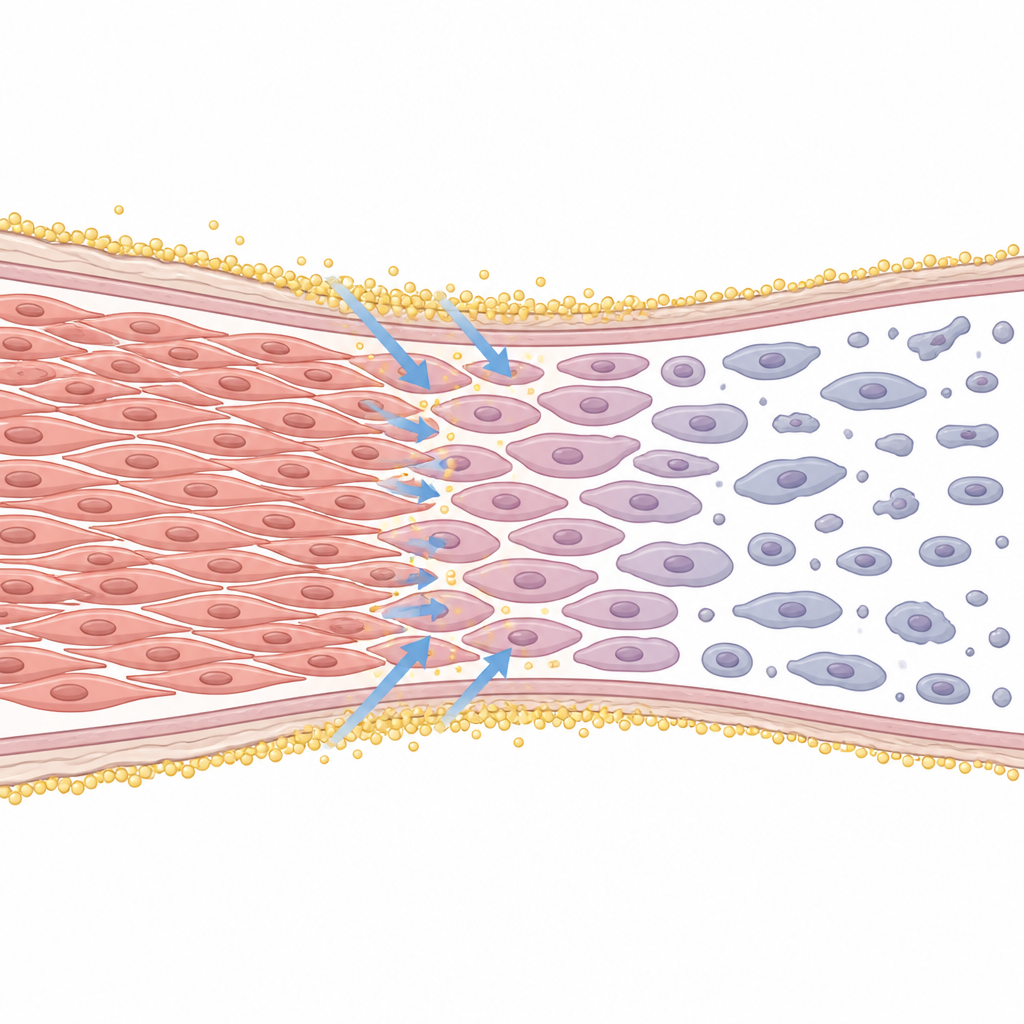
دور الكالسيوم داخل الخلايا
فحصت الدراسة أيضًا تدفّق أيونات الكالسيوم، التي تعمل كإشارات داخلية قوية. باستخدام أصباغ فلورية، أظهر الفريق أن الإيديلفوسين تسبب في ارتفاع سريع في مستويات الكالسيوم داخل الخلايا العضلية الملساء. الأدوية التي تمنع دخول الكالسيوم من خارج الخلية أو تعيق إفرازه من المخازن الداخلية خففت هذا الارتفاع وقلّلت جزئيًا موجة الموت الخلوي المبكرة. يشير ذلك إلى أن اضطراب تعامل الخلايا مع الكالسيوم المرتبط بالإجهاد الداخلي هو أحد الخطوات المبكرة التي يدفع بها الإيديلفوسين هذه الخلايا نحو التوقف والإزالة.
اختبار النهج في شرايين حية
للتأكد ما إذا كانت النتائج المخبرية ذات صلة في جسم حَيّ، استخدم الباحثون نموذج فئران حيث يسبب ربط شريان السبات reliably سماكة الطبقة الداخلية. لفّوا الشريان المصاب بهلام مائي يحتوي على الإيديلفوسين أو مركب حميد. بعد أسبوعين، أظهرت الشرايين المعالجة بالإيديلفوسين طبقات داخلية أرق ومجرى أوسع، بينما بقيت الطبقة العضلية الوسطى سليمة. كشفت صبغات تكسر الحمض النووي عن عدد أكبر من الخلايا التي تمر بالموت المبرمج في جدار الوعاء لدى الحيوانات المعالجة، متسقة مع تجارب الأطباق ودون علامات تلف واضح في الوعاء أو تكوّن خثرات في هذه الدراسة قصيرة المدى.
ماذا قد يعني هذا للمرضى
تشير النتائج إلى أن الإيديلفوسين يمكنه إيقاف خلايا العضلات الملساء المفرطة النشاط عن الانقسام ودفعها نحو عملية انتحار خلوي منظمة، مما يخفف من السُمك الذي يهدد بإعادة انسداد الشرايين المعالجة. بعمله عبر مسارات متعلقة بالغشاء والإجهاد الداخلي بدلًا من استهدافات الانقسام الكلاسيكية، يختلف عن الأدوية المستخدمة حاليًا في الدعامات المطلية بالأدوية وقد يحافظ على المزيد من الأنسجة السليمة المحيطة. وبينما لا يزال هناك الكثير لاختباره، خصوصًا في أوعية بشرية وعلى مدى فترات أطول، تثير النتائج احتمال أن دواءً شحميًا مستوحى من السرطان قد يساعد يومًا ما في إبقاء الشرايين المعاد فتحها أنقى لفترة أطول عبر تقليم الخلايا نفسها التي تسبب تضييقها من جديد.
الاستشهاد: Sun, J., Gui, Y., Liu, Y. et al. Edelfosine induces cell cycle arrest and apoptosis in vascular smooth muscle cells to suppress neointimal hyperplasia. Sci Rep 16, 14944 (2026). https://doi.org/10.1038/s41598-026-44632-z
الكلمات المفتاحية: إيديلفوسين, الخلايا العضلية الوعائية الملساء, فرط النسيج الداخلي, إعادة التضييق, الموت المبرمج