Clear Sky Science · fr
Edelfosine induit un arrêt du cycle cellulaire et l’apoptose dans les cellules musculaires lisses vasculaires pour supprimer l’hyperplasie néointimale
Pourquoi les artères bouchées comptent
Lorsqu’une artère est réouverte par ballon ou par stent, l’objectif est de restaurer le flux sanguin vers le cœur ou le cerveau. Mais le vaisseau réagit souvent en formant une nouvelle couche interne de muscle et de tissu cicatriciel qui re‑bouche progressivement le passage. Cette étude examine si un médicament appelé edelfosine, initialement conçu pour tuer les cellules cancéreuses, peut être utilisé localement sur les vaisseaux pour freiner cette surcroissance et maintenir les artères ouvertes plus longtemps.
Un examen détaillé de la prolifération de la paroi vasculaire
Après des procédures comme l’angioplastie ou la pose de stent, les cellules musculaires lisses de la paroi vasculaire peuvent basculer en mode prolifératif. Elles se multiplient et migrent vers l’intérieur, formant une couche épaisse appelée néointima qui rétrécit le canal par lequel le sang doit circuler. Les stents actuels libèrent des médicaments qui ralentissent la croissance cellulaire, mais ils n’empêchent pas toujours complètement ce phénomène et peuvent affecter d’autres types cellulaires. Les auteurs ont supposé qu’un médicament capable de pousser sélectivement les cellules musculaires lisses hyperactives vers un programme de mort contrôlée pourrait offrir une manière plus ciblée et plus efficace d’empêcher la re‑rétrécissement.
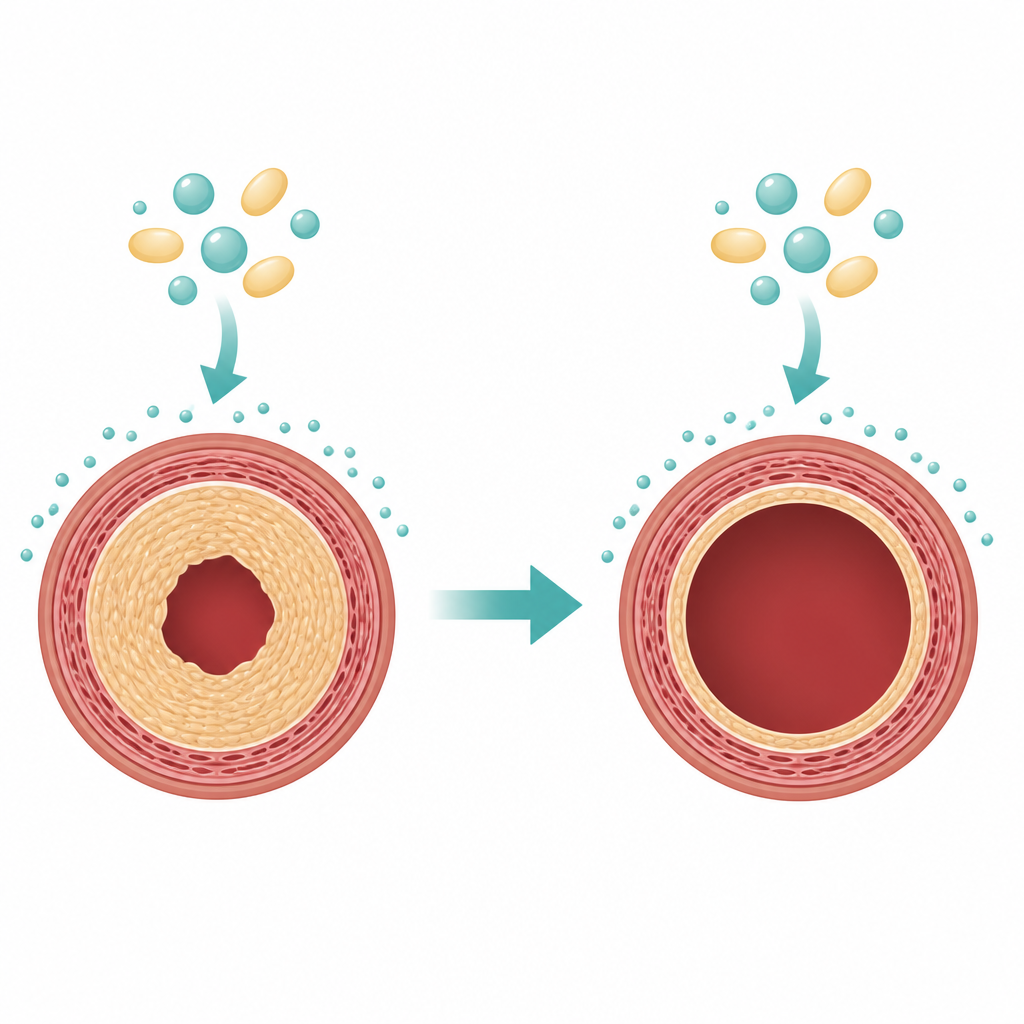
Emprunter un médicament anticancéreux pour les vaisseaux
L’edelfosine est une molécule synthétique lipophile qui s’insère dans les membranes cellulaires et est connue pour déclencher des programmes d’autodestruction dans les cellules cancéreuses à division rapide tout en épargnant de nombreuses cellules au repos. L’équipe a testé l’edelfosine sur des cellules musculaires lisses prélevées dans des artères de rat et de souris et cultivées en culture. À des doses modérées, le médicament a fortement réduit le nombre de cellules viables et la quantité d’ADN nouvellement synthétisé, signe qu’elles avaient cessé de se diviser. Ces effets étaient plus marqués en l’absence de facteurs de croissance présents dans le sérum, ce qui suggère que l’edelfosine frappe d’autant plus fort lorsque les cellules dépendent de signaux de croissance actifs.
Comment l’edelfosine arrête et élimine les cellules problématiques
Pour savoir ce qui se passe à l’intérieur des cellules, les chercheurs ont suivi leur progression dans le cycle cellulaire, les étapes par lesquelles passe une cellule avant de se diviser. Avec l’edelfosine, de nombreuses cellules s’accumulaient juste avant et pendant la division et échouaient souvent à se séparer correctement, aboutissant à des cellules à deux noyaux. Cela indiquait un blocage au niveau du point de contrôle de la division. Parallèlement, des marqueurs moléculaires d’une réponse au stress dans une structure interne appelée réticulum endoplasmique augmentaient, et des protéines « exécutrices » clés de la mort programmée étaient activées. Le blocage de ces enzymes de mort a sauvé de nombreuses cellules, confirmant que l’edelfosine n’avait pas seulement ralenti la croissance mais déclenché activement une forme ordonnée de suicide cellulaire.
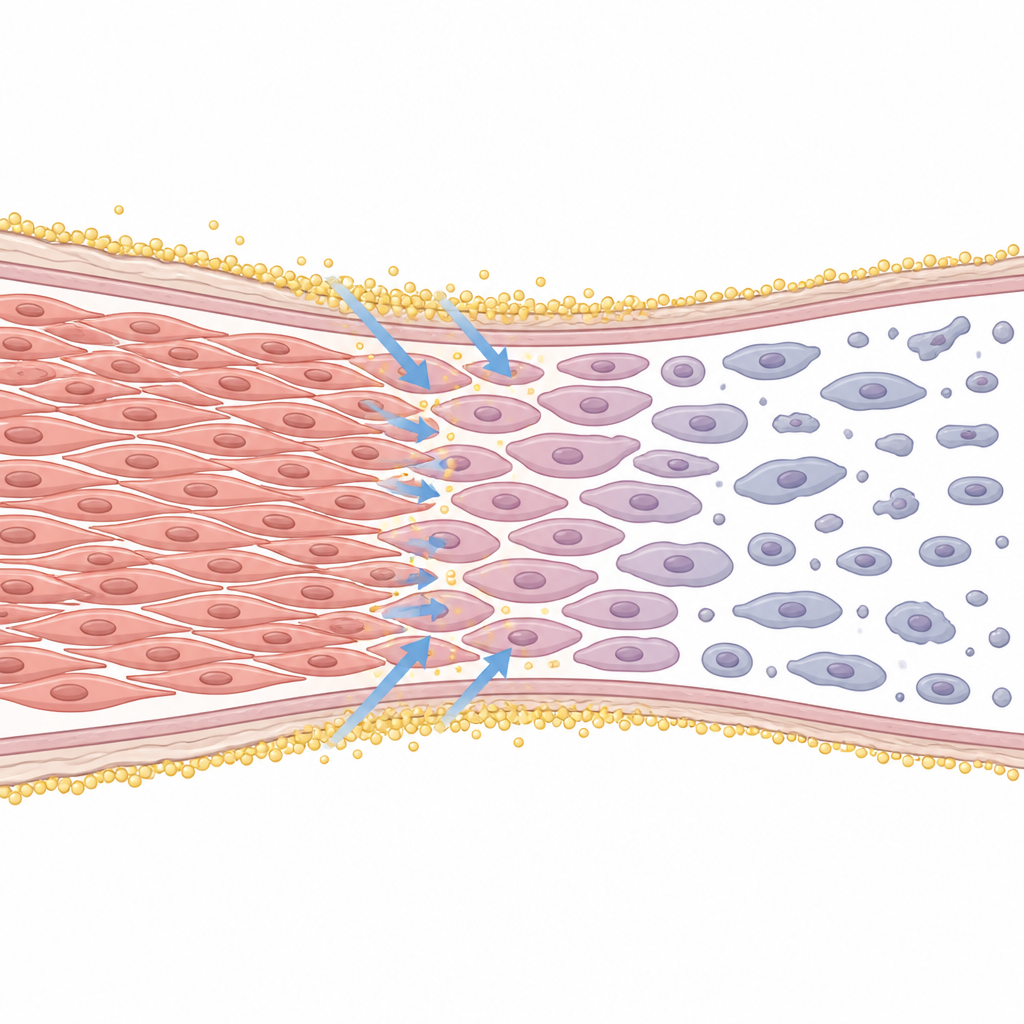
Le rôle du calcium à l’intérieur des cellules
L’étude a également examiné le flux d’ions calcium, qui servent de signaux internes puissants. En utilisant des sondes fluorescentes, l’équipe a montré que l’edelfosine provoquait une hausse rapide des niveaux de calcium intracellulaire dans les cellules musculaires lisses. Des médicaments bloquant l’entrée de calcium depuis l’extérieur ou interférant avec la libération de calcium depuis les réserves internes ont réduit cette élévation et atténué en partie la première vague de mort cellulaire. Cela suggère qu’une perturbation du contrôle du calcium, liée au stress interne, constitue une des premières étapes par lesquelles l’edelfosine pousse ces cellules vers l’arrêt et l’élimination.
Tester l’approche dans des artères vivantes
Pour savoir si ces résultats in vitro avaient une portée in vivo, les chercheurs ont utilisé un modèle murin dans lequel la ligature d’une artère carotidienne provoque de manière fiable l’épaississement de la couche interne. Ils ont entouré l’artère blessée d’un hydrogel contenant de l’edelfosine ou un véhicule inerte. Après deux semaines, les artères traitées à l’edelfosine présentaient une néointima beaucoup plus fine et un canal plus large, tandis que la couche musculaire médiane restait intacte. La coloration révélant l’ADN fragmenté montrait davantage de cellules en cours d’apoptose dans la paroi vasculaire des animaux traités, conforme aux observations en culture et sans signes évidents de dommage vasculaire ou de formation de caillots dans cette étude à court terme.
Ce que cela pourrait signifier pour les patients
Les travaux suggèrent que l’edelfosine peut à la fois empêcher les cellules musculaires lisses hyperactives de se diviser et les pousser vers un programme de mort contrôlée, réduisant ainsi l’épaississement qui menace de re‑boucher les artères traitées. En agissant via des voies membranaires et de stress intracellulaire plutôt que par les cibles classiques de la division cellulaire, il diffère des médicaments utilisés actuellement sur les stents enduits et pourrait épargner davantage les tissus sains environnants. Bien que de nombreuses étapes restent à tester, en particulier sur des vaisseaux humains et sur des périodes plus longues, ces résultats ouvrent la possibilité qu’un médicament lipidique inspiré de la cancérologie puisse un jour aider à maintenir plus longtemps la perméabilité des artères rouvres en élaguant les cellules responsables de leur rétrécissement.
Citation: Sun, J., Gui, Y., Liu, Y. et al. Edelfosine induces cell cycle arrest and apoptosis in vascular smooth muscle cells to suppress neointimal hyperplasia. Sci Rep 16, 14944 (2026). https://doi.org/10.1038/s41598-026-44632-z
Mots-clés: edelfosine, cellule musculaire lisse vasculaire, hyperplasie néointimale, résténose, apoptose