Clear Sky Science · ru
Влияние стимуляции PSA по сравнению с STN-DBS на эффективную связанность при болезни Паркинсона – исследование состояния покоя с использованием 3,0 Т фМРТ
Почему это исследование операции на мозге важно
Для людей с болезнью Паркинсона глубокая электрическая стимуляция в мозге может заметно уменьшать тремор и облегчать скованность движений. Хирурги уже широко используют проверенную мишень — субталамическое ядро (STN), но соседняя область — задняя субталамическая область (PSA) — проявила себя как перспективная альтернатива, особенно у пациентов, у которых основная проблема — тремор. Это исследование использует современные методы сканирования мозга, чтобы проследить, как каждая из этих двух точек стимуляции перестраивает внутреннее взаимодействие между участками мозга, с прицелом на более персонализированный выбор лечения в будущем.
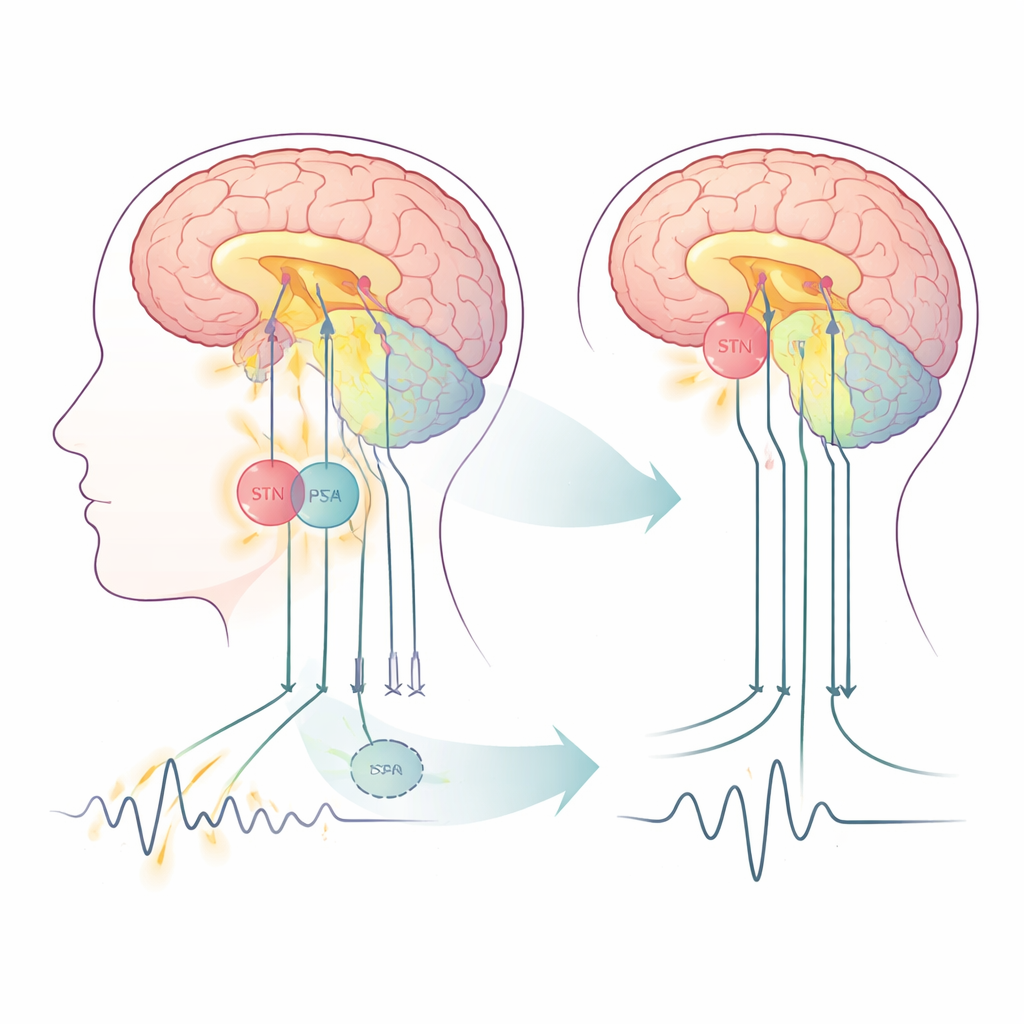
Два близких «переключателя» в сети, управляющей движением
Болезнь Паркинсона нарушает набор мозговых цепей, контролирующих движение, включая кору большого мозга, глубокие структуры — базальные ганглии — и «тонкую настройку» в задней части мозга, мозжечок. Глубокая мозговая стимуляция (DBS) подаёт быстрые электрические импульсы через имплантированные электроды и уже признана эффективным лечением, когда медикаменты перестают быть достаточными. Традиционно основной мишенью было STN. PSA, богатая волокнами зона прямо позади и над STN, привлекает внимание, потому что она тесно связана с путями, вовлечёнными в тремор. В этом исследовании пятнадцати людям с тремор-доминантной формой болезни Паркинсона установили одну пару электродов так, чтобы разные контакты могли стимулировать либо STN, либо PSA вдоль одной и той же траектории — это позволило редкое внутримозговое сравнение «голова к голове».
Наблюдение за покоящимся мозгом с высокой детализацией
Исследователи сканировали каждого участника трижды на мощном 3-тесловом МРТ-сканере: до операции, при выключенной стимуляции, и после операции — при стимуляции либо PSA, либо STN. Все сканирования выполнялись в состоянии покоя, без двигательных заданий, чтобы зафиксировать естественные паттерны активности мозга. С помощью метода функциональной МРТ в состоянии покоя измеряли медленные колебания оксигенации крови, отражающие активность нейронов. Затем применяли модельный подход, оценивающий не только наличие связей между регионами, но и то, насколько сильно один регион управляет другим — так называемую «эффективную связанность». Моделировали две основные петли: корково–базальные ганглии, вовлечённую в запуск и остановку движения, и корково–мозжечково–таламическую петлю, которую считают поддерживающей и формирующей тремор.
Общие успокаивающие эффекты на гиперактивные связи
И PSA, и STN-стимуляция привели к большим и клинически значимым улучшениям двигательных показателей, включая тремор, замедленность, скованность и позу, без явного преимущества одного метода по суммарному облегчению симптомов в этой небольшой группе. В мозговых сетях обе мишени показали несколько общих эффектов. Стимуляция в любой из точек ослабляла прямой путь от главной двигательной зоны коры к STN («гиперпрямой» вход) и усиливала тенденцию STN тормозить собственную активность. Обе мишени также сокращали передачи сигналов от коры к мозжечку. Что важно, степень подавления пути «кора→STN» и укрепления саморегуляции STN коррелировала с тем, насколько улучшились движения: более выраженные изменения в этих связях шли в паре с большими приростами скорости и общих моторных показателей.
Различный акцент на цепях, связанных с тремором
Несмотря на общие закономерности, мишени не были тождественны в том, как они перестраивали сеть. Стимуляция PSA более сильно снижала связь «кора→мозжечок», чем STN-стимуляция, и усиливала передачу от стриатума (ещё одной структуры базальных ганглиев) к STN. Во всех условиях сканирования у людей с более выраженным тремором обычно отмечали более сильную двустороннюю связность, вовлекающую мозжечок, тогда как суммарные оценки и баллы за брадикинезию (замедленность) были связаны со силой связи «кора→STN». Эти взаимосвязи поддерживают «двухцепочную» модель тремора при Паркинсоне: области базальных ганглиев действуют как переключатель, запускающий тремор, а петля, центром которой является мозжечок, работает как регулятор интенсивности (как «диммер»). Полученные данные позволяют предположить, что стимуляция PSA может быть особенно эффективна для снижения этого «диммера» тремора, даже если в пределах этого небольшого исследования дополнительный физиологический эффект ещё не отразился в явно лучших клинических оценках тремора по сравнению только с STN.
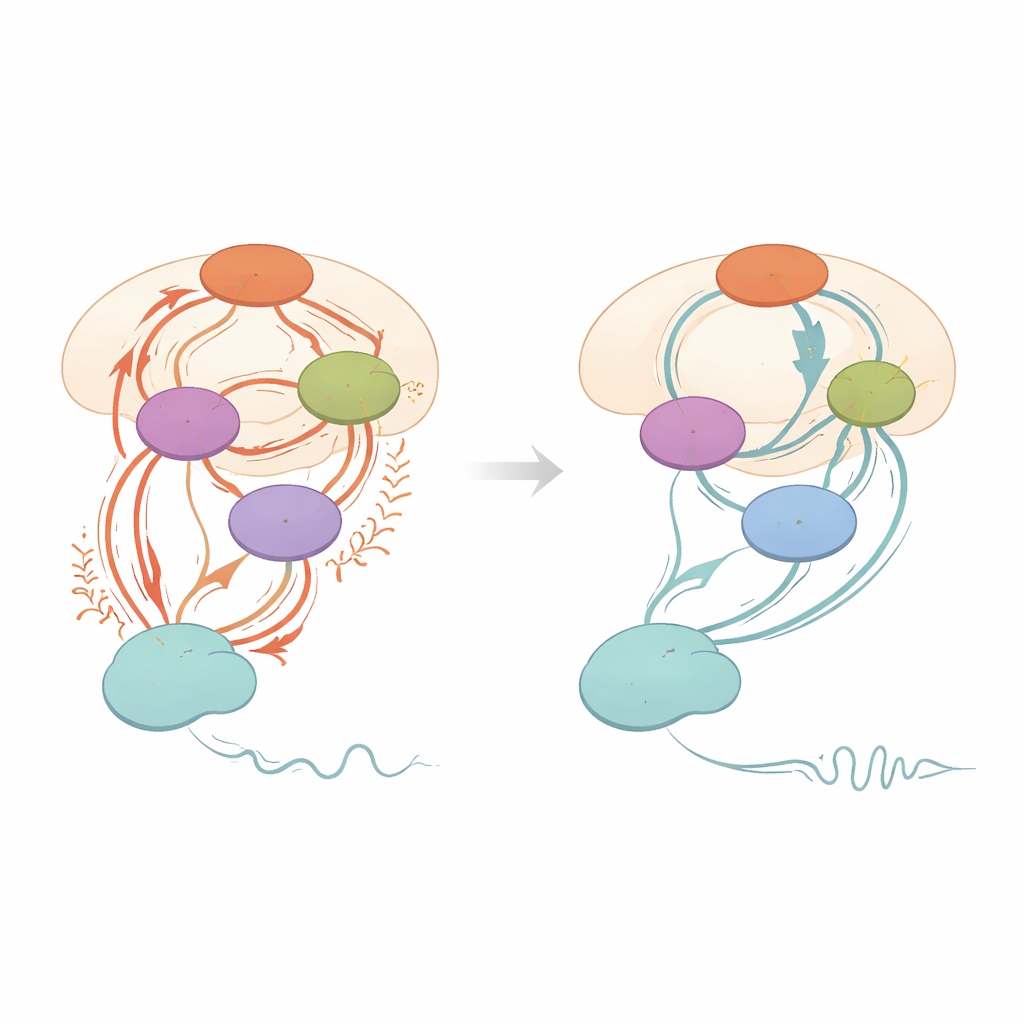
К шагу к персонализированной стимуляции мозга при болезни Паркинсона
Проще говоря, работа показывает, что стимуляция любой из двух тесно расположенных областей может успокаивать аномальный «трафик» в ключевых двигательных цепях и улучшать симптомы, но каждая мишень по‑своему влияет на сеть. STN-стимуляция сильнее воздействует на пути, связанные с общим контролем движения, тогда как PSA-стимуляция мощнее подавляет мозжечковые маршруты, связанные с поддержанием тремора. Размещение современных управляемых электродов вдоль границы между этими зонами может позволить клиницистам «смешивать» стимуляцию — направляя ток больше в сторону STN при ригидности и замедленности, или больше в сторону PSA при упорном треморе. Хотя исследование небольшое и сосредоточено на краткосрочных эффектах, оно даёт механистическую карту для превращения DBS из универсальной процедуры в более точную, управляемую с точки зрения цепей терапию для людей с тремор-доминантной формой болезни Паркинсона.
Цитирование: Lin, Z., Zeng, Z., Duan, C. et al. Impact of PSA- versus STN-DBS on effective connectivity in Parkinson’s disease – a 3.0T resting-state fMRI study. npj Parkinsons Dis. 12, 92 (2026). https://doi.org/10.1038/s41531-026-01305-y
Ключевые слова: Болезнь Паркинсона, глубокая мозговая стимуляция, субталамическое ядро, задняя субталамическая область, связность мозга