Clear Sky Science · de
Auswirkung von PSA- vs. STN-DBS auf effektive Konnektivität bei Parkinson – eine 3,0T Ruhe‑fMRI‑Studie
Warum diese Hirn‑OP‑Studie wichtig ist
Bei Menschen mit Parkinson kann elektrische Stimulation tief im Gehirn das Zittern deutlich beruhigen und die Muskelsteifigkeit lindern. Chirurgen haben bereits ein gut erprobtes Ziel, den subthalamischen Nukleus (STN), doch eine benachbarte Region – die posteriore subthalamische Area (PSA) – gilt zunehmend als vielversprechende Alternative, insbesondere bei patienten, deren Hauptproblem Tremor ist. Diese Studie nutzt moderne Hirnbildgebung, um zu beobachten, wie jede dieser beiden Stimulationsstellen die Kommunikation im Gehirn umgestaltet, mit dem Ziel, künftige Behandlungsentscheidungen stärker zu individualisieren.
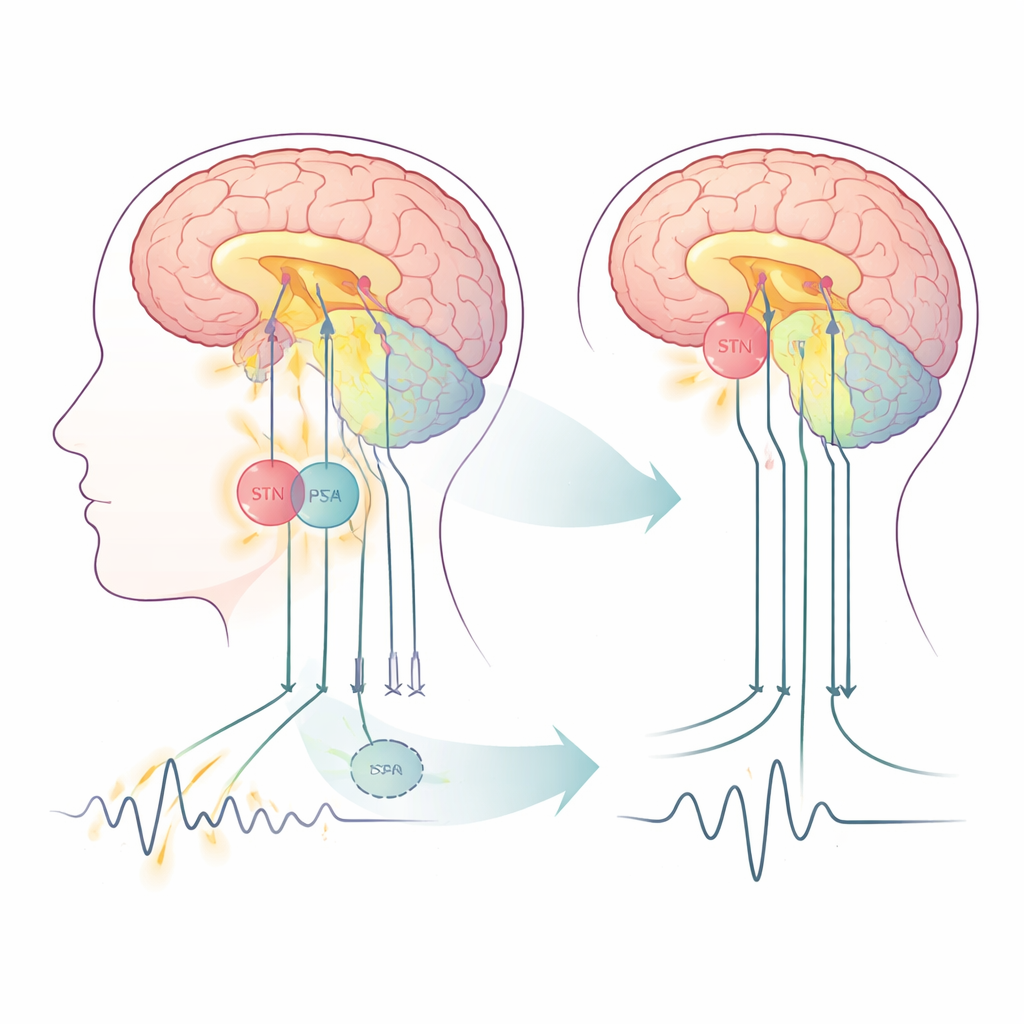
Zwei nahe Schaltstellen im Bewegungsnetzwerk
Die Parkinson‑Erkrankung stört ein Netz von Hirnschaltkreisen, die die Bewegung steuern, und umfasst die Großhirnrinde, tiefere Strukturen der Basalganglien und eine „Feinabstimmungs‑“Region im hinteren Gehirn, das Kleinhirn. Die Tiefenhirnstimulation (DBS) liefert schnelle elektrische Impulse über implantierte Elektroden und ist bereits eine etablierte Therapie, wenn Medikamente nicht mehr ausreichen. Traditionell ist der STN das Hauptziel. Die PSA, eine faserreiche Zone unmittelbar hinter und oberhalb des STN, gewinnt an Interesse, weil sie starke Verbindungen zu tremorbezogenen Bahnen hat. In dieser Studie erhielten fünfzehn Menschen mit tremordominantem Parkinson ein einzelnes Elektrodenpaar so platziert, dass unterschiedliche Kontakte entweder den STN oder die PSA entlang derselben Bahn stimulieren konnten – was einen seltenen direkten Vergleich innerhalb derselben Gehirne erlaubt.
Ruhe‑Hirnverkehr hochauflösend beobachten
Die Forschenden scannten jede Person dreimal mit einem leistungsstarken 3‑Tesla‑MRT: vor der Operation, mit abgeschalteter Stimulation, und nach der Operation bei Stimulation entweder der PSA oder des STN. Alle Scans wurden in Ruhe ohne Bewegungsaufgabe durchgeführt, um die laufenden Aktivitätsmuster des Gehirns zu erfassen. Mithilfe der sogenannten Ruhe‑fMRT maßen sie langsame Schwankungen der Blutoxygenierung, die zugrundeliegende Nervenzellaktivität widerspiegeln. Anschließend wandten sie ein Modellierungsverfahren an, das nicht nur feststellt, ob Regionen verknüpft sind, sondern wie stark eine Region eine andere antreibt – bekannt als „effektive Konnektivität“. Modelliert wurden zwei Hauptschleifen: eine Cortex–Basalganglien‑Schleife, die an Start und Stop von Bewegung beteiligt ist, und eine Cortex–Kleinhirn–Thalamus‑Schleife, die als wichtig für Erhalt und Ausformung von Tremor gilt.
Gemeinsame beruhigende Effekte auf überaktive Verbindungen
Sowohl PSA‑ als auch STN‑Stimulation führten zu großen und klinisch bedeutsamen Verbesserungen der Bewegungswerte, einschließlich Tremor, Verlangsamung, Steifheit und Haltung, ohne in dieser kleinen Gruppe einen klaren Sieger bei der Gesamtbeschwerdelinderung. In den Netzwerken zeigten beide Ziele mehrere gemeinsame Effekte. Stimulation an beiden Stellen dämpfte einen direkten Weg von der Hauptbewegungsregion der Großhirnrinde hinab zum STN (der „hyperdirekte“ Input) und erhöhte die Tendenz des STN, seine eigene Aktivität zu bremsen. Beide Ziele reduzierten außerdem Signale, die vom Cortex zum Kleinhirn fließen. Wichtig ist, dass das Ausmaß, in dem dieser Cortex‑zu‑STN‑Weg beruhigt wurde, und die Verstärkung der Selbstkontrolle des STN mit der motorischen Verbesserung der Patienten korrelierten: stärkere Veränderungen in diesen Verbindungen gingen Hand in Hand mit größeren Zuwächsen an Geschwindigkeit und Gesamtmotorik.
Unterschiedliche Betonung tremorbezogener Schaltkreise
Trotz dieser gemeinsamen Muster formten die beiden Ziele das Netzwerk nicht identisch. PSA‑Stimulation führte zu einer stärkeren Reduktion der Cortex‑zum‑Kleinhirn‑Verbindung als die STN‑Stimulation und erhöhte die Kommunikation vom Striatum (einer weiteren Basalganglienstruktur) zum STN. Über alle Scan‑Bedingungen hinweg zeigten Personen mit stärkerem Tremor tendenziell stärkere zweiseitige Kopplungen mit Beteiligung des Kleinhirns, während Gesamt‑ und Bradykinese‑Werte (Verlangsamung) mit der Stärke der Cortex‑zu‑STN‑Verbindungen verknüpft waren. Diese Zusammenhänge stützen eine „Zwei‑Kreislauf‑“Sicht auf den Parkinson‑Tremor: Basalganglien‑Regionen wirken als Schalter, der den Tremor auslöst, während die kleinhirnzentrierte Schleife wie ein Dimmer dessen Intensität reguliert. Die Befunde legen nahe, dass PSA‑Stimulation besonders wirksam sein könnte, diesen Tremor‑"Dimmerschalter" herunterzuregeln, auch wenn sich dieser zusätzliche physiologische Effekt innerhalb der Grenzen dieser kleinen Studie noch nicht klar in besseren Tremorwerten gegenüber alleiniger STN‑Stimulation niedergeschlagen hat.
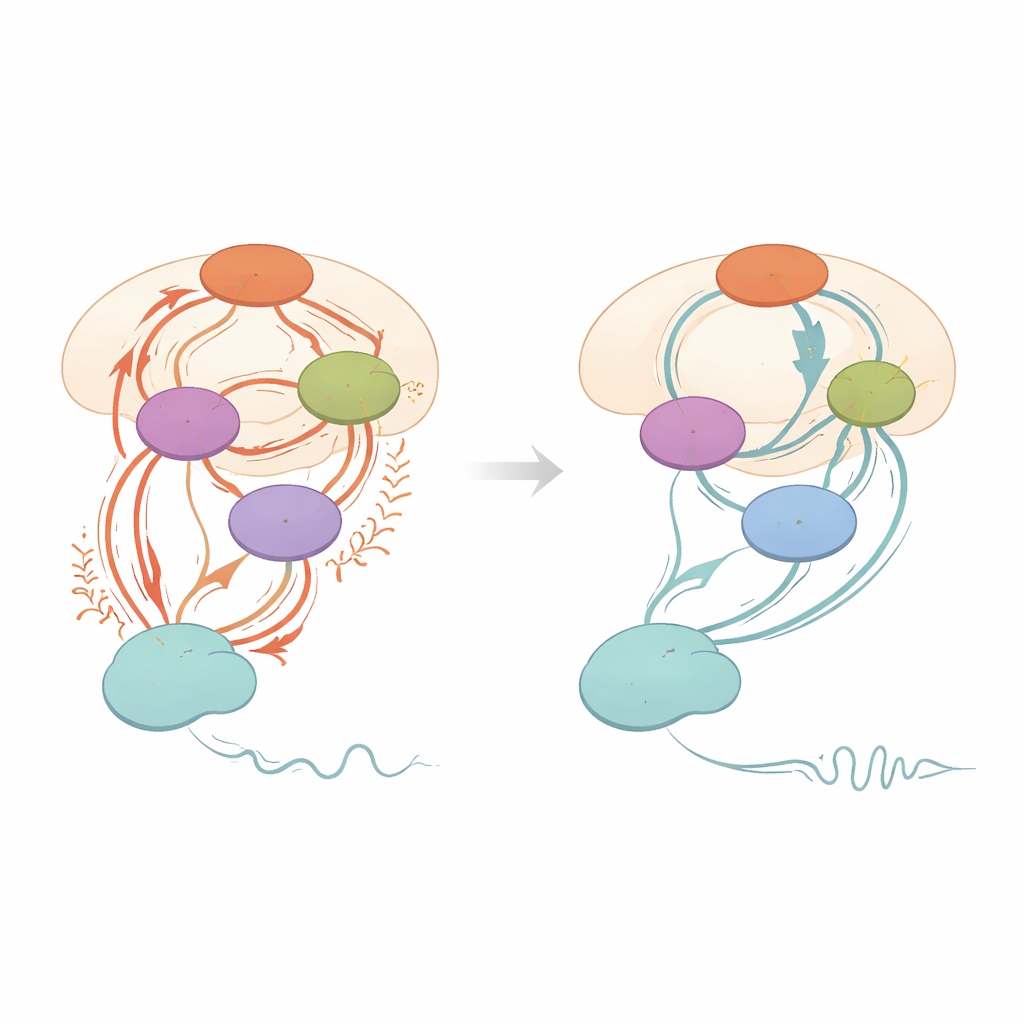
Auf dem Weg zu maßgeschneiderter Hirnstimulation bei Parkinson
Einfach gesagt zeigt diese Arbeit, dass die Stimulation einer von zwei dicht beieinander liegenden Hirnregionen abnormen Verkehr in wichtigen Bewegungsnetzwerken beruhigen und Symptome verbessern kann, wobei jedes Ziel das Netzwerk auf leicht unterschiedliche Weise beeinflusst. STN‑Stimulation wirkt stark auf Bahnen, die mit der Gesamtbewegungskontrolle verknüpft sind, während PSA‑Stimulation kraftvoller kleinhirnbezogene Routen dämpft, die mit der Aufrechterhaltung des Tremors zusammenhängen. Durch das Platzieren moderner, lenkbarer Elektroden entlang der Grenze zwischen diesen Bereichen könnten Kliniker eine „Mischung“ der Stimulation erreichen – Strom eher Richtung STN für Rigidität und Verlangsamung, oder eher Richtung PSA für hartnäckigen Tremor. Obwohl die Studie klein ist und sich auf kurzfristige Effekte konzentriert, bietet sie eine mechanistische Landkarte, um DBS von einem Einheitsverfahren in eine präzisere, schaltkreisgesteuerte Therapie für Menschen mit tremordominantem Parkinson weiterzuentwickeln.
Zitation: Lin, Z., Zeng, Z., Duan, C. et al. Impact of PSA- versus STN-DBS on effective connectivity in Parkinson’s disease – a 3.0T resting-state fMRI study. npj Parkinsons Dis. 12, 92 (2026). https://doi.org/10.1038/s41531-026-01305-y
Schlüsselwörter: Parkinson‑Krankheit, Tiefenhirnstimulation, subthalamischer Nukleus, posteriore subthalamische Region, Hirnkonnektivität