Clear Sky Science · nl
Effect van PSA- versus STN-DBS op effectieve connectiviteit bij de ziekte van Parkinson – een 3,0T rusttoestand fMRI-studie
Waarom deze hersenoperatiestudie ertoe doet
Voor mensen met de ziekte van Parkinson kan elektrische stimulatie diep in de hersenen het beven aanzienlijk stabiliseren en stijfheid verminderen. Chirurgen hebben al een goed onderzochte doelstructuur, de subthalamische kern (STN), maar een nabijgelegen gebied — het posterieure subthalamische gebied (PSA) — is naar voren gekomen als een veelbelovende alternatieve doelplaats, vooral voor patiënten bij wie tremor het belangrijkste probleem is. Deze studie gebruikt geavanceerde hersenscans om te volgen hoe elk van deze twee stimulatieplaatsen de communicatie binnen de hersenen verandert, met het oog op meer gepersonaliseerde behandelingskeuzes in de toekomst.
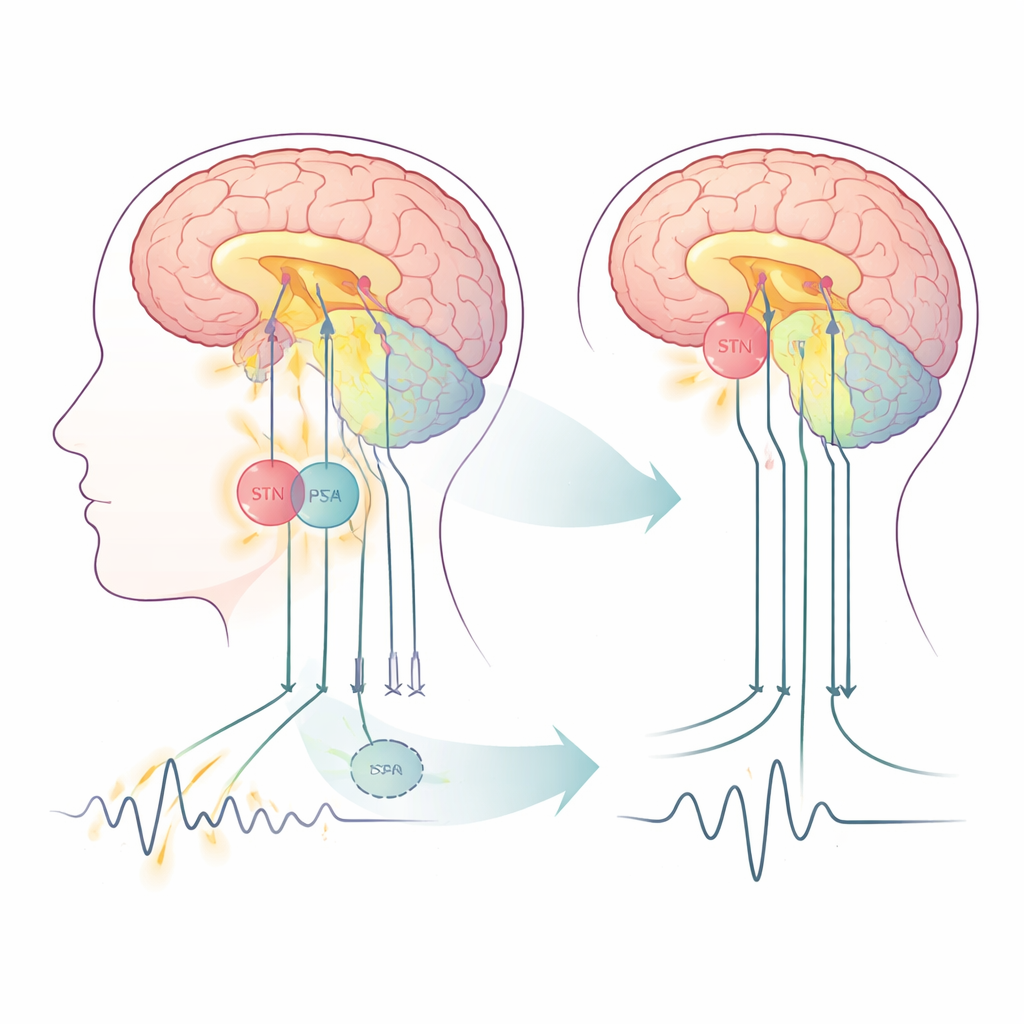
Twee nabije schakelaars in het bewegingsnetwerk
De ziekte van Parkinson verstoort een reeks hersencircuits die beweging aansturen, waarbij de buitenste hersenschors (cortex), diepere structuren die de basale ganglia worden genoemd, en een "fijnsturende" regio achterin de hersenen, het cerebellum, betrokken zijn. Deep brain stimulation (DBS) levert snelle elektrische pulsen via geïmplanteerde elektroden en is al een gevestigde behandeling wanneer medicijnen niet langer voldoende zijn. Traditioneel is de STN het belangrijkste doel. De PSA, een vezelrijk gebied net achter en boven de STN, krijgt steeds meer aandacht omdat het sterk verbonden is met tremor-gerelateerde banen. In deze studie kregen vijftien mensen met tremordominante Parkinson één paar elektroden geplaatst langs zodanig dat verschillende contacten ofwel STN ofwel PSA konden stimuleren langs hetzelfde traject, waardoor een zeldzame head-to-head vergelijking binnen dezelfde hersenen mogelijk werd.
Rustend hersenverkeer observeren op hoge resolutie
De onderzoekers scanden iedere deelnemer driemaal met een krachtige 3-Tesla MRI-scanner: vóór de operatie, met stimulatie uit, en na de operatie terwijl ofwel de PSA ofwel de STN werd gestimuleerd. Alle scans werden in rust uitgevoerd, zonder bewegingsopdracht, om de voortdurende activiteitspatronen van de hersenen vast te leggen. Met een techniek genaamd rusttoestand-functionele MRI maten zij langzame schommelingen in bloedzuurstof die de onderliggende zenuwcelactiviteit weerspiegelen. Vervolgens pasten ze een modelleringsbenadering toe die niet alleen bepaalt of regio’s verbonden zijn, maar ook hoe sterk de ene regio de andere aanstuurt — bekend als "effectieve connectiviteit." Twee hoofdloops werden gemodelleerd: een cortex–basale ganglia-loop die betrokken is bij het starten en stoppen van beweging, en een cortex–cerebellum–thalamus-loop waarvan wordt gedacht dat deze tremor in stand houdt en vormgeeft.
Gedeelde kalmerende effecten op overactieve verbindingen
Zowel PSA- als STN-stimulatie leidden tot grote en klinisch betekenisvolle verbeteringen in bewegingsscores, inclusief tremor, traagheid, stijfheid en houding, zonder duidelijke winnaar qua algemene symptoomverlichting in deze kleine groep. In de hersennetwerken toonden de twee doelplaatsen meerdere gemeenschappelijke effecten. Stimulatie op beide locaties dempte een directe baan van het belangrijkste bewegingsgebied van de cortex naar de STN (de zogeheten "hyperdirecte" input), en vergrootte de neiging van de STN om zijn eigen activiteit terug te schakelen. Beide doelen verminderden ook signalen van de cortex naar het cerebellum. Belangrijk is dat de mate waarin deze cortex‑naar‑STN-baan werd stilgelegd en de versterking van de zelfregulatie van de STN samenhingen met hoe veel beter patiënten bewoog: sterkere veranderingen in deze verbindingen gingen hand in hand met grotere verbeteringen in snelheid en totale motorische scores.
Verschillende nadruk op tremor-gerelateerde circuits
Ondanks deze gedeelde patronen waren de twee doelplaatsen niet identiek in hoe ze het netwerk vormgaven. PSA-stimulatie veroorzaakte een sterkere reductie van de cortex‑naar‑cerebellum-verbinding dan STN-stimulatie, en versterkte de communicatie van het striatum (een andere basale gangliastruktuur) naar de STN. Over alle scancondities lieten mensen met ernstiger tremor doorgaans sterkere tweerichtingskoppeling zien waarbij het cerebellum betrokken was, terwijl de totale scores en bradykinesie (traagheid) gerelateerd waren aan de sterkte van cortex‑naar‑STN-verbindingen. Deze relaties ondersteunen een "twee‑circuit"-visie op Parkinson-tremor: basale ganglia fungeren als een schakelaar die tremor activeert, terwijl de cerebellum‑gecentreerde lus als een dimmer werkt die de intensiteit reguleert. De bevindingen suggereren dat PSA-stimulatie bijzonder effectief kan zijn in het terugdraaien van deze tremor‑"dimmer", ook al vertaalde dat extra fysiologische effect binnen de grenzen van deze kleine studie nog niet duidelijk in betere tremorscores dan STN-stimulatie alleen.
Op weg naar op maat gemaakte hersenstimulatie voor Parkinson
In eenvoudige bewoordingen laat dit werk zien dat stimulatie van twee dicht bij elkaar gelegen hersenregio’s abnormaal verkeer in sleutelcircuits voor beweging kan kalmeren en symptomen kan verbeteren, maar dat elk doel het netwerk op een iets andere manier beïnvloedt. STN-stimulatie beïnvloedt paden die verband houden met algemene bewegingscontrole sterk, terwijl PSA-stimulatie krachtiger cerebellaire routes dempt die gekoppeld zijn aan het in stand houden van tremor. Door moderne, stuurbare elektroden langs de grens tussen deze gebieden te plaatsen, kunnen clinici mogelijk "blended" stimulatie toepassen — meer stroom richting de STN voor rigiditeit en traagheid, of meer richting de PSA voor hardnekkige tremor. Hoewel de studie klein is en gericht op kortetermijneffecten, biedt zij een mechanistische routekaart om DBS te veranderen van een one-size-fits-all-procedure in een preciezere, circuitgeïntegreerde therapie voor mensen met tremordominante ziekte van Parkinson.
Bronvermelding: Lin, Z., Zeng, Z., Duan, C. et al. Impact of PSA- versus STN-DBS on effective connectivity in Parkinson’s disease – a 3.0T resting-state fMRI study. npj Parkinsons Dis. 12, 92 (2026). https://doi.org/10.1038/s41531-026-01305-y
Trefwoorden: Ziekte van Parkinson, deep brain stimulation, subthalamische kern, posterieure subthalamische gebied, hersenconnectiviteit