Clear Sky Science · es
Impacto de la ECP-PSA frente a la ECP-STN en la conectividad eficaz en la enfermedad de Parkinson: estudio de reposo con IRMf a 3.0T
Por qué importa este estudio sobre cirugía cerebral
Para las personas con enfermedad de Parkinson, la estimulación eléctrica en lo profundo del cerebro puede reducir de forma notable las manos temblorosas y aliviar la rigidez. Los cirujanos ya cuentan con un objetivo bien estudiado, el núcleo subtalámico (STN), pero una región cercana —la zona subtalámica posterior (PSA)— ha surgido como alternativa prometedora, sobre todo en pacientes cuyo problema principal es el temblor. Este estudio emplea técnicas avanzadas de imagen cerebral para observar cómo cada uno de estos dos puntos de estimulación reorganiza la comunicación dentro del cerebro, con la vista puesta en opciones de tratamiento más personalizadas en el futuro.
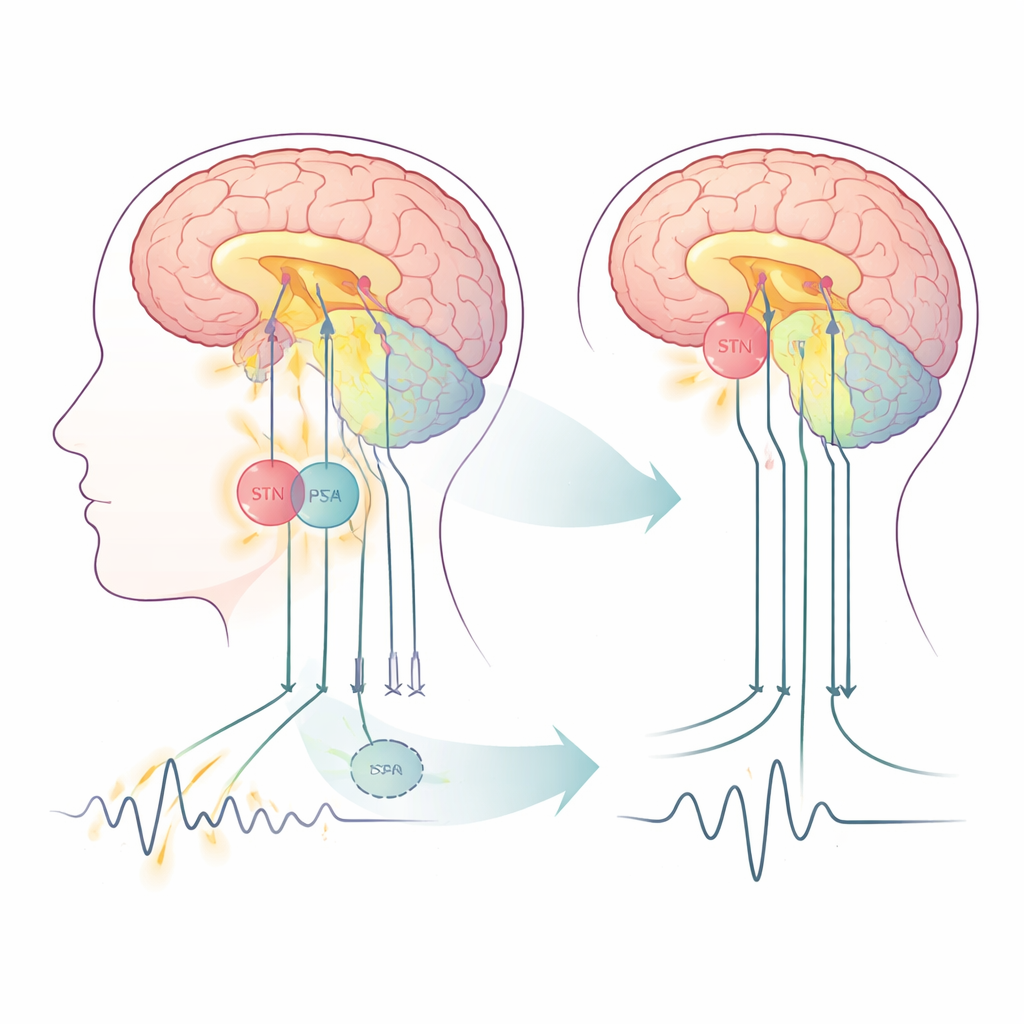
Dos interruptores vecinos en la red del movimiento
La enfermedad de Parkinson altera un conjunto de circuitos cerebrales que controlan el movimiento, que abarcan la corteza (la superficie cerebral), estructuras profundas llamadas ganglios basales y una región de “afinamiento” en la parte posterior del cerebro, el cerebelo. La estimulación cerebral profunda (DBS) administra pulsos eléctricos rápidos a través de electrodos implantados y ya es un tratamiento establecido cuando la medicación no es suficiente. Tradicionalmente, el STN ha sido el objetivo principal. La PSA, una zona rica en fibras situada justo detrás y por encima del STN, suscita interés porque se conecta fuertemente con las vías relacionadas con el temblor. En este estudio, quince personas con Parkinson dominante en temblor recibieron un único par de electrodos colocados de modo que distintos contactos pudieran estimular ya sea el STN o la PSA a lo largo del mismo trayecto, lo que permitió una rara comparación cara a cara dentro de los mismos cerebros.
Vigilar el tráfico cerebral en reposo con alta resolución
Los investigadores escanearon a cada participante tres veces con un potente escáner de 3 teslas: antes de la cirugía, con la estimulación apagada, y después de la cirugía mientras se estimulaba ya la PSA o el STN. Todos los escaneos se realizaron en reposo, sin tareas de movimiento, para capturar los patrones de actividad cerebral en curso. Usando una técnica llamada resonancia magnética funcional en estado de reposo (IRMf), midieron fluctuaciones lentas en la oxigenación de la sangre que reflejan la actividad neuronal subyacente. A continuación aplicaron un enfoque de modelado que estima no solo si las regiones están conectadas, sino cómo de fuertemente una región influye sobre otra —lo que se conoce como “conectividad eficaz”. Se modelaron principalmente dos circuitos: un bucle corteza–ganglios basales implicado en iniciar y detener el movimiento, y un bucle corteza–cerebelo–tálamo pensado para mantener y dar forma al temblor.
Efectos calmantes compartidos sobre enlaces hiperactivos
Tanto la estimulación de la PSA como la del STN produjeron mejoras grandes y clínicamente relevantes en las puntuaciones motoras, incluyendo temblor, lentitud, rigidez y postura, sin un vencedor claro en el alivio global de los síntomas en este pequeño grupo. En las redes cerebrales, ambos objetivos mostraron varios efectos comunes. La estimulación en cualquiera de los dos sitios atenuó una vía directa desde la principal zona motora de la corteza hacia el STN (entrada “hiperdirecta”) y aumentó la tendencia del STN a inhibir su propia actividad. Ambos objetivos también redujeron las señales que fluyen desde la corteza al cerebelo. Es importante que el grado en que se silenciaba la vía corteza→STN y el fortalecimiento del autocontrol del STN se relacionaron con la mejora motora: cambios más pronunciados en estas conexiones fueron acompañados por mayores ganancias en velocidad y en las puntuaciones motoras totales.
Diferente énfasis en los circuitos relacionados con el temblor
A pesar de estos patrones compartidos, los dos objetivos no fueron idénticos en cómo moldearon la red. La estimulación de la PSA produjo una reducción más marcada de la conexión corteza→cerebelo que la estimulación del STN y potenció la comunicación desde el cuerpo estriado (otra estructura de los ganglios basales) hacia el STN. En todas las condiciones de escaneo, las personas con temblor más intenso tendieron a mostrar un acoplamiento bidireccional más fuerte que involucraba al cerebelo, mientras que las puntuaciones globales y las de bradicinesia (lentitud) se asociaron con la fuerza de las conexiones corteza→STN. Estas relaciones respaldan una visión de “dos circuitos” del temblor parkinsoniano: las regiones de los ganglios basales actúan como un interruptor que desencadena el temblor, mientras que el bucle centrado en el cerebelo funciona como un regulador que controla su intensidad. Los hallazgos sugieren que la estimulación de la PSA podría ser especialmente eficaz para reducir este “regulador” del temblor, aunque, dentro de los límites de este estudio pequeño, ese efecto fisiológico adicional aún no se tradujo en puntuaciones de temblor claramente superiores a las de la estimulación del STN.
Hacia una estimulación cerebral personalizada para el Parkinson
En términos sencillos, este trabajo muestra que estimular cualquiera de dos regiones cerebrales muy próximas puede calmar el tráfico anómalo en circuitos clave del movimiento y mejorar los síntomas, pero cada objetivo empuja la red de manera ligeramente distinta. La estimulación del STN afecta con fuerza a las vías vinculadas al control global del movimiento, mientras que la estimulación de la PSA atenúa con mayor potencia las rutas cerebelosas asociadas al mantenimiento del temblor. Al colocar electrodos modernos y dirigibles a lo largo de la frontera entre estas áreas, los clínicos podrían “mezclar” la estimulación: dirigir más corriente hacia el STN para rigidez y lentitud, o más hacia la PSA para temblores rebeldes. Aunque el estudio es pequeño y se centra en efectos a corto plazo, ofrece una hoja de ruta mecanicista para transformar la DBS de un procedimiento único en una terapia más precisa y guiada por circuitos para personas con enfermedad de Parkinson dominante en temblor.
Cita: Lin, Z., Zeng, Z., Duan, C. et al. Impact of PSA- versus STN-DBS on effective connectivity in Parkinson’s disease – a 3.0T resting-state fMRI study. npj Parkinsons Dis. 12, 92 (2026). https://doi.org/10.1038/s41531-026-01305-y
Palabras clave: enfermedad de Parkinson, estimulación cerebral profunda, núcleo subtalámico, zona subtalámica posterior, conectividad cerebral