Clear Sky Science · ru
Скрининг целых белков и мульти‑модальное профилирование антиген‑специфичных CD4+ T‑клеток с разрешением до одной клетки
Почему это важно для здравоохранения и онкологической помощи
Наша иммунная система опирается на хелперные клетки, которые координируют атаки на вирусы и опухоли, но учёным трудно подробно отслеживать эти клетки. В этом исследовании предложен мощный лабораторный метод, способный обнаруживать редкие хелперные T‑клетки в крови, определять, что именно они распознают, и считывать их поведение по одной клетке. Работа может повысить точность разработки вакцин и поддержать создание новых клеточных терапий против инфекций, таких как COVID‑19, и опухолей, связанных с вирусом папилломы человека (ВПЧ).
Нахождение дирижёров иммунитета
Хелперные T‑клетки, также называемые CD4+ T‑клетками, действуют как дирижёры иммунного оркестра. Они реагируют, когда другие клетки показывают им короткие фрагменты вирусов или опухолевых белков, и в ответ помогают B‑клеткам‑продуцентам антител, киллерам‑T‑клеткам и другим защитникам выполнять их функции. Исследовать этих дирижёров было сложно, потому что каждая клетка распознаёт слегка отличающуюся белковую фрагментацию, а существующие инструменты для поиска в крови либо искажают их естественное состояние, либо могут тестировать лишь небольшое число мишеней одновременно. Авторы поставили задачу создать метод, который мог бы просканировать целые белки, поймать релевантные хелперные клетки непосредственно из крови и за один проход прочитать как их генетические программы, так и уникальные T‑клеточные рецепторы.

Создание библиотеки белков для хелперных клеток
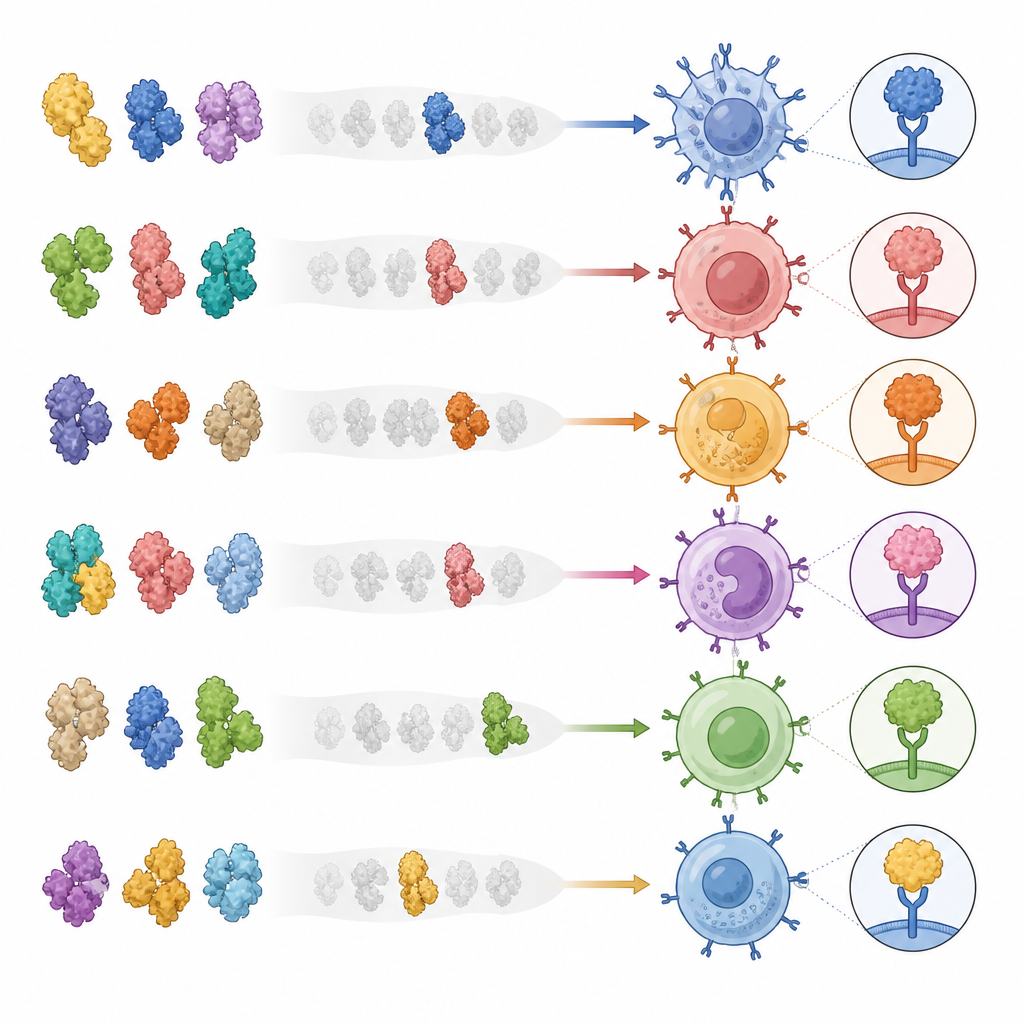
Команда создала большую библиотеку искусственных белковых комплексов, имитирующих то, что показывают иммунные клетки хелперным T‑клеткам. Каждый комплекс содержит определённый фрагмент вирусного или опухолевого белка в фиксированной форме, прикреплённый к человеческой молекуле‑дисплею. Объединяя части в единую цепь, они упростили массовое производство сотен различных комплексов в культурах человеческих клеток без необходимости синтезировать каждый пептид по отдельности. Авторы продемонстрировали, что эти комплексы связываются только с соответствующими хелперными T‑клетками, работают через несколько распространённых типов генов HLA и могут обнаруживать даже редкие клетки в крови при очень низкой частоте. Важно, что связывание с этими комплексами также предсказывало реактивность тех же T‑клеток при презентации мишеней живыми клетками, а не только в искусственных тестах.
Отслеживание хелперных клеток против COVID‑19 во времени
Имея эту платформу, исследователи просканировали весь рецептор‑связывающий домен спайк‑белка SARS‑CoV‑2 вместе с другими вирусными регионами в образцах крови 22 человек, переболевших COVID‑19. С помощью штрихкодов и секвенирования по одной клетке они захватили 2 188 вирус‑специфичных хелперных T‑клеток и выяснили для каждой клетки, какой вирусный фрагмент она распознаёт, какой ген HLA его предъявляет, как выглядит её T‑клеточный рецептор и какие гены она экспрессирует. Набор состояний клеток оказался разнообразным: клетки с фенотипом памяти, эффекторные, регуляторные и схожие на истощённые. Со временем ответы склонялись в сторону эффекторной памяти, но в способе, отличающемся от ранее изученных киллерных T‑клеток. Команда разработала «оценку иммуногенности», объединяющую, сколько людей и клонов T‑клеток откликнулись на тот или иной вирусный фрагмент, насколько расширялись эти клоны и как долго они сохранялись. Более высокие оценки для фрагментов рецептор‑связывающего домена спайка коррелировали с более сильными уровнями антител позднее, что указывает на то, что эти хелперные клетки могут поддерживать более высокое качество антител.
Поиск хелперных клеток против ВПЧ для онкотерапии
Затем исследователи обратились к онкологии, сосредоточившись на ВПЧ‑16, одной из основных причин рака шейки матки и других опухолей. Они создали библиотеку, покрывающую два белка ВПЧ, E6 и E7, используя фрагменты разной длины, чтобы исследовать, как «окружающие» области вокруг центрального ядра влияют на распознавание хелперными T‑клетками. Эту библиотеку применили к пациентам с предраковыми поражениями, получившим терапевтические ВПЧ‑вакцины, и идентифицировали десятки ВПЧ‑специфичных хелперных T‑клеток. Из них они отобрали панель T‑клеточных рецепторов для углублённых испытаний. Некоторые рецепторы продемонстрировали сильные и селективные ответы при переносе в человеческие T‑клетки, вырабатывая несколько полезных сигналов и убивая целевые клетки, загруженные фрагментами ВПЧ или полным белком E6, при этом практически не реагируя на похожие человеческие белки или на широкий набор других типов HLA. Один рецептор в исследовании, обозначенный как H2, выделился как перспективный кандидат для будущих терапий с инженерными T‑клетками.
Что это значит для будущих вакцин и терапий
Для неспециалистов ключевая мысль такова: авторы создали нечто вроде «поисковой системы» по хелперным T‑клеткам. Она может просматривать целые белки вирусов или опухолей, вычленять редкие клетки, распознающие конкретные фрагменты, и одновременно показывать, как эти клетки себя ведут и как их можно использовать. В случае COVID‑19 этот подход связал определённые фрагменты спайка с сильными ответами хелперных клеток и более высоким уровнем антител, давая подсказки для улучшения вакцин. В заболеваниях, связанных с ВПЧ, метод выявил T‑клеточные рецепторы, которые выглядят достаточно мощными и безопасными, чтобы рассматривать их для таргетной онко‑иммунотерапии. Хотя требуется дополнительная работа для расширения метода на другие типы HLA и большие когорты пациентов, платформа открывает практический путь к картированию и в конечном счёте направлению хелперной ветви иммунной системы при многих заболеваниях.
Цитирование: Zhang, R., Qi, J., McKasson, M. et al. Whole-protein screening and multi-modal profiling of antigen-specific CD4+ T cells at single-cell resolution. Nat Commun 17, 3979 (2026). https://doi.org/10.1038/s41467-026-72396-7
Ключевые слова: CD4 T cells, single-cell profiling, SARS-CoV-2 immunity, HPV immunotherapy, T cell receptors