Clear Sky Science · ja
全タンパク質スクリーニングと抗原特異的CD4+ T細胞の単一細胞レベルでの多モーダル解析
健康とがん治療にとっての意義
私たちの免疫系はウイルスや腫瘍への攻撃を調整するヘルパー細胞に依存していますが、これらの細胞を詳細に追跡することはこれまで困難でした。本研究は、血液中の希少なヘルパーT細胞を見つけ出し、それが何を認識するかを特定し、個々の細胞ごとに挙動を読み取る強力な実験手法を提示します。この手法はワクチン設計を洗練し、COVID-19のような感染症やヒトパピローマウイルス(HPV)に関連するがんに対する新たな細胞療法の支援につながる可能性があります。
免疫の指揮者を見つける
ヘルパーT細胞、つまりCD4+ T細胞は免疫オーケストラの指揮者のように働きます。これらは他の細胞が提示するウイルスやがんタンパク質の短い断片に応答し、抗体を作るB細胞やキラーT細胞などの働きを助けます。こうした指揮者を研究するのは難しく、各細胞がわずかに異なるタンパク断片を認識するうえ、血液中でそれらを見つける既存のツールは自然な状態を乱すか、一度に扱える標的が限られていました。著者らは全タンパク質を検索でき、血液から該当するヘルパー細胞を直接捕獲し、同時に遺伝子発現プログラムと固有のT細胞受容体を一度に読み取れる方法を構築しようとしました。

ヘルパー細胞のためのタンパク質ライブラリの構築
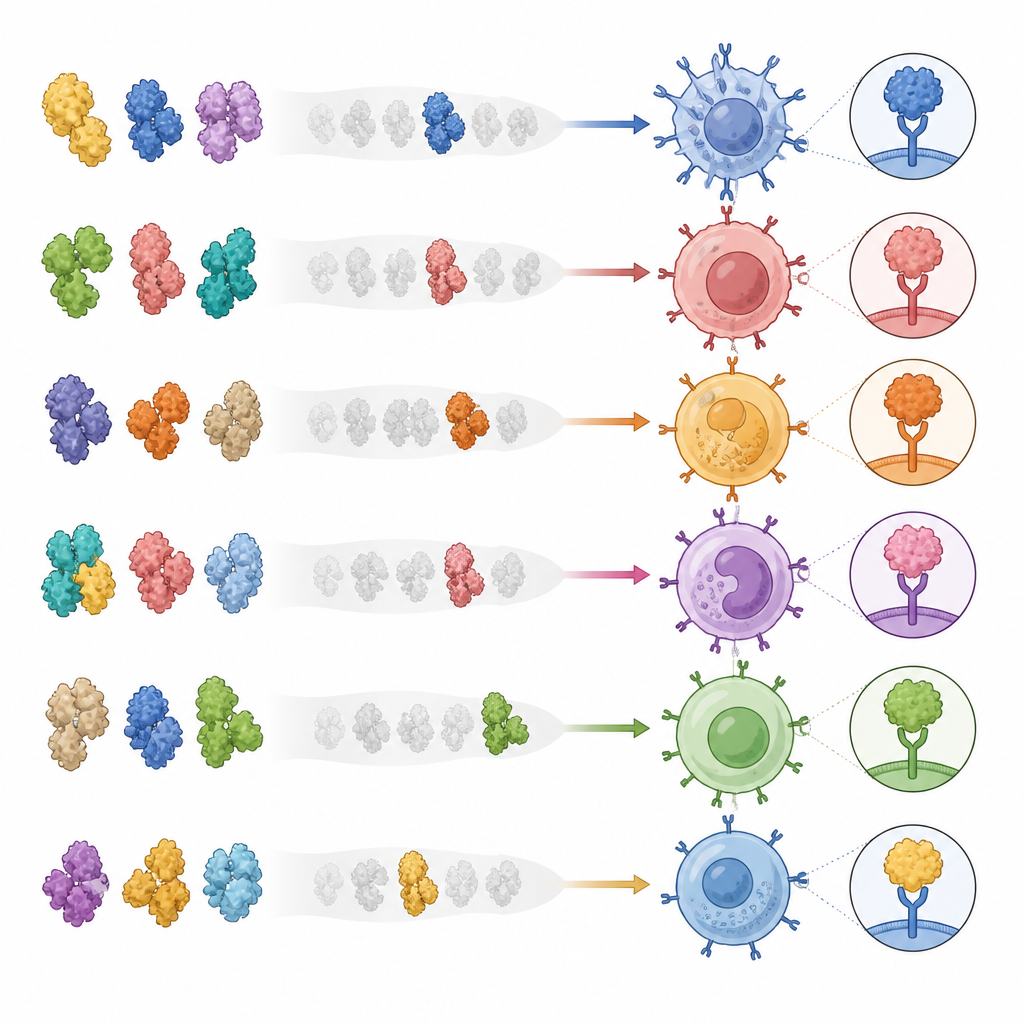
研究チームは、ヘルパーT細胞に提示されるものを模した大規模な人工タンパク質複合体のライブラリを設計しました。それぞれの複合体はウイルスやがんタンパク質由来の特定の断片を固定された形で保持し、人の提示分子に結合しています。部品を一本鎖に連結することで、個々のペプチドを別々に合成する必要なく、人細胞培養系で数百種類の複合体を大量生産しやすくしました。これらの複合体は一致するヘルパーT細胞にのみ結合し、複数の一般的なHLA型で機能し、血液中でごく低頻度の希少細胞も検出できることを示しました。重要なのは、これらの複合体への結合が、人工系だけでなく生きた細胞上で標的が提示された場合にも同じT細胞が応答することを予測した点です。
COVID-19ヘルパー細胞の時間経過追跡
このプラットフォームを用いて、研究者らはSARS-CoV-2スパイクタンパク質の受容体結合ドメイン全体や他のウイルス領域を、COVID-19既往の22名の血液サンプルで走査しました。バーコードと単一細胞シーケンスを活用して、2,188個のウイルス特異的ヘルパーT細胞を捕捉し、各細胞がどのウイルス断片を認識し、どのHLA遺伝子が提示しており、T細胞受容体の形状や発現している遺伝子が何であるかを明らかにしました。記憶様、エフェクター、制御性、疲弊様など多様な細胞状態が観察されました。時間経過とともに反応はエフェクターメモリー細胞へ移行する傾向がありましたが、以前に研究されたキラーT細胞とは異なる様相を示しました。研究チームは“免疫原性スコア”を作成し、あるウイルス断片に対して何人と何クローンのT細胞が反応したか、そのクローンがどれだけ増殖したか、どれだけ持続したかを組み合わせて評価しました。スパイク受容体結合ドメイン断片のスコアが高いほど、後の抗体レベルが強かったことと関連し、これらのヘルパー細胞が抗体の質を支える可能性を示唆しました。
がん治療を目指したHPVヘルパー細胞の探索
次に研究者らはがんに着目し、子宮頸がんなどの主要原因であるHPV-16に焦点を当てました。彼らはHPVのE6およびE7という二つのタンパク質全体をタイル状に網羅するライブラリを構築し、中心となるコア周辺の“フランキング”領域がヘルパーT細胞の認識にどのように影響するかを、異なる長さの断片で調べました。このライブラリを治療用HPVワクチンを受けた前癌病変の患者に適用し、数十のHPV特異的ヘルパーT細胞を同定しました。そこからさらにT細胞受容体の候補パネルを選び出し、詳細に試験しました。いくつかの受容体はヒトT細胞に導入した際に強く選択的に応答し、複数の有益なシグナルを産生し、HPV断片や全長E6タンパク質を載せた標的細胞を殺傷しました。一方で類似するヒトタンパク質や多様なHLA型に対してはほとんど反応を示さないものもありました。研究で“H2”と名付けられた受容体は、将来の遺伝子改変T細胞療法の有望候補として際立ちました。
将来のワクチンと療法にとっての意味
専門外の読者にとっての要点は、著者らがヘルパーT細胞のための一種の「免疫サーチエンジン」を構築したことです。ウイルスやがんの全タンパク質を横断的に検索し、特定の断片を認識する希少な細胞を引き出し、それらの細胞の振る舞いと利用可能性を同時に明らかにできます。COVID-19では、このアプローチが特定のスパイク断片と強いヘルパー細胞応答および高い抗体レベルを結びつけ、ワクチン改良の手掛かりを提供しました。HPV関連疾患では、強力で安全性が期待できるヘルパーT細胞受容体を同定し、標的化がん免疫療法の候補を示しました。さらに多くのHLA型やより大規模な患者集団への適用が必要ですが、このプラットフォームは多くの疾患でヘルパー免疫の地図化と制御に向けた実用的な道筋を開きます。
引用: Zhang, R., Qi, J., McKasson, M. et al. Whole-protein screening and multi-modal profiling of antigen-specific CD4+ T cells at single-cell resolution. Nat Commun 17, 3979 (2026). https://doi.org/10.1038/s41467-026-72396-7
キーワード: CD4 T細胞, 単一細胞プロファイリング, SARS-CoV-2免疫, HPV免疫療法, T細胞受容体