Clear Sky Science · pl
Badanie całych białek i wielomodalne profilowanie swoistych dla antygenu limfocytów CD4+ na poziomie pojedynczych komórek
Dlaczego to ma znaczenie dla zdrowia i opieki onkologicznej
Nasz układ odpornościowy polega na komórkach pomocniczych, które koordynują ataki na wirusy i guzy, jednak naukowcy mieli trudności ze śledzeniem tych komórek w detalach. W tym badaniu wprowadzono wydajną metodę laboratoryjną, która potrafi wykryć rzadkie limfocyty pomocnicze we krwi, ustalić dokładnie, co rozpoznają, i odczytać ich zachowanie komórka po komórce. Praca ta może udoskonalić projektowanie szczepionek i wesprzeć nowe terapie komórkowe przeciwko infekcjom takim jak COVID-19 oraz nowotworom powiązanym z ludzkim wirusem brodawczaka (HPV).
Odnajdywanie dyrygentów odporności
Komórki pomocnicze, zwane też limfocytami CD4+, pełnią rolę dyrygentów orkiestry odpornościowej. Reagują, gdy inne komórki prezentują im krótkie fragmenty wirusów lub białek nowotworowych, a w zamian wspierają komórki B produkujące przeciwciała, cytotoksyczne limfocyty T i inne elementy obrony. Badanie tych „dyrygentów” było trudne, ponieważ każda komórka rozpoznaje nieco inny fragment białka, a narzędzia do ich wykrywania we krwi albo zakłócają ich naturalny stan, albo pozwalają jednocześnie testować niewielką liczbę celów. Autorzy postawili sobie za cel zbudowanie metody, która przeszuka całe białka, wyłapie odpowiednie komórki pomocnicze bezpośrednio z krwi i jednocześnie odczyta ich programy genetyczne oraz unikatowe receptory komórek T.

Budowa biblioteki białek dla komórek pomocniczych
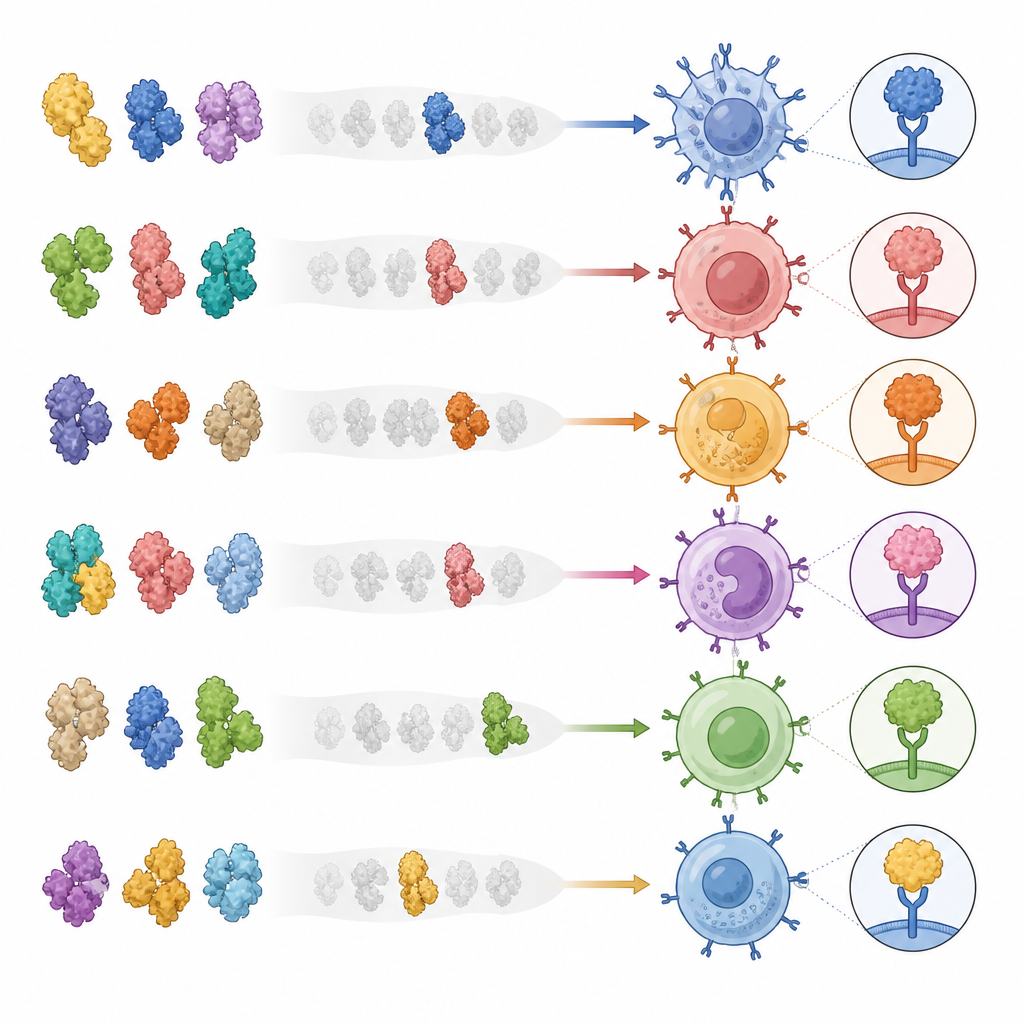
Zespół skonstruował dużą bibliotekę sztucznych kompleksów białkowych, które naśladują to, co komórki prezentują komórkom pomocniczym. Każdy kompleks utrzymuje określony fragment białka wirusa lub nowotworu w ustalonej konformacji, połączony z ludzką cząsteczką prezentującą. Łącząc elementy w pojedynczy łańcuch, ułatwili masową produkcję setek różnych kompleksów w hodowlach komórek ludzkich bez konieczności wytwarzania każdego peptydu osobno. Pokazali, że te kompleksy wiążą tylko dopasowane komórki pomocnicze, działają w kontekście kilku powszechnych typów genów HLA i potrafią wykrywać nawet rzadkie komórki we krwi przy bardzo niskich częstościach. Co ważne, wiązanie do tych kompleksów przewidywało również, że te same limfocyty zareagują, gdy cele zostaną zaprezentowane na żywych komórkach, a nie tylko w sztucznych testach.
Śledzenie komórek pomocniczych COVID-19 w czasie
Dysponując tą platformą, badacze zeskanowali cały domenę wiążącą receptor białka kolca SARS-CoV-2 oraz inne regiony wirusa w próbkach krwi od 22 osób, które przeszły COVID-19. Dzięki kodom kreskowym i sekwencjonowaniu pojedynczych komórek zarejestrowali 2 188 swoistych dla wirusa limfocytów CD4 i poznali dla każdej komórki, jaki fragment wirusa rozpoznaje, który gen HLA go prezentuje, jak wygląda jego receptor T oraz jakie geny wyraża. Zaobserwowali bogatą mieszankę stanów komórkowych, w tym przypominające pamięć, efektorowe, regulacyjne i podobne do wyczerpanych. Z czasem odpowiedzi przesuwały się ku komórkom pamięci efektorowej, choć w sposób różniący się od wcześniej badanych komórek cytotoksycznych. Zespół stworzył „skorę immunogenności”, łączącą, ile osób i klonów T zareagowało na dany fragment wirusa, jak bardzo te klony się rozrosły i jak długo się utrzymywały. Wyższe wartości tej skali dla fragmentów domeny wiążącej receptor kolca wiązały się z silniejszymi poziomami przeciwciał później, co sugeruje, że te komórki pomocnicze mogą wspierać lepszą jakość przeciwciał.
Wydobywanie komórek pomocniczych HPV pod kątem terapii przeciwnowotworowej
Następnie badacze zwrócili się ku onkologii, koncentrując się na HPV-16, głównej przyczynie raka szyjki macicy i innych nowotworów. Zbudowali bibliotekę obejmującą dwa białka HPV, E6 i E7, używając fragmentów o różnej długości, aby sprawdzić, jak obszary „flankujące” wokół rdzenia wpływają na rozpoznawanie przez limfocyty pomocnicze. Zastosowali tę bibliotekę u pacjentów z zmianami przednowotworowymi, którzy otrzymali terapeutyczne szczepionki przeciw HPV, i zidentyfikowali dziesiątki swoistych limfocytów pomocniczych. Z tych komórek wybrali panel receptorów T do głębszych badań. Niektóre receptory wykazały silne i selektywne odpowiedzi po przeniesieniu do ludzkich komórek T, generując wiele korzystnych sygnałów i zabijając komórki docelowe załadowane fragmentami HPV lub pełnej długości białkiem E6, przy jednoczesnym braku reakcji na podobne białka ludzkie czy szeroki panel innych typów genów HLA. Jeden receptor, oznaczony w badaniu jako H2, wyróżnił się jako obiecujący kandydat do przyszłych terapii z użyciem inżynierowanych komórek T.
Co to znaczy dla przyszłych szczepionek i terapii
Dla czytelnika niebędącego specjalistą kluczowy wniosek jest taki, że autorzy zbudowali coś w rodzaju „wyszukiwarki odporności” dla komórek pomocniczych. Potrafi ona przeszukać całe białka wirusów lub nowotworów, wyłowić rzadkie komórki rozpoznające konkretne fragmenty i jednocześnie ujawnić, jak te komórki się zachowują i jak można je wykorzystać. W kontekście COVID-19 podejście to powiązało pewne fragmenty kolca z mocnymi odpowiedziami komórek pomocniczych i wyższymi poziomami przeciwciał, dostarczając wskazówek do udoskonalania szczepionek. W chorobach związanych z HPV odkryto receptory limfocytów pomocniczych, które wyglądają na wystarczająco silne i bezpieczne, by rozważyć je w ukierunkowanej immunoterapii przeciwnowotworowej. Chociaż potrzebne są dalsze prace, by rozszerzyć metodę na dodatkowe typy genów HLA i większe grupy pacjentów, ta platforma otwiera praktyczną drogę do mapowania i w końcu ukierunkowania pomocniczego ramienia układu odpornościowego w wielu chorobach.
Cytowanie: Zhang, R., Qi, J., McKasson, M. et al. Whole-protein screening and multi-modal profiling of antigen-specific CD4+ T cells at single-cell resolution. Nat Commun 17, 3979 (2026). https://doi.org/10.1038/s41467-026-72396-7
Słowa kluczowe: Limfocyty CD4, profilowanie pojedynczych komórek, odporność na SARS-CoV-2, immunoterapia HPV, receptory komórek T