Clear Sky Science · ru
Структурные и функциональные механизмы, лежащие в основе динамики активационного затвора и доступности мотива IFM в человеческом Nav1.5
Почему важны крошечные «вратца» сердца
Электрический ритм каждого сердцебиения зависит от микроскопических ворот в кардиомиоцитах, которые на доли секунды открываются, позволяя натриевым ионам втереться внутрь. Эти ворота — белки, называемые натриевыми каналами, и при их сбоях возникают опасные нарушения сердечного ритма. В данном исследовании рассматривается главный кардиальный натриевый канал Nav1.5 и выявлено ранее не видимое промежуточное состояние его затвора, а также скрытый ионный карман рядом с ключевым «защёлочным» участком, который выключает канал. Понимание этого механизма в таких подробностях может помочь в разработке более точных и менее побочных лекарств от аритмий.
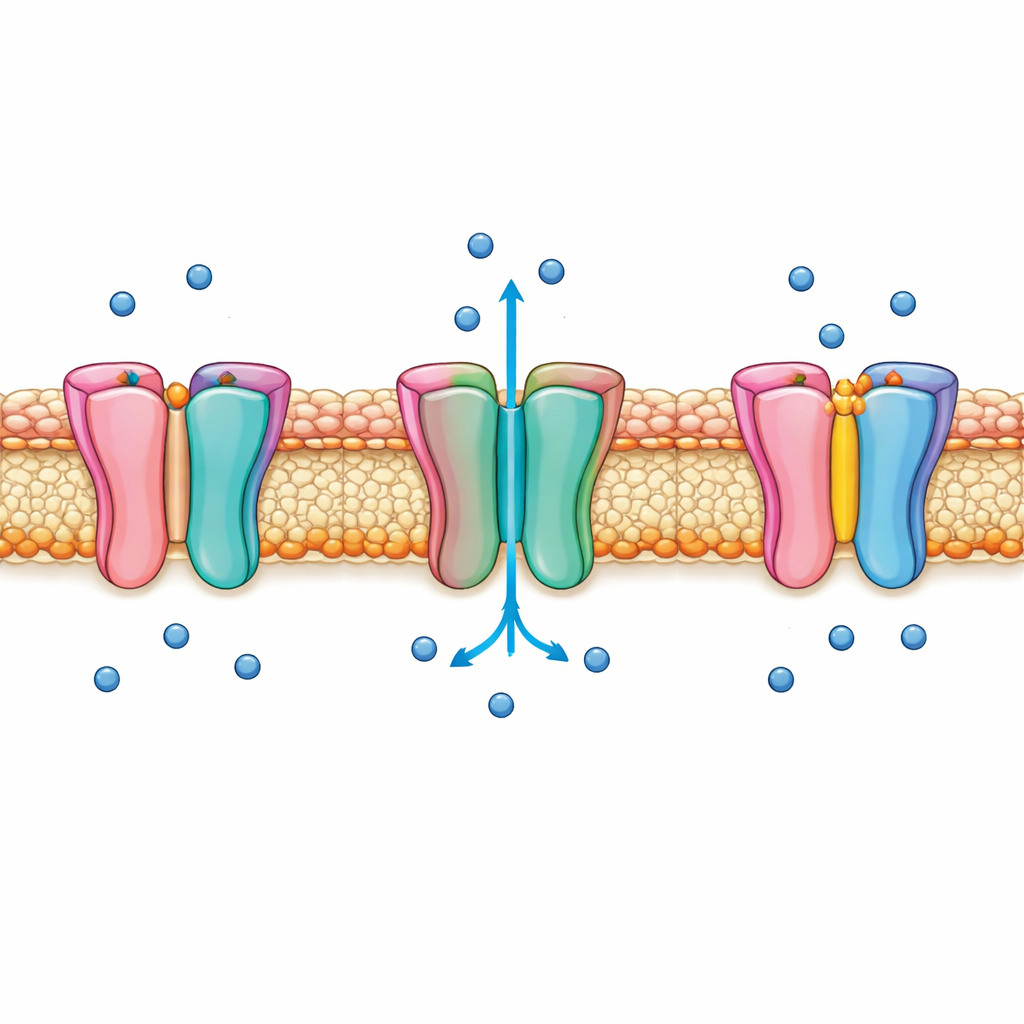
Внимательнее к «дверце» натрия в сердце
Nav1.5 располагается в мембране сердечной клетки и открывается всего на несколько тысячных долей секунды, создавая резкий подъём электрического сигнала, запускающего сокращение. Почти сразу он сам себя отключает в процессе, называемом быстрой инактивацией, предотвращая избыточный приток натрия. В течение десятилетий считалось, что короткий сегмент из трёх аминокислот, прозванный мотивом IFM, действует как пробка, заходя на место и перекрывая поток. Тем не менее многие детали того, как движется главный затвор в основании канала и как мотив IFM фактически управляет этим движением, оставались неясными. Эти пробелы ограничивали попытки разработать лекарства, нацеленные на канал, не нарушая его тонкую временную организацию.
Фиксация промежуточного открытого состояния
С помощью криоэлектронной микроскопии высокого разрешения авторы запечатлели полноразмерный человеческий Nav1.5 в том, что они называют промежуточным открытым состоянием. В этой конфигурации четыре внутренних спирали, формирующие активационный затвор, разошлись настолько, что пропускают гидратированные натриевые ионы, но не так широко, как в ранее описанных полностью открытых структурах. Молекулярные моделирования при приложенном напряжении показали, что вода и ионы натрия могут пересекать пору, хотя только при более высоких напряжениях, чем в полностью открытом канале, что подтверждает проводимость этого состояния и его положение между обычным открытым и инактивированным формами. Молекула детергента, застрявшая в затворе, помогает удерживать это хрупкое устройство, иллюстрируя, как небольшие изменения формы тонко регулируют, пропускает ли канал ионы или остаётся закрытым.
Как боковые контакты управляют затвором
Команда также разрешила поверхность взаимодействия между N‑концевым доменом канала, выступающим внутри клетки, и одной из спиралей, формирующих затвор, известной как S6 в домене I. Определённые заряженные аминокислоты в этих областях образуют солевые мосты, действующие как крошечные защёлки, помогающие стабилизировать открытый затвор. Когда исследователи изменяли эти остатки, общая форма электрических токов менялась: в частности, некоторые мутации замедляли выключение канала после открытия. Дополнительные анализы показали, что спираль S6 может раскачиваться внутрь и наружу, сужая или расширяя затвор. Различные схемы контактов с N‑концевым доменом соответствовали этим сдвигам, связывая микроскопическое движение единственной спирали со способностью канала переключаться между открытыми и более закрытыми, похожими на инактивированные, состояниями.
Скрытый карман рядом с «защёлкой» инактивации
Возможно, самое поразительное открытие обнаружено рядом с самим мотивом IFM. В структуре промежуточного открытия сегмент IFM сохраняет характерную U‑образную позу, плотно встроенный в гидрофобный карман, а не полностью откидывается, как предполагают некоторые модели. Рядом с ним авторы выявили второй карман, выстланный отрицательно заряженными остатками, который удерживает ион натрия. Моделирования и эксперименты указывают, что в эту нишу могут также попадать другие положительно заряженные ионы. Мутации, изменявшие заряд или химию этого кармана, изменяли лёгкость инактивации канала и поведение мотива IFM, что свидетельствует о том, что связывание иона здесь ослабляет или укрепляет «защёлку» IFM без необходимости полного выхода мотива из его гнезда. Такая переинтерпретация помогает объяснить прежние эксперименты, где реактивные ионы могли помечать вживлённые цистеиновые остатки рядом с мотивом IFM, хотя мотив, казалось бы, оставался захороненным.

Что это значит для ритма сердца и будущих лекарств
В совокупности эти результаты обновляют классическую «дверь‑и‑клин» модель инактивации натриевого канала. Вместо простого выдвигающегося и убирающегося пробкового механизма Nav1.5, по-видимому, использует скоординированный «танец»: затвор может находиться в промежуточно‑открытом положении, боковые контакты стабилизируют или расслабляют эту конфигурацию, а близлежащий ионно‑настроенный карман регулирует, насколько плотно мотив IFM удерживает затвор закрытым. Раскрытие этой альтернативной ионо-доступной дорожки и её влияния на переключение открывает уточнённый структурный план того, как кардиальные натриевые каналы дают сбой при заболеваниях, и указывает на новые, более селективные мишени для антиаритмических терапий.
Цитирование: Biswas, R., López-Serrano, A.L., Purohit, A. et al. Structural and functional mechanisms underlying activation gate dynamics and IFM motif accessibility in human Nav1.5. Nat Commun 17, 2820 (2026). https://doi.org/10.1038/s41467-026-69672-x
Ключевые слова: кардиальный натриевый канал, Nav1.5, быстрая инактивация, крио-ЭМ, сердечная аритмия