Clear Sky Science · pl
Mechanizmy strukturalne i funkcjonalne leżące u podstaw dynamiki bramki aktywacyjnej i dostępności motywu IFM w ludzkim Nav1.5
Dlaczego małe „drzwi” serca mają znaczenie
Elektrochemiczne bicie każdego serca zależy od mikroskopijnych „drzwi” w komórkach serca, które na krótko otwierają się, pozwalając na napływ jonów sodu. Te „drzwi” to białka zwane kanałami sodowymi, a gdy zawodzą, mogą powodować groźne zaburzenia rytmu serca. W badaniu skupiono się na głównym kardialnym kanale sodowym, oznaczonym jako Nav1.5, i opisano dotąd niezaobserwowany stan pośredni jego bramki oraz ukrytą kieszeń jonową obok kluczowego „zamka”, który wyłącza kanał. Dogłębne zrozumienie tego mechanizmu może pomóc w projektowaniu lepszych leków na arytmie — działających precyzyjniej i z mniejszą liczbą skutków ubocznych.
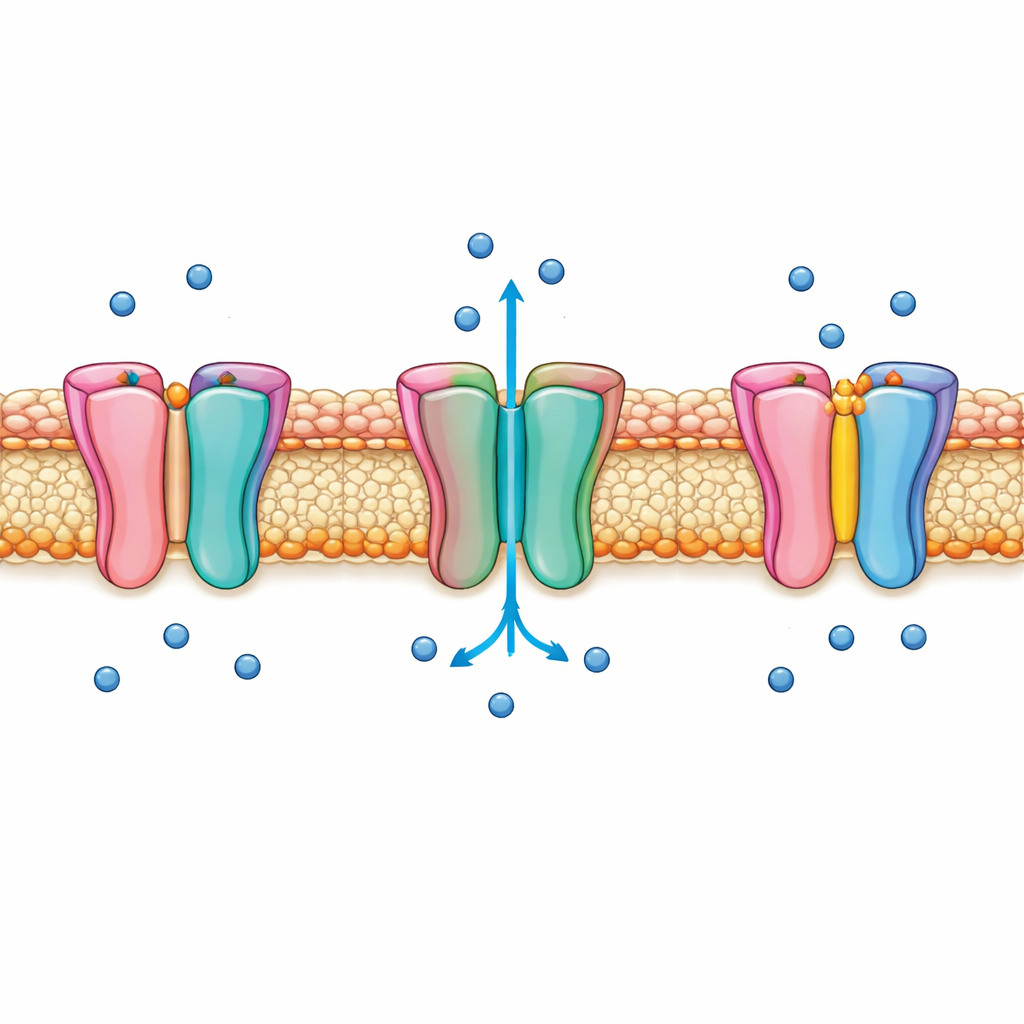
Bliższe spojrzenie na sodowe „drzwi” serca
Nav1.5 osadza się w błonie komórkowej kardiomiocytów i otwiera jedynie na kilka tysięcznych sekundy, generując ostry wzrost sygnału elektrycznego wywołującego skurcz. Niemal natychmiast wyłącza się w procesie zwanym szybką inaktywacją, zapobiegając nadmiernemu napływowi sodu. Od dekad krótki trójaminokwasowy fragment, określany jako motyw IFM, uważano za wtyczkę, która wsuwa się na miejsce, aby zatrzymać przepływ. Jednak wiele szczegółów dotyczących ruchu głównej bramki u podstawy kanału oraz sposobu, w jaki motyw IFM kontroluje ten ruch, pozostawało niejasnych. Luki te utrudniały projektowanie leków celujących w kanał bez zaburzania jego precyzyjnego czasu pracy.
Uchwycenie stanu pośrednio otwartego
Wykorzystując wysokorozdzielczą krioelektronową mikroskopię, autorzy zarejestrowali pełnometrażowy ludzki kanał Nav1.5 w tym, co opisują jako stan pośrednio otwarty. W tej konfiguracji cztery wewnętrzne helisy tworzące bramkę aktywacyjną są rozstawione na tyle, by umożliwić przejście uwodnionym jonów sodu, ale nie tak szeroko jak w dotychczas opisanych w pełni otwartych strukturach. Symulacje molekularne przy przyłożonym napięciu wykazały, że woda i jony sodu mogą przepływać przez pore, choć tylko przy wyższych napięciach niż w kanale całkowicie otwartym, co potwierdza, że stan ten przewodzi, lecz znajduje się między typowymi stanami otwartym i inaktywowanym. Cząsteczka detergentu osadzona przy bramce pomaga utrzymać tę delikatną konfigurację, ilustrując, jak małe zmiany kształtu mogą precyzyjnie regulować, czy kanał przepuszcza jony, czy pozostaje zamknięty.
Jak boczne kontakty kontrolują bramkę
Zespół rozwiązał również powierzchnię interakcji między domeną N‑terminalną kanału, która zwisa wewnątrz komórki, a jedną z helis formujących bramkę, znaną jako S6 w domenie I. Konkretne naładowane aminokwasy w tych rejonach tworzą mostki solne działające jak drobne zamki stabilizujące otwartą bramkę. Gdy badacze zmieniali te reszty, ogólny kształt prądów elektrycznych ulegał zmianie: w szczególności niektóre mutacje spowalniały tempo wyłączania kanału po otwarciu. Dalsze analizy wykazały, że helisa S6 może wychylać się do wnętrza i na zewnątrz, zwężając lub rozszerzając bramkę. Różne wzorce kontaktów z domeną N‑terminalną odpowiadały tym przesunięciom, łącząc mikroskopijny ruch pojedynczej helisy z zdolnością kanału do przełączania się między stanem otwartym a bardziej zamkniętymi, przypominającymi inaktywację kształtami.
Ukryta kieszeń obok zamka inaktywacji
Być może najbardziej uderzające odkrycie znajduje się obok samego motywu IFM. W strukturze pośrednio otwartej segment IFM zachowuje charakterystyczną U‑kształtną pozycję dobrze zadokowaną w hydrofobowym zagłębieniu, zamiast całkowicie odchylać się, jak sugerują niektóre modele. Obok niego autorzy zidentyfikowali jednak drugą kieszeń wyścieloną ujemnie naładowanymi resztami, która mieści jon sodu. Symulacje i eksperymenty sugerują, że inne dodatnio naładowane jony również mogą zajmować tę niszę. Mutacje zmieniające ładunek lub chemię tej kieszeni wpływały na skłonność kanału do inaktywacji i na zachowanie motywu IFM, wskazując, że związanie jonu tutaj poluzowuje lub usztywnia „zaczep” IFM bez konieczności całkowitego opuszczenia jego gniazda. Ta reinterpretacja pomaga wyjaśnić wcześniejsze eksperymenty, w których reaktywne jony mogły znakować wprowadzone cysteiny w pobliżu motywu IFM, mimo że motyw wydawał się pozostawać ukryty.

Znaczenie dla rytmu serca i przyszłych leków
W sumie wyniki te aktualizują klasyczny obraz „drzwi‑i‑klin” inaktywacji kanału sodowego. Zamiast prostego wtykania i wyciągania, Nav1.5 wydaje się wykorzystywać skoordynowany układ: bramkę, która może zajmować pozycję pośrednio otwartą, boczne kontakty stabilizujące lub rozluźniające tę konfigurację oraz pobliską kieszeń regulowaną jonami, która dostosowuje, jak mocno motyw IFM trzyma bramkę zamkniętą. Ujawniając tę alternatywną ścieżkę dostępu jonów i jej wpływ na sterowanie bramkowaniem, praca dostarcza dopracowanego modelu strukturalnego wyjaśniającego, jak kanały sodowe serca zawodzą w chorobie, i wskazuje nowe, bardziej selektywne cele dla terapii przeciwarytmicznych.
Cytowanie: Biswas, R., López-Serrano, A.L., Purohit, A. et al. Structural and functional mechanisms underlying activation gate dynamics and IFM motif accessibility in human Nav1.5. Nat Commun 17, 2820 (2026). https://doi.org/10.1038/s41467-026-69672-x
Słowa kluczowe: kanał sodowy serca, Nav1.5, szybka inaktywacja, cryo-EM, arytmia serca